

河北省秦皇岛市青龙满族自治县部分学校联考2023-2024学年高三上学期12月月考化学试题
展开
这是一份河北省秦皇岛市青龙满族自治县部分学校联考2023-2024学年高三上学期12月月考化学试题,共24页。试卷主要包含了选择题,填空题等内容,欢迎下载使用。
分值:100分 考试时间:75分钟
第I卷 选择题(共39分)
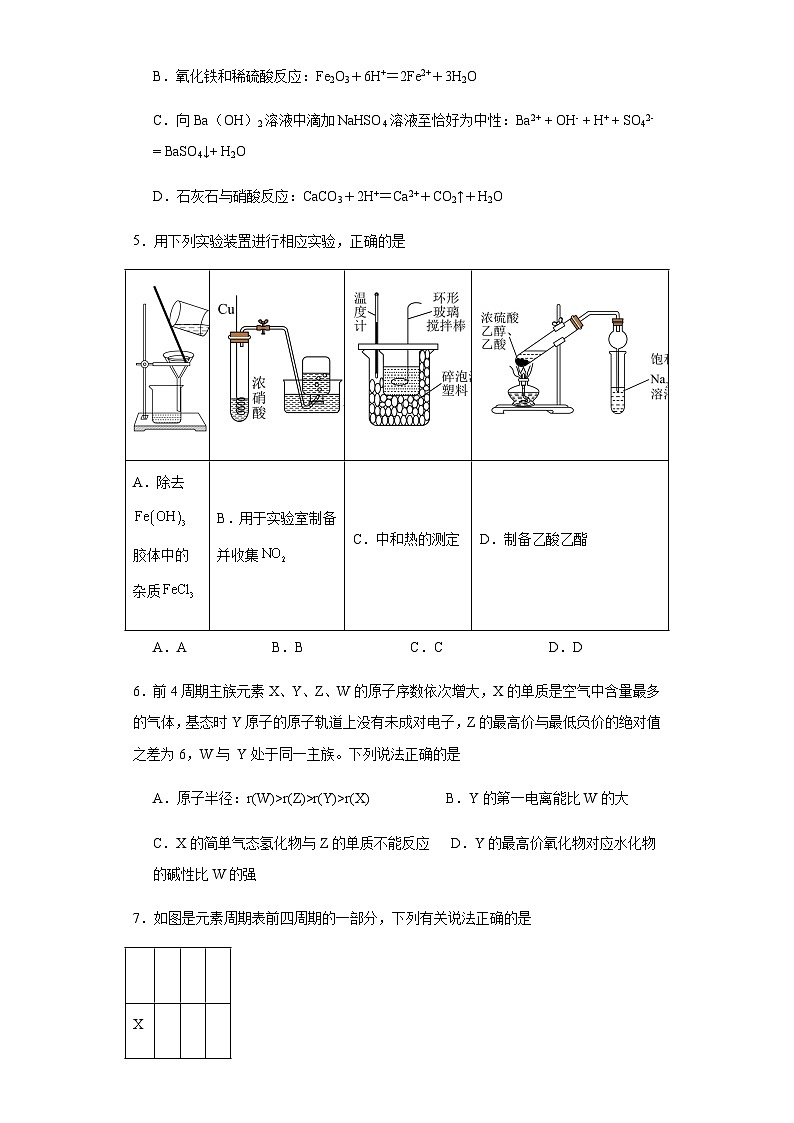
一、选择题(共14小题,每小题3分,共42分。每小题只有一个选项符合题意)
1.化学与能源开发、环境保护、资源利用、食品安全等密切相关,下列说法正确的是
A.自来水生产中应尽量用氯气消毒
B.充分利用地沟油提炼食用油,提高原料利用率
C.添加硫酸铁制“铁强化酱油”,添加碘酸钾制加碘盐
D.高纯硅及其氧化物在太阳能电池及信息高速传输中有重要应用
2.下列有关氢化物的叙述中正确的是( )
A.稳定性:H2Sr(Z)>r(Y)>r(X) B.Y的第一电离能比W的大
C.X的简单气态氢化物与Z的单质不能反应 D.Y的最高价氧化物对应水化物的碱性比W的强
7.如图是元素周期表前四周期的一部分,下列有关说法正确的是
A.电负性:W>X B.第一电离能:W2Q1
第Ⅱ卷 非选择题(共58分)
二、填空题(本题包括4个小题,共58分)
15.(11分)实验室用燃烧法测定某种氨基酸的分子组成。取Wg该种氨基酸放在纯氧气中燃烧,燃烧后生成的的体积用F装置进行测量,所需装置如下图夹持仪器及部分加热装置已略去:
(1)该实验装置的合理连接顺序为:A、C、 、F。(装置可以重复选用)
(2)实验开始时,首先打开止水夹a,关闭止水夹b,通一段时间的纯氧,这样做的目的是 。
(3)燃烧管D中放入CuO的作用是 ,装置B的作用是 。
(4)为了确定此氨基酸的分子式,除了准确测量N2的体积外,还需得到的数据有 (填字母)。
A.该氨基酸的摩尔质量 B.生成二氧化碳气体的质量
C.生成水的质量 D.通入O2的体积
(5)在读取F装置中所排水的体积时,液面左低右高,则所测气体的体积 (填“偏大”、“偏小”或“无影响”)。
(6)已知分子式为的有机物也含有氨基酸中的某个官能团,请设计实验证明该官能团试剂任选 。
16.(15分)研究表明丰富的CO2完全可以作为新碳源,解决当前应用最广泛的碳 源(石油和天然气)到本世纪中叶将枯竭的危机,同时又可缓解由CO2累积所产生的温室效应,实现CO2的良性循环。
(1)目前工业上有一种方法是用CO2和H2在230℃催化剂条件下转化生成甲醇蒸汽和水蒸气。下图表示恒压容器中0.5 ml CO2和1.5 ml H2转化率达80%时的能量变化示意图。能判断该反应达到化学平衡状态的依据是 。
a.容器中压强不变
b.H2的体积分数不变
c.c(H2)=3c(CH3OH)
d.容器中密度不变
e.2个C=O断裂的同时有6个H-H断裂。
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应
CO(g)+H2O(g)CO2(g)+H2(g),得到如下三组数据:
①实验2条件下平衡常数K= 。
②实验3中,若平衡时,CO的转化率大于水蒸气,则a/b 的值 (填具体值或取值范围)。
③实验4,若900℃时,在此容器中加入CO、H2O、CO2、H2均为1ml,则此时V正 V逆(填“”,“=”)。
(3)已知在常温常压下:
①2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH=-1275.6 kJ/ml
②2CO (g)+ O2(g) = 2CO2(g) ΔH=-566.0 kJ/ml
③H2O(g) = H2O(l) ΔH=-44.0 kJ/ml
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式: 。
(4)已知草酸是一种二元弱酸,草酸氢钠(NaHC2O4)溶液显酸性。常温下,向10 mL 0.01 ml·L-1 H2C2O4溶液中滴加10mL 0.01ml·L-1 NaOH溶液时,比较溶液中各种离子浓度的大小关系 ;
(5)以甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池的负极反应式为 ;
17.(16分)1774年,瑞典化学家舍勒在研究软锰矿(主要成分MnO2,含有少量的Al、Si、Fe等的氧化物)的过程中,将其与某酸混合加热,产生了一种黄绿色气体。二氧化锰是一种重要的化工原料,以软锰矿为原料制取MnO2的一种工艺流程如图:
已知:①室温下,Ksp[Al(OH)3]=1×10-32,Ksp[Fe(OH)3]=1×10-38
②Mn2+开始沉淀生成Mn(OH)2时pH=7.3
(1)将软锰矿研磨的目的是
(2)用软锰矿制取黄绿色气体的化学方程式为:
(3)滤渣1的成分为: (用化学式表示)。
(4)“氧化"时,如何检验Fe2+是否被完全氧化:
(5)室温时,“调pH除杂"除去MnSO4溶液中的Fe3+、Al3+(使其浓度小于1×10-5ml/L),需要调节pH的范围为:
(6)工业上通过电解硫酸锰溶液制备二氧化锰,产生二氧化锰的电极是: (填“阳极”或“阴极”)。
(7)写出二氧化锰与熔融苛性钾在空气中反应生成锰酸钾(K2MnO4)的化学方程式:
(8)二氧化锰可用于制备干电池和涂料等,已知碱性锌锰电池总反应为:Zn+2H2O+2MnO2=Zn(OH)2+2MnO(OH),写出电池的正极反应式: 。
18.(16分)氧氮杂环是新药研制过程中发现的一类重要活性物质,有抗肿瘤功效。下面是某研究团队提出的一种氧氮杂环类化合物F的合成路线:
已知:+
回答下列问题:
(1)A的名称是 ,B中含氧官能团的名称是羧基、 ,E中手性碳原子的数目为 。
(2)根据C的结构特征,分析预测其可能的化学性质,完成下表。
(3)B有多种同分异构体,满足以下条件的同分异构体有 种。
①仅含苯环一个环状结构,且苯环上仅有2个取代基
②仅含2种官能团且能发生银镜反应
③不含,不含.
其中核磁共振氢谱有三组吸收峰,峰面积之比为3∶2∶2的一种同分异构体结构简式 。
(4)参照上述合成路线和信息,写出由 和为原料合成 的路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件,无机试剂任选) 。
A.除去胶体中的杂质
B.用于实验室制备并收集
C.中和热的测定
D.制备乙酸乙酯
X
W
Y
R
Z
实验组
温度℃
起始量/ml[
平衡量/ml
达到平衡所需
时间/min
CO
H2O
H2
CO
1
650
4
2
1.6
2.4
6
2
900
2
1
0.4
1.6
3
3
900
a
b
c
d
t
序号
结构特征
反应的试剂、条件
反应形成的新结构或产物
反应类型
①
、
还原反应
②
M的结构简式
D
反应
③
硫酸、加热
B和乙醇
取代反应
参考答案:
1.D
【详解】A、自来水生产中用氯气消毒,余氯对人有害,A项错误;
B、地沟油提炼出的食用油对人体有害,B项错误;
C、“铁强化酱油”是指是在酱油中添加高吸收的铁剂钠铁EDTA,C项错误;
D、高纯硅及其氧化物在太阳能电池及信息高速传输中有重要应用,D项正确;
答案选D。
2.A
【详解】A.元素的非金属性越强,其气态氢化物的稳定性更强。F的非金属性比S的强,则HF的稳定性比H2S的强,A项正确;
B.HCl为共价化合物,其电子式为,B项错误;
C.1个D2O分子,1个D原子中有1个中子,1个O原子有8个中子,则1个D2O分子中共1×2+8=10个中子,C项错误;
D.卤化氢中,HF由于分子间可形成氢键,其沸点最高,D项错误;
本题答案选A。
3.B
【详解】A.根据结构式,每个铝原子形成3个共价键、1个配位键,即1ml Al2Cl6分子中含配位键的数目为2NA,A错误;
B.NaClO溶液中存在水解平衡:,加水,平衡正向移动,ClO−的水解程度增大,而溶液体积增大,溶液碱性减弱,B正确;
C.反应2BaO2(s)2BaO(s)+O2(g)达到平衡后压缩体积,平衡逆向移动,反应达到新平衡后由于温度不变,K不变,故c(O2)不变,C错误;
D.被保护的钢铁设备作阴极,用活性电极作辅助阳极,该方法为牺牲阳极的阴极保护法,D错误;
故选B。
4.D
【详解】A. NH4HCO3溶液与过量KOH浓溶液共热反应生成碳酸钾、氨气和水,离子方程式为:NH4++ 2OH-+HCO3-NH3↑+ 2H2O+CO32-,故A错误;
B. 氧化铁和稀硫酸反应生成硫酸铁和水,离子方程式为:Fe2O3+6H+=2Fe3++3H2O,故B错误;
C. 向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性,则反应生成硫酸钡、硫酸钠和水,离子方程式为:Ba2+ + 2OH- +2 H+ + SO42- = BaSO4↓+ 2H2O,故C错误;
D. 石灰石与硝酸发生复分解反应,生成硝酸钙、二氧化碳和水,离子方程式为:CaCO3+2H+=Ca2++CO2↑+H2O,故D正确,
故选D。
5.D
【详解】A.胶体中的胶体粒子及杂质的离子都能够通过滤纸,不能采用过滤的方法分离提纯,应该采用渗析方法提纯胶体,A错误;
B.铜和浓硝酸可以生成,但和水反应生成硝酸和NO,不能用排水法收集,B错误;
C.中和热的测定中,温度计应该插入溶液中以测量溶液的温度变化,C错误;
D.乙醇、乙酸和浓硫酸共热可以制取乙酸乙酯,用饱和碳酸钠溶液收集生成的乙酸乙酯,同时除去杂质乙酸和乙醇,用图示装置可以防止倒吸,D正确;
故选D。
6.B
【分析】前4周期主族元素X、Y、Z、W的原子序数依次增大,X的单质是空气中含量最多的气体,则X为N元素;基态时Y原子的原子轨道上没有未成对电子,其电子排布式为1s22s22p63s2,则Y为Mg元素;W与 Y处于同一主族,则W为Ca元素;Z的最高价与最低负价的绝对值之差为6,则Z为Cl元素。
【详解】A.同一周期从左到右,原子半径逐渐减小;同一主族从上到下,原子半径逐渐增大,则原子半径:r(W)>r(Y)>r(Z)>r(X),A项错误;
B.同一主族从上到下,第一电离能逐渐减小,则Y的第一电离能比W的大,B项正确;
C.X的简单气态氢化物为NH3,Z的单质为Cl2,二者可以发生氧化还原反应,C项错误;
D.元素的金属性越强,其最高价氧化物对应水化物的碱性越强,金属性:W>Y,则Y的最高价氧化物对应水化物的碱性比W的弱,D项错误;
答案选B。
7.D
【分析】根据元素在周期表中的位置可知,R为元素、Z为元素、Y为S元素、W为P元素、X为N元素。
【详解】A.同周期元素,从左到右,电负性呈增大趋势,同主族元素,从上到下,电负性呈减小趋势,所以电负性: ,故A项错误;
B.同周期元素,从左到右,第一电离能呈增大趋势,但第VA族元素的第一电离能大于同周期相邻元素的第一电离能,所以第一电离能: ,故B项错误;
C.在常温下为液体,而S和P在常温下为固体,所以五种元素的单质中,沸点最高的不是,故C项错误;
D.R同主族下一周期元素的原子为36,R与其同主族下一周期元素的原子序数相差18,故D项正确;
答案选D。
8.B
【详解】A. 由X的结构可知,其分子式为C5H4O2N3F,A项正确;
B. 由Z的结构可知,其结构中含有2个氯原子,1个硝基,一个酚羟基,一个肽键,一共4种官能团,B项错误;
C. 与4个不一样的原子或原子团相连接的碳原子为手性碳原子,则手性碳原子必须为饱和碳原子,由此可知Y分子中含有4个手性碳原子,C项正确;
D. 由X和Z的结构可知,X和Z中都含有肽键,所以都能发生水解反应;X中含有碳碳双键可以发生加成反应,Y中含有苯环也可以发生加成反应,D项正确;
答案选B。
9.D
【详解】A.在氮化铝的合成反应中,N2是氧化剂,C为还原剂,Al2O3既不是氧化剂,也不是还原剂,A正确;
B.N2是氧化剂,C为还原剂,氧化剂与还原剂物质的量比是1:3,B正确;
C.N元素化合价降低,N2为氧化剂,AlN是还原产物,C正确;
D.上述反应中N元素化合价由0价降低到-3价,每生成1ml AlN,N2得到3ml电子,D错误;
故答案选D。
10.C
【详解】A.明矾即KAl(SO4)2·12H2O其电离出的Al3+水解形成的Al(OH)3胶体能吸附水中的悬浮物,可用于水的净化,A正确;
B.由于Zn比Fe活泼,则在海轮外壳上镶入锌块,可以形成牺牲阳极的阴极保护法,从而可减缓船体的腐蚀速率,B正确;
C.电解NaCl饱和溶液,反应为:2NaCl+2H2O2NaOH+H2↑+Cl2↑,则得不到金属钠,应该电解熔融的氯化钠才可制得金属钠,C错误;
D.2NO(g)+2CO(g)=N2(g)+2CO2(g)在常温下能自发进行,由于该反应是一个气体体积减小的反应即熵减的反应,则该反应的△H c(OH-) CH3OCH3+16OH-—12e-=2CO32-+11H2O
【详解】试题分析:(1)CO2和H2在230℃催化剂条件下转化生成甲醇蒸汽和水蒸气的化学方程式为:CO2+3H2CH3OH+ H2O,反应是在恒压条件下进行,压强保持不变,故不能用压强来判断是否达到平衡,a错;H2的体积分数不变,说明H2的浓度不再改变,反应达到了平衡状态,b对;c(H2)=3c(CH3OH)不能说明浓度不再改变,不能判断是否达到平衡,c错;气体的总质量不变,由于是在恒压下反应,所以如果没有达到平衡,体积就会发生改变,密度也会改变,现密度不变说明反应达到了平衡,d对;不管反应在任何时候2个C=O断裂的同时有6个H-H断裂,e错,选bd。
(2)①根据表中数据有:
CO(g)+H2O(g)CO2(g)+H2(g),
n(起始) 2 1 0 0
n(变化) 0.4 0.4 0.4 0.4
n(平衡) 1.6 0.6 0.4 0.4 两边的气体系数相等,平衡常数为K=(0.4×0.4)÷(1.6×0.6)=1/6;②CO的转化率要大于水蒸气,相当于增大水蒸气的浓度,那么a/bK=1/6,反应向逆向进行,故V正 c(HC2O4-)> c(H+)> c(C2O42-) > c(OH-)。(5)燃料电池中燃料反应的一极是负极,氧气在正极反应,所以负极是甲醚发生反应,由于是碱性电解质溶液,故生成的CO2会与碱反应生成CO32-,电极反应为:CH3OCH3+16OH—-12e- =2CO32- +11H2O
考点:化学平衡状态的判断、化学平衡常数的计算、盖斯定律的应用、燃料电池的电极反应的书写。
17.(1)增大接触面积,增大与酸反应的速率,提高浸出率
(2)MnO2+4HCl(浓)MnCl2+Cl2+2H2O
(3)SiO2
(4)取少量氧化后的溶液于试管中,滴入1-2滴铁氰化钾溶液,若出现蓝色沉淀则表明Fe2+未被完全氧化,反之未出现蓝色沉淀,表明Fe2+已被完全氧化
(5)5≤pH
相关试卷
这是一份109,河北省秦皇岛市青龙满族自治县青龙部分学校2023-2024学年高三上学期1月期末化学试题,共17页。试卷主要包含了选择题,填空题等内容,欢迎下载使用。
这是一份19,河北省秦皇岛市青龙满族自治县青龙部分学校2023-2024学年高三上学期1月期末化学试题,共11页。试卷主要包含了选择题,填空题等内容,欢迎下载使用。
这是一份河北省秦皇岛市青龙满族自治县青龙部分学校2023-2024学年高一上学期1月期末联考化学试题(含答案),共12页。试卷主要包含了选择题,填空题等内容,欢迎下载使用。










