

高中苏教版 (2019)第三单元 海洋化学资源的综合应用当堂检测题
展开1.碘元素在下列物质中以单质存在的是( )
A.碘酒B.海带
C.含碘食盐D.人工降雨剂
2.现有三组溶液:①汽油和氯化钠溶液 ②碘的CCl4溶液
③氯化钠和单质溴的水溶液,分离以上各混合物的正确方法依次是( )
A.萃取、蒸发、分液
B.分液、蒸馏、萃取
C.分液、萃取、蒸馏
D.蒸馏、萃取、分液
3.实验室用水浸取干海带制取纯碘主要包含的步骤有:
①通氯气氧化
②用CCl4萃取分液
③在碘的CCl4溶液中加入NaOH溶液反萃取(转化为NaI和NaIO3)并分液
④水相用硫酸酸化分离出粗碘
⑤干燥后加适量KI固体(将IBr和ICl转化为I2、KBr及KCl)混匀加热得纯碘等。选择下列装置进行实验:
下列说法错误的是( )
A.步骤①可利用甲装置氧化I-
B.步骤②③分液操作时可用乙装置:从下口先放出有机相,再放出水相
C.步骤④可用丙装置将碘与母液分离
D.步骤⑤可用丁装置升华法提纯碘
4.从海水中提取镁的工业生产流程如下:
海水Mg(OH)2MgCl2·6H2OMgCl2Mg
下列说法中错误的是( )
A.此法的优点之一是原料来源丰富
B.该提取镁的过程中复分解反应只发生了一次
C.步骤①②③的目的是从海水中提取无水MgCl2
D.步骤②中加盐酸的离子方程式为Mg(OH)2+2H+===Mg2++2H2O
5.下列物质的性质与应用对应关系不正确的是( )
A.氧化镁的熔点高,可作优质的耐高温材料
B.钠具有强还原性,可用于制取钛、锆等金属
C.氯气有强氧化性,可用氯气漂白干燥有色布条
D.NaHCO3可与盐酸反应,小苏打可用于治疗胃酸过多症
6.某课外小组将灼烧海带产生的灰烬浸泡后过滤,得到澄清的滤液。他们设计了如下几个方案,你认为能证明海带灼烧后的灰烬中含有碘元素的是( )
A.取适量滤液,蒸干,观察是否有紫色固体生成
B.取适量滤液,加入苯,振荡,静置,苯层无色,证明不含碘元素
C.取适量滤液,向其中加入淀粉溶液,无明显现象,证明不含碘元素
D.取适量滤液,加入酸化的H2O2溶液,再加入淀粉溶液,溶液呈蓝色证明含有碘元素
7.碘及其化合物广泛用于医药、染料等方面。中国海洋大学提出一种从海带中提取碘的方法,其流程如图。下列说法错误的是( )
海带海带灰含I-溶液氧化碘水碘的CCl4溶液碘单质
A.操作①的目的是分解除去其中的有机化合物
B.操作②用到的玻璃仪器有漏斗、烧杯、玻璃棒
C.操作④的名称为萃取分液,CCl4可以用苯、酒精等代替
D.操作⑤可以为蒸馏
8.镁着火时,可用来灭火的物质是( )
A.N2B.CO2
C.沙土D.煤油
9.从海水中提取部分物质的过程如图所示,下列有关说法正确的是( )
A.在粗盐中含有Mg2+、SO42-、Ca2+等杂质,加入除杂试剂的顺序为Na2CO3溶液→NaOH溶液→BaCl2溶液→盐酸
B.母液到无水MgCl2的一系列变化中涉及氧化还原反应
C.工业上一般用电解氯化镁溶液的方法制取Mg单质
D.③和⑤均涉及反应:2Br-+Cl2===Br2+2Cl-,该反应属于置换反应
二、关键能力提升
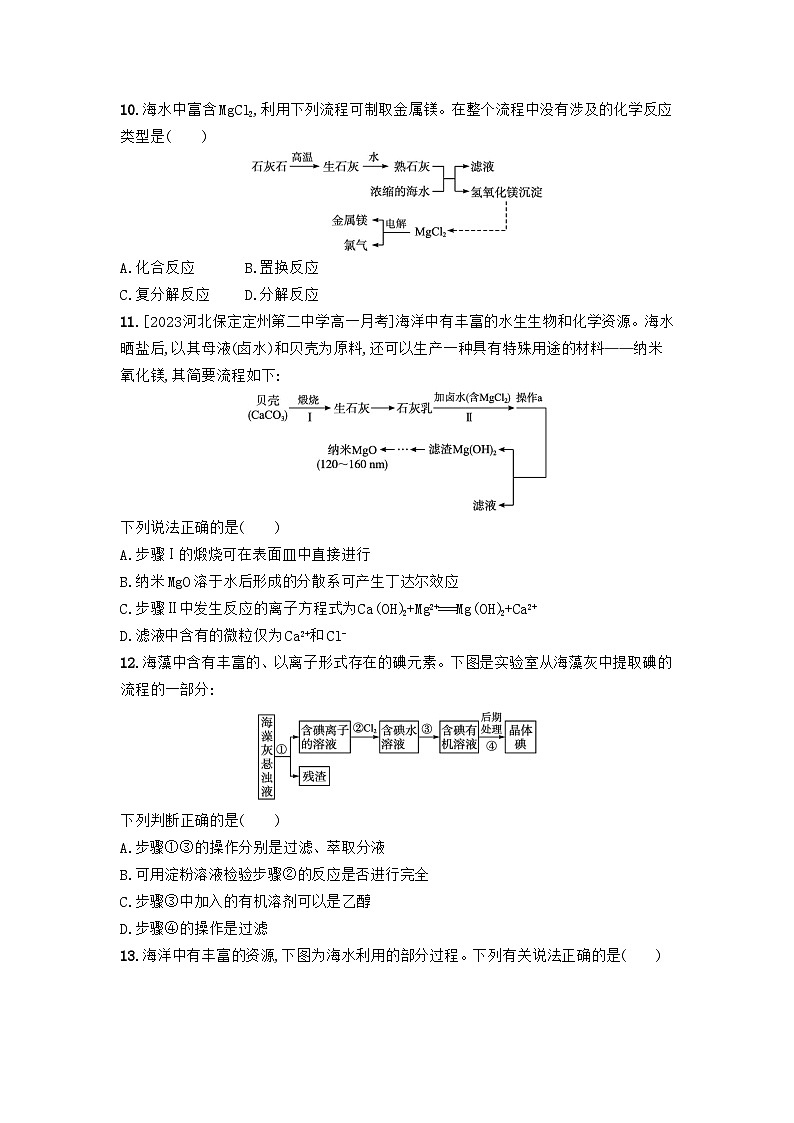
10.海水中富含MgCl2,利用下列流程可制取金属镁。在整个流程中没有涉及的化学反应类型是( )
A.化合反应B.置换反应
C.复分解反应D.分解反应
11.[2023河北保定定州第二中学高一月考]海洋中有丰富的水生生物和化学资源。海水晒盐后,以其母液(卤水)和贝壳为原料,还可以生产一种具有特殊用途的材料——纳米氧化镁,其简要流程如下:
下列说法正确的是( )
A.步骤Ⅰ的煅烧可在表面皿中直接进行
B.纳米MgO溶于水后形成的分散系可产生丁达尔效应
C.步骤Ⅱ中发生反应的离子方程式为Ca(OH)2+Mg2+===Mg(OH)2+Ca2+
D.滤液中含有的微粒仅为Ca2+和Cl-
12.海藻中含有丰富的、以离子形式存在的碘元素。下图是实验室从海藻灰中提取碘的流程的一部分:
下列判断正确的是( )
A.步骤①③的操作分别是过滤、萃取分液
B.可用淀粉溶液检验步骤②的反应是否进行完全
C.步骤③中加入的有机溶剂可以是乙醇
D.步骤④的操作是过滤
13.海洋中有丰富的资源,下图为海水利用的部分过程。下列有关说法正确的是( )
A.由反应①可知:相同温度下,NaHCO3的溶解度大于Na2CO3
B.反应②的离子方程式为Br2+SO2+2H2O===SO42-+2Br-+4H+
C.可通过电解MgCl2溶液的方法制得金属镁
D.粗盐中含有的Mg2+、SO42-等杂质离子,可通过依次加入BaCl2溶液、NaOH溶液、盐酸等试剂加以去除
14.下列有关从海带中提取碘的实验原理和装置能达到实验目的的是( )
A.用装置甲灼烧碎海带
B.用装置乙过滤海带灰的浸泡液
C.用装置丙制备用于氧化浸泡液中I-的Cl2
D.用装置丁吸收氧化浸泡液中I-后的Cl2尾气
15.人造光卤石(KCl·MgCl2·6H2O)是盐化工生产的中间产物。以光卤石为原料制得金属镁,可通过下列步骤实现:①过滤 ②溶解 ③加入适量Ca(OH)2 ④蒸发 ⑤用盐酸溶解 ⑥电解熔融MgCl2 ⑦在HCl气流中强热MgCl2·6H2O晶体。正确的顺序是( )
A.⑤③①②④⑥⑦B.②③①⑤④⑦⑥
C.②④①③⑦⑤⑥D.⑤③①④②⑦⑥
16.工业“从海水中提取镁”的流程图如图:
请根据图示回答以下问题:
(1)过滤操作需要的玻璃仪器有漏斗、 、玻璃棒。
(2)滤液b中含有H2O、 等物质(填两种物质的化学式即可)。
(3)流程图中操作c的名称为 。
(4)写出反应a的化学方程式: 。
17.海洋是资源的宝库,海水中所含食盐高达4×1016 t。从海水中可提取食盐、金属镁或镁的化合物,其过程如图所示:
请回答:
(1)贝壳主要成分的化学式是 。
(2)步骤④反应的离子方程式是 。
(3)实验室由粗盐结晶制精盐的操作包括溶解、过滤、蒸发等步骤,粗盐提纯过程中过滤的目的是 (填序号)。
①获得NaCl晶体
②除去难溶性物质
③除去易挥发物质
④除去可溶性物质
过滤需要用到的玻璃仪器有玻璃棒、 、 。
(4)电解MgCl2制金属Mg的化学方程式为MgCl2(熔融)Mg+Cl2↑,电解0.2 ml MgCl2可生成金属Mg g,同时可得到标准状况下的氯气 L。
18.海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验(苯是一种不溶于水,密度比水小的有机溶剂):
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是 (填字母)。
A.烧杯B.坩埚
C.表面皿D.泥三角
E.酒精灯F.干燥器
(2)步骤③的实验操作名称是 ;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是 。
(3)步骤⑤是萃取、分液,某学生选择用苯来提取碘的理由是 。
在分液操作中,应充分振荡,然后静置,待分层后 (填字母),以下略。
A.直接将含碘苯溶液从分液漏斗上口倒出
B.直接将含碘苯溶液从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将含碘苯溶液从下口放出
D.先将水层从分液漏斗的下口放出,再将含碘苯溶液从上口倒出
参考答案
一、必备基础知识
1.A 解析 单质碘溶解在酒精中得到碘酒,A符合题目要求;海带中碘元素以化合态的形式存在,B不符合题目要求;含碘食盐中碘元素以碘酸钾的形式存在,C不符合题目要求;人工降雨剂中碘元素以碘化银的形式存在,D不符合题目要求。
2.B
3.B 解析 步骤①可用甲装置通入氯气氧化I-,A项正确;步骤②③为分液操作,有机相在下层,先放出有机相,再从上口倒出水相,B项错误;④水相用硫酸酸化后生成碘单质,可利用过滤法分离出粗碘,C项正确;步骤⑤可用丁装置升华提纯碘,D项正确。
4.B 解析 此法的原料是贝壳、海水,优点之一是原料来源丰富,故A正确;该提取镁的过程中步骤①和②都发生了复分解反应,B错误;由流程图可知步骤①②③的目的是从海水中提取无水MgCl2,故C正确;步骤②主要发生氢氧化镁和盐酸的反应,属于离子反应,离子方程式为Mg(OH)2+2H+===Mg2++2H2O,故D正确。
5.C 6.D
7.C 解析 从流程图分析可知,操作①是灼烧,操作②是过滤,操作③通入氯气氧化I-得到I2,操作④是萃取和分液,操作⑤是蒸馏,据此分析解答。
由题图可知,操作①为灼烧,目的是分解除去其中的有机化合物,故A正确;由分析可知,操作②为过滤,用到的玻璃仪器有漏斗、烧杯、玻璃棒,故B正确;由分析可知,操作④为萃取分液,酒精和水混溶,不能作萃取剂,故C错误;由分析可知,操作⑤为蒸馏,故D正确。
8.C 解析 A项,3Mg+N2Mg3N2,N2不能用于镁燃烧时的灭火物质;B项,2Mg+CO22MgO+C,CO2不能用于镁燃烧时的灭火物质;C项,沙土不燃烧且和镁不反应,沙土可用于镁燃烧时的灭火物质;D项,煤油能燃烧,不能用作灭火物质。
9.D 解析 在粗盐中含有Mg2+、SO42-、Ca2+等杂质,加入Na2CO3溶液的目的是除去Ca2+和过量的Ba2+,应在BaCl2溶液之后加,故A错误;母液到无水MgCl2的一系列变化中,没有元素化合价变化,不涉及氧化还原反应,故B错误;工业上一般用电解熔融氯化镁的方法制取Mg单质,故C错误;③和⑤都是氯气把Br-氧化为Br2,涉及反应的离子方程式是2Br-+Cl2===Br2+2Cl-,该反应属于置换反应,故D正确。
二、关键能力提升
10.B
11.C 解析 固体煅烧应该在坩埚中进行,因此步骤Ⅰ的煅烧不能在表面皿中直接进行,A错误;纳米MgO的微粒直径超过100 nm,溶于水后形成的分散系不是胶体,不能产生丁达尔效应,B错误;步骤Ⅱ沉淀镁离子,其中发生反应的离子方程式为Ca(OH)2+Mg2+===Mg(OH)2+Ca2+,C正确;滤液中含有的微粒主要为Ca2+和Cl-,还含有少量镁离子等,D错误。
12.A 解析 ①分离悬浊液可通过过滤除去不溶物,③是将水中的碘单质萃取到有机层中,操作为萃取分液,A正确;淀粉可检验碘单质是否生成,检验②中反应是否进行完全,应检验溶液中是否含有碘离子,若无碘离子则证明反应完全,B错误;萃取剂必须与原溶剂不互溶,乙醇与水互溶,C错误;步骤④的操作应该是蒸馏,D错误。
13.B 解析 向NaCl溶液中先后通入氨气、二氧化碳气体,得到的沉淀是NaHCO3,说明碳酸氢钠的溶解度小于氯化钠和Na2CO3,A错误;反应②中二氧化硫水溶液与单质溴反应生成硫酸和HBr,反应的离子方程式为Br2+SO2+2H2O===SO42-+2Br-+4H+,B正确;镁是活泼的金属,工业上通过电解熔融MgCl2制得金属镁,C错误;粗盐中含有的Mg2+、SO42-等杂质离子可转化为沉淀,依次加入BaCl2溶液、NaOH溶液、盐酸时,过量的BaCl2溶液无法除去,可依次加入BaCl2溶液、NaOH溶液、Na2CO3溶液,过滤后再加入盐酸,D错误。
14.B
15.B 解析 先将光卤石溶解于水,再加石灰乳沉淀Mg2+,Mg(OH)2的溶解度比Ca(OH)2更小,所以加入Ca(OH)2可以制得Mg(OH)2,洗涤后溶于适量的盐酸生成MgCl2,蒸发后冷却结晶得MgCl2·6H2O,为了防止加热MgCl2·6H2O的过程中发生副反应,故在HCl气氛中加热MgCl2·6H2O得到纯净的无水MgCl2,电解熔融MgCl2可制得金属镁。
16.答案 (1)烧杯 (2)NaCl、CaCl2(或NaOH等合理即可)
(3)蒸发浓缩、冷却结晶 (4)CaO+H2O===Ca(OH)2
17.答案 (1)CaCO3 (2)Mg(OH)2+2H+===Mg2++2H2O (3)② 漏斗 烧杯 (4)4.8 4.48
解析 (1)贝壳的主要成分是碳酸钙。(2)步骤④是Mg(OH)2与盐酸反应,化学方程式为Mg(OH)2+2HCl===MgCl2+2H2O,离子方程式为Mg(OH)2+2H+===Mg2++2H2O。(3)粗盐提纯过程中,过滤的目的是除去难溶性物质,选②;过滤需要用到的玻璃仪器有玻璃棒、漏斗、烧杯。(4)由MgCl2(熔融)Mg+Cl2↑可知,电解0.2 ml MgCl2生成0.2 ml金属Mg和0.2 ml氯气,金属Mg的质量为0.2 ml×24 g·ml-1=4.8 g,标准状况下氯气的体积为0.2 ml×22.4 L·ml-1=4.48 L。
18.答案 (1)BDE (2)过滤 蒸馏
(3)苯与水不互溶、不反应,且碘单质在苯中的溶解度远大于在水中的溶解度 D
苏教版 (2019)必修 第一册第三单元 海洋化学资源的综合应用第2课时课后练习题: 这是一份苏教版 (2019)必修 第一册第三单元 海洋化学资源的综合应用第2课时课后练习题,共8页。试卷主要包含了下列有关镁的说法正确的是,下列关于镁的叙述正确的是等内容,欢迎下载使用。
【同步讲义】高中化学(苏教版2019)必修第一册--3.3.2 从海水中提取镁 从海带中提取碘 讲义: 这是一份【同步讲义】高中化学(苏教版2019)必修第一册--3.3.2 从海水中提取镁 从海带中提取碘 讲义,文件包含同步讲义高中化学苏教版2019必修第一册--332从海水中提取镁从海带中提取碘讲义学生版docx、同步讲义高中化学苏教版2019必修第一册--332从海水中提取镁从海带中提取碘讲义教师版docx等2份试卷配套教学资源,其中试卷共25页, 欢迎下载使用。
高中化学苏教版 (2019)必修 第一册第三单元 海洋化学资源的综合应用第2课时习题: 这是一份高中化学苏教版 (2019)必修 第一册第三单元 海洋化学资源的综合应用第2课时习题,共5页。













