

甘肃省部分学校2023-2024学年高二上学期期末学业质量监测化学试题
展开
这是一份甘肃省部分学校2023-2024学年高二上学期期末学业质量监测化学试题,共13页。试卷主要包含了下列有关化学用语的表述错误的是,化学实验是学习化学的重要途径,对于反应,下列有关说法错误的是,已知等内容,欢迎下载使用。
本试卷满分100分 考试时间75分钟。
可能用到的相对原子质量:H—1 N—14 C—12 O—16 Na—23 Zn—65
考生注意:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号框涂黑。如需改动,用橡皮擦干净后,再选涂其它答案标号框。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
一、选择题(本大题包括14小题,每小题3分,共42分。每小题列出的四个备选项中只有一个是符合题目要求的,不选、多选、错选均不得分)
1.化学与生产、生活关系密切,下列有关说法错误的是( )
A.使用含氟牙膏可预防龋齿B.草木灰的溶液可洗涤油污
C.金属腐蚀中析氢腐蚀最普遍D.食醋可除去水垢中的碳酸钙
2.下列反应的焓变与下图所示的图象相符的是( )
A.碳与水蒸气的反应B.过氧化钠与水的反应
C.碳酸氢钠与盐酸的反应D.氢氧化钡晶体与氯化铵的反应
3.下列各组离子可大量共存的是( )
A.、、、B.、、、
C.、、、D.、、、
4.下列有关化学用语的表述错误的是( )
A.的水解:
B.电解精炼铜的阴极反应:更多优质资源可进入 C.S的原子结构示意图:
D.的电子式:
5.化学实验是学习化学的重要途径。下列所示装置或操作不能达到实验目的的是( )
6.对于反应,下列有关说法错误的是( )
A.该反应同时向生成HI和生成的方向进行
B.该反应的与HI不可能同时存在同一个反应体系中
C.该反应中生成HI的反应与生成的反应的条件相同
D.该反应中不可能全部转化为H1
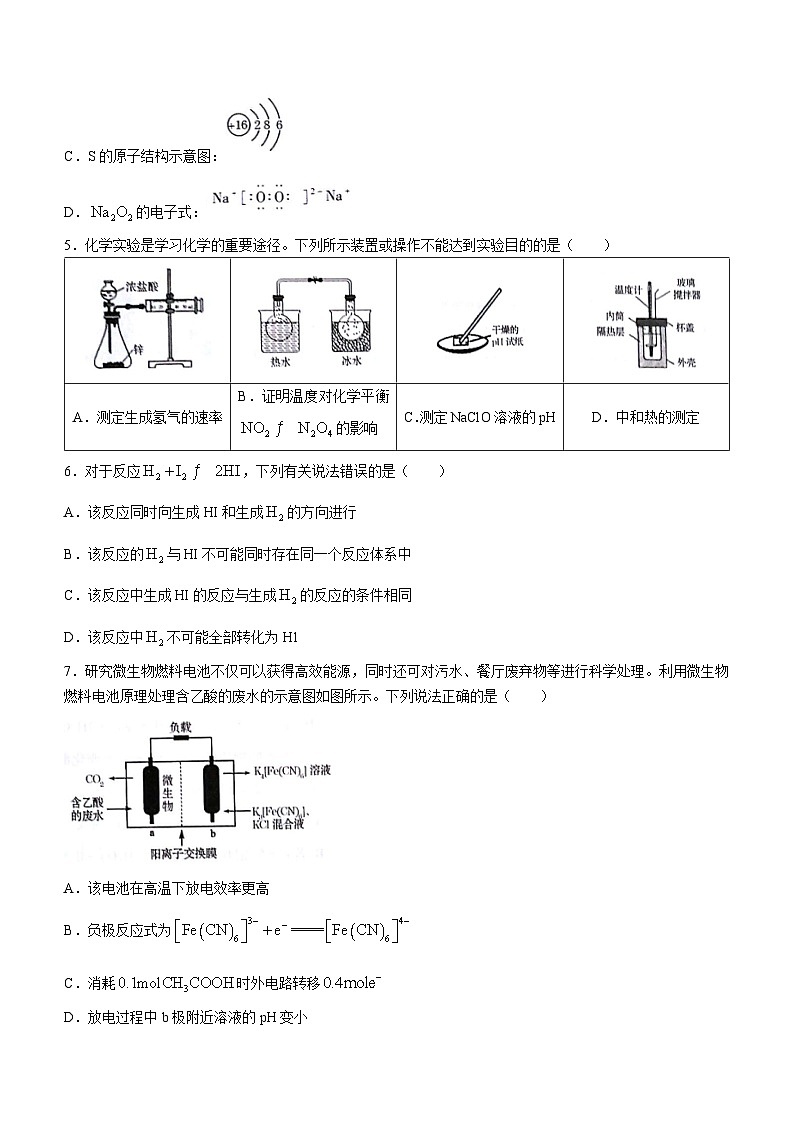
7.研究微生物燃料电池不仅可以获得高效能源,同时还可对污水、餐厅废弃物等进行科学处理。利用微生物燃料电池原理处理含乙酸的废水的示意图如图所示。下列说法正确的是( )
A.该电池在高温下放电效率更高
B.负极反应式为
C.消耗时外电路转移
D.放电过程中b极附近溶液的pH变小
8.反应 在密闭容器中进行,下列关于该反应的说法正确的是( )
A.升高温度能使平衡向逆反应方向移动
B.达到平衡状态时的浓度等于的浓度
C.增大压强,正反应速率增大,逆反应速率减小
D.使用催化剂,可增大反应物转化率
9.已知:①
②
③
下列说法正确的是( )
A.的燃烧热为
B.的总能量一定大于的总能量
C.一定温度下在恒容密闭容器中充入和足量充分反应后可放热92.4kJ
D.氨的催化氧化反应的热方程式为
10.科学家研制的无隔膜流动海水电解法制高纯度的装置如下图所示,其中高选择性催化剂PRT可抑制产生。下列说法错误的是( )
A.催化剂PRT选择性越高,的纯度越高
B.电解过程中海水的pH不断下降
C.理论上转移生成标准状况下22.4L的
D.阳极的电极反应式为
11.在2L的密闭容器中,发生如下反应: ,下列说法错误的是( )
A.该反应的
B.Y点的化学平衡常数小于Z点的化学平衡常数
C.图中X点v(正)”、“(2分) ③(2分)
(4)①的实验转化率未达到平衡转化率(2分)
②温度升高,反应Ⅰ逆向移动,反应Ⅲ正向移动,当温度高于260℃时,反应Ⅲ正向移动的程度大于反应Ⅰ逆向移动的程度(2分)
③在该条件下反应Ⅰ的速率大于反应Ⅲ,单位时间内生成甲醇的量比生成CO的量多(2分)
【解析】(1)由盖斯定律可得:反应①×2+反应②=目标方程式,则。
(2)由图示1可知,能垒:过渡态1>过渡态2,能垒越大反应速率越小,化学反应的决速步是由反应速率慢的一步所决定,则一定条件下,的反应速率由第1步决定的。
(3)①在前,相同温度下,甲醇的物质的量分数:催化剂甲>催化剂乙,则相同温度下,催化剂效果:催化剂甲>催化剂乙;
②反应为放热反应,升高温度平衡逆向移动;由2可知,即平衡常数。
③设甲醇的物质的量的变化量为aml,则由三段式
起(ml)1300
变(ml)
终(ml)
有:,
解得,则平衡后气体的总物质的量,反应前气体的总物质的量,由阿伏伽德罗定律的推论可知,
则;平衡时的分压为:,
(4)①由图可知,的实验转化率低于平衡转化率,所以实验中反应均未达到化学平衡状态。
②反应①为放热反应、反应③吸热反应,所以升高温度,反应①逆向移动,反应③正向移动,当温度高于260℃时,反应③正向移动的程度大于反应①逆向移动的程度。
③在该条件下反应①的速率大于反应③,单位时间内生成甲醇的量比生成CO的量多,温度相同时选择性的实验值略高于其平衡值。A.测定生成氢气的速率
B.证明温度对化学平衡的影响
C.测定NaClO溶液的pH
D.中和热的测定
实验装置
实验序号
烧杯中所加的试剂
电压表的读数
硫酸溶液
V/mL
V/mL
V/mL
1
30.0
/
10.0
2
30.0
1.0
9.0
3
30.0
2.0
8.0
4
30.0
1.0
实验装置
实验序号
实验操作
电压表的读数
5
/
6
向①__________(填“左”或“右”)侧烧杯中滴加硫酸溶液
7
向另一侧烧杯中滴加硫酸溶液
金属离子
开始沉淀时的pH
3.4
4.8
7.7
9.1
完全沉淀时()的pH
5.0
6.7
9.5
11.2
实验序号
1
2
3
4
消耗NaOH溶液的体积mL
15.95
15.00
15.05
14.95
醋酸的浓度()
0.0010
0.0100
0.0200
0.1000
0.2000
pH
3.88
3.38
3.23
2.88
2.73
相关试卷
这是一份2024届广东部分学校高三百日冲刺联合学业质量监测(一模)化学试题,共13页。
这是一份江西省部分学校2023-2024学年高二上学期期末教学质量检测化学试题(含答案),共11页。试卷主要包含了本试卷分选择题和非选择题两部分,本卷命题范围,可能用到的相对原子质量,下列现象与氢键无关的是,下列曲线表示第ⅦA族元素等内容,欢迎下载使用。
这是一份江西省抚州市2023-2024学年高二上学期1月学生学业质量监测(期末考试)化学试题(含答案),共10页。试卷主要包含了已知反应,下列说法正确的是,常温下,下列叙述正确的是,下列有关化学用语正确的是,2 NaOH溶液完全反应等内容,欢迎下载使用。









