
所属成套资源:2024郑州高三上学期第一次质量预测试题(一模)及答案(九科)
2024郑州高三上学期第一次质量预测试题(一模)化学含答案
展开
这是一份2024郑州高三上学期第一次质量预测试题(一模)化学含答案,共13页。试卷主要包含了下图为硝酸和甘油反应的断键机理等内容,欢迎下载使用。
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。考试时间 90 分钟,满分 100 分。考生应首先阅读答题卡上的文字信息,然后在答题卡上作答,在试题卷上作答无效。交卷时只交答题卡。
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Na—23 Si—28 S—32 As—75
第Ⅰ卷(选择题 共 45 分)
(本题包括15小题,每小题3分,每小题只有一个选项符合题意)
1.青海省的察尔汗盐湖是我国最大的盐湖,湖水中含有 555 亿吨氯化钠,还含有丰富的钾、镁、锂等元素,被称为“盐”的世界、富“钾”天下、“镁”不胜收、“锂”争上游。下列相关说法错误的是
A.湖水中所含金属元素均以化合态存在
B.从湖水中提取盐分时可利用其溶解度特点进行操作
C.从湖水中获取这几种金属元素的单质均可通过热还原法
D.不同区域的湖水色彩斑斓,可能与所含金属阳离子的种类、浓度有关
2.实验室常用 NH₄Cl和 Ca(OH)₂ 加热制备氨气,同时生成 CaCl₂。氨气和氯气反应可以生成漂白剂 NCl₃。下列对应化学用语错误的是
A. CaCl₂ 的电子式B. NH₃ 的球棍模型:
C.中子数为 8 的氮原子 D. NCl₃的电子式为:
3.下列表示客观事实的化学方程式或离子方程式正确的是
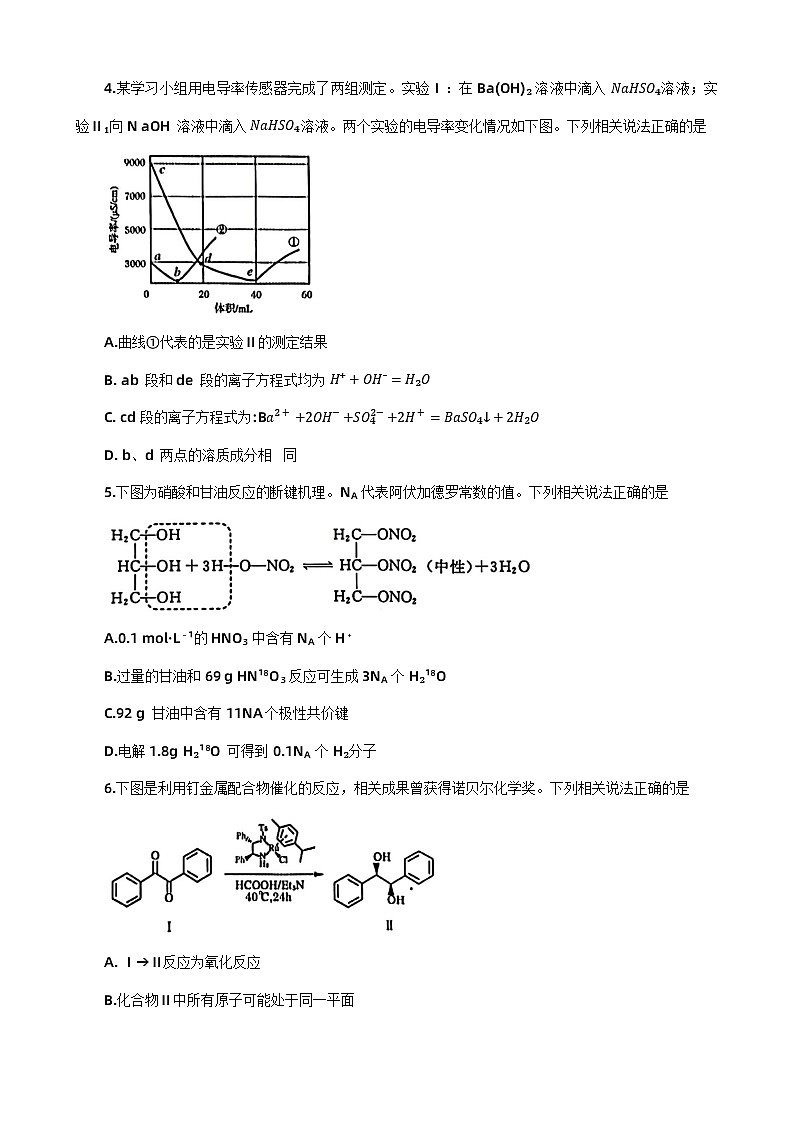
4.某学习小组用电导率传感器完成了两组测定。实验Ⅰ:在 Ba(OH)₂ 溶液中滴入 NaHSO₄溶液;实验Ⅱ₁向N aOH溶液中滴入 NaHSO₄溶液。两个实验的电导率变化情况如下图。下列相关说法正确的是
A.曲线①代表的是实验Ⅱ的测定结果
B. ab段和de段的离子方程式均为 H⁺+OH⁻=H₂O
C. cd 段的离子方程式为:Ba2++2OH−+SO42−+2H+=BaSO4↓+2H2O
D. b、d两点的溶质成分相 同
5.下图为硝酸和甘油反应的断键机理。NA 代表阿伏加德罗常数的值。下列相关说法正确的是
A.0.1 ml·L⁻¹的 HNO₃ 中含有 NA 个 H⁺
B.过量的甘油和69 g HN¹⁸O₃ 反应可生成3NA 个 H₂¹⁸O
C.92 g甘油中含有 11NA 个极性共价键
D.电解1.8g H₂¹⁸O可得到0.1NA个 H₂分子
6.下图是利用钉金属配合物催化的反应,相关成果曾获得诺贝尔化学奖。下列相关说法正确的是
A. Ⅰ→Ⅱ反应为氧化反应
B.化合物Ⅱ中所有原子可能处于同一平面
C.化合物Ⅱ的同分异构体中不可能含有萘环()结构
D.化合物Ⅰ可发生取代、加成、还原等反应类型
7.按下图进行实验,所对应的装置、药品或操作均正确的是
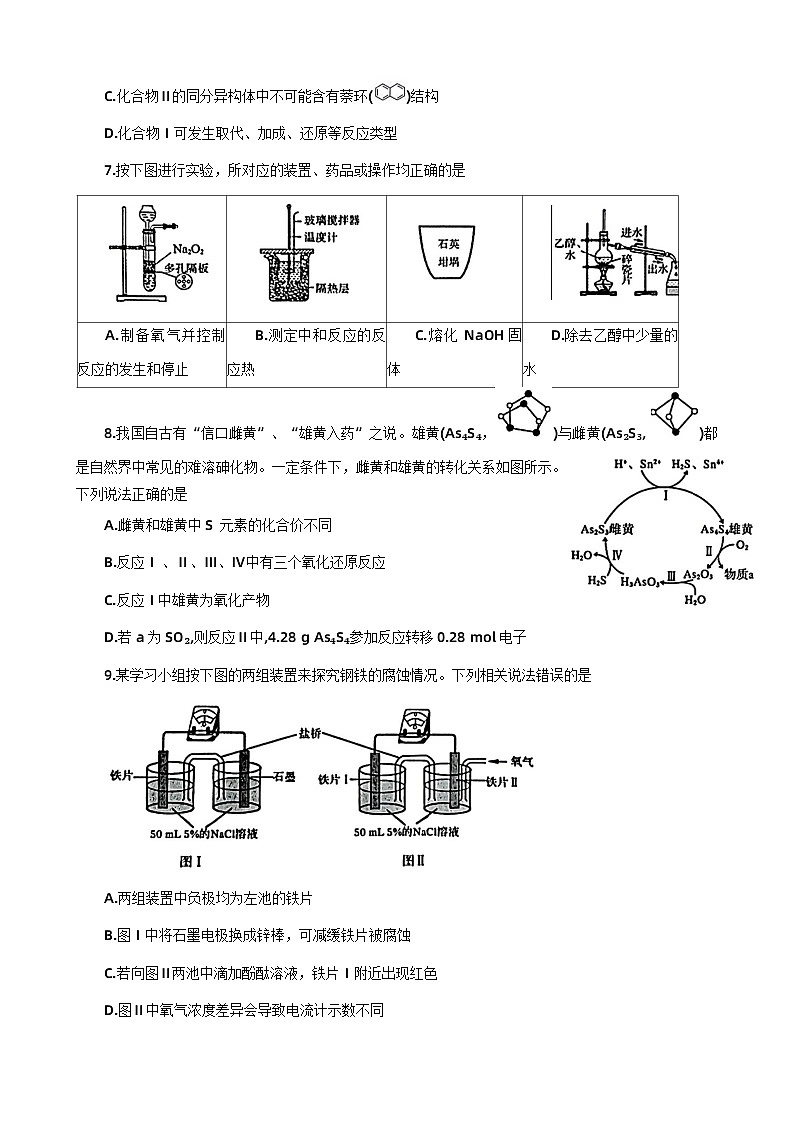
8.我国自古有“信口雌黄”、“雄黄入药”之说。雄黄(As₄S₄,)与雌黄(As₂S₃,)都是自然界中常见的难溶砷化物。一定条件下,雌黄和雄黄的转化关系如图所示。下列说法正确的是
A.雌黄和雄黄中S元素的化合价不同
B.反应Ⅰ 、Ⅱ、Ⅲ、Ⅳ中有三个氧化还原反应
C.反应Ⅰ中雄黄为氧化产物
D.若 a 为 SO₂,则反应Ⅱ中,4.28 g As₄S₄参加反应转移0.28 ml 电子
9.某学习小组按下图的两组装置来探究钢铁的腐蚀情况。下列相关说法错误的是
A.两组装置中负极均为左池的铁片
B.图Ⅰ中将石墨电极换成锌棒,可减缓铁片被腐蚀
C.若向图Ⅱ两池中滴加酚酞溶液,铁片Ⅰ附近出现红色
D.图Ⅱ中氧气浓度差异会导致电流计示数不同
10.化合物( YX₄₂MWZ₄₂⋅X₂Z是广泛用于印染工业的媒染剂。其中X、Y、Z、W 四种元素为原子序数依次增大的短周期元素,它们的原子序数之和为 32,Z、W两种元素最低负化合价相同。M 元素为人类使用最广泛的金属元素。下列相关说法正确的是
A.原子半径顺序:Z>Y>X
B.最高化合价:W>Y>X
C. Z元素的氢化物一定比 Y的稳定
D.向该化合物的水溶液中滴加酸性) KMnO₄,,振荡,溶液变无色
11.环氧乙烷(,简称 EO)是一种重要的工业原料和消毒剂。 由乙烯经电解制备 EO 的原理示意图如下。下列说法错误的是
A. X极电势高于 Y 极
B.阳极反应为 Cl⁻−2e⁻+OH⁻=HClO
C.溶液 a 为 KOH 和 KCl的混合溶液
D.制备总反应为CH₂=CH₂+H₂O→ +H₂
12.碳酸二苯酯可广泛使用于医药、农药、高分子材料等。由苯酚合成碳酸二苯酯的反应为:
2H₂O。相同时间内,产率随着温度升高或压强增大的变化如下图所示。已知常、压下苯酚和碳酸二苯酯的沸点分别为 182℃、306℃。下列相关说法错误的是
A.该反应正向为放热反应
B.使用催化剂可提高生产效率,但不能改变平衡转化率
C.加压有利于提高碳酸二苯酯的产率,但压强不宜无限增大
D.左图中 400 K后产率减小的原因一定是因为升温导致平衡向逆反应方向移动
13.莫尔法测定生理盐水浓度的过程如下:移取 10.00 mL 稀释后的生理盐水置于 250 mL 锥形瓶中,加入 3 滴 K₂CrO₄指示剂,用 0.1000ml⋅L⁻¹AgNO₃标准溶液滴定至终点。重复3次,消耗标准溶液的体积平均为 V mL,然后计算出NaCl的浓度。已知: KₛₚAgCl=1.77×10⁻¹⁰;KₛₚAg₂CrO₄=1.12×10⁻¹²; Ag₂CrO₄为砖红色沉淀。下列关于本实验的说法正确的是
A. 可用酸式滴定管装 AgNO₃ 标准溶液
B. 该稀释后的生理盐水浓度为 0.1Vml⋅L⁻¹
C. 实验中若用生理盐水润洗锥形瓶将导致测定结果偏低
D. 在相同浓度的 KCl和 K₂CrO₄混合溶液中滴入. AgNO₃溶液,先出现砖红色沉淀
14.已知草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水。草酸晶体 H₂C₂O₄⋅2H₂O无色,熔点为 101°C,易溶于水,受热脱水、升华, 170°C以上分解。某同学按照下图所示的实验装置,检验草酸晶体的分解产物。下列说法正确的是
A. a中加热草酸晶体的试管,试管口应朝下倾斜
B. 去掉 b装置,根据c中石灰水变浑浊即可以判断分解产物中含有( CO₂
C. d中 CuSO₄粉末变蓝,可以判断分解产物中有水产生
D. 将 CuSO₄粉末改为碱石灰,若e 中C uO变红色,f中变浑浊,则分解产物中有 CO
15.常温下,用浓度为 0.0200ml⋅L⁻¹的 NaOH 标准溶液滴定浓度均为 0.0200ml⋅L⁻¹的 HCl 和 CH₃COOH的混合溶液,滴定过程中溶液的p H随 ηη=V标准溶液V待测溶液的变化曲线如图所示。下列说法错误的是
A. b点: cNa⁺>cCH₃COO⁻>cCl⁻>cCH₃COOH
B. c点: Na⁺=2cCH₃COO⁻+cCH₃COOH
C. 水的电离程度:c>b>a
D. 常温下( CH₃COONa的水解平衡常数约为 10−9.24
第Ⅱ卷( 非选择题 共55 分)
16.(6分)以下是含硫物质的“价一类”二维图。回答以下问题:
(1)写出一个B转化为 D的化学方程式 。
(2)将 B 通入 BaNO₃₂溶液中,反应现象为 ;
(3)D的浓溶液可以使胆矾变白色,则 D表现的性质为 ;
(4)若 F 的化学式为 Na₂S₂O₃,向含有 Mn²⁺的废水中滴加 Na₂S₂O₈溶液会变紫红色,同时生成一种含硫价态相同的物质。该反应中氧化剂和还原剂的物质的量之比为 。
17.(7分)以下是合成水杨酸的路线图。
回答以下问题:
(1)③的反应类型为 。
(2)E中官能团的名称为 。
(3)写出反应①的化学方程式 。
(4)C的同分异构体中,属于芳香族化合物,且含有相同官能团的物质还有 种;其中含有4种等效氢原子物质的结构简式为 。
18.(10分)铜是人类广泛使用的金属之一。一种从废旧电路板中回收铜元素的工艺如下:
为了探究上述反应原理,分别取 50 mL 30%的 H₂O₂进行如下实验:
问题与讨论:
(1)实验Ⅰ中 Cu 与 H₂O₂ 发生微弱的反应,其化学方程式为 。
(2)实验Ⅱ相比实验Ⅰ的反应速率明显加快,其可能原因是 。
(3)经检测实验Ⅲ中蓝色溶液主要成分为( CuNH₃₄²⁺,则由铜生成该离子的离子方程式为 。
(4)已知 Cu²⁺+4NH₃⋅H₂O=CuNH₃₄²⁺+4H₂O的平衡常数 K= 4.7×10¹²,KₚCuOH₂=2.6×10−19
则反应Cu(OH)₂+4NH₃·H₂O ⇌[Cu(NH₃)₄]²⁺+4H₂O+2OH⁻的平衡常数的数值为 。
请分析实验Ⅳ中铜片表面无附着物的原因 。
19.(11分)实验室由正丁醛制备辛烯醛的反应为:
相关物质的性质和制备装置示意图如下。
实验步骤为:
Ⅰ.向 a瓶中加入6.3mL 2% NaOH 溶液,向 b中加入5.00 g正丁醛。
Ⅱ.通冷凝水,开启搅拌器,打开 b 的活塞,缓慢滴入正丁醛(30 min滴完后关闭活塞),反应瓶内温度保持在 78℃。持续反应1 h。
Ⅲ.拆除 b、c装置,转移 a 瓶中的反应液,分去碱液层。向有机层中加水,洗涤 2~3 次至水洗液呈中性。
Ⅳ.向有机层中加入无水硫酸钠,20 min后过滤;将滤液减压蒸馏、收集产品称量,得到 3.00 g辛烯醛。
回答下列问题:
(1)a装置的名称为 。
(2)步骤Ⅱ中采取的加热方式为 ,缓慢滴入正丁醛的目的是 。
(3)步骤Ⅲ中“分去碱液层”所需的玻璃仪器为 。检验水洗液呈中性的操作是 。
(4)步骤Ⅳ中,无水硫酸钠的作用是 。采用减压蒸馏的目的是
(5)本实验辛烯醛的产率为 %(保留小数点后一位)。
20.(10分)乙烯是一种重要化工原料。 乙炔加氢是一种制备乙烯的生产工艺。
I.乙炔热催化制乙烯
(1)已知: ①H2Og+COg⇌CO2g+H2g ∆ H=−41.5kJ⋅ml−1
②H2g+C2H2g⇌C2H4 (g) ∆H=−241.6kJ⋅ml−1
则反应(③ H2Og+COg+C2H2g⇌C2H4g+CO2g ∆H = kJ·ml-¹。
(2)在50℃、P kPa下,向恒压密闭容器中充入物质的量均为1m l的CO、H₂O、 C₂H₂气体,在催化剂作用下发生反应③和副反应 H₂Og+C₂H₂g= CH₃CHOg,,达到平衡时( C₂H₂的转化率为 60%,选择性: C2H4CH3CHO=41,则副反应的压力平衡常数 Kₚ=_____________________ kPa⁻¹。
Ⅱ.乙炔电催化制乙烯
该工艺乙炔的转化率超过99%,乙烯产物的选择性高达83%。其反应历程如下图所示。“ *”表示吸附。
(3)①该反应历程中有 个基元反应,反应速率最慢的基元反应方程式为 。
②下列说法中正确的是 。
A.1→2 中断裂O-H 键吸收能量小于生成 C-H 键释放的能量
B.3→4 中 H₂O的作用是与O∗生成 OH∗
C.4→6 中 CO的作用是与O∗生成CO₂∗ ⋅
21.(11分)锆是一种重要的战略金属,在国民经济中的地位举足轻重。中国科学院工程研究所研发了以锆英矿(主要成分为: ZrSiO₄,含少量 Al₂O₃,SiO₂杂质)制氧氯化锆的工艺如下:
注: Na₂ZrO₃、Na₂ZrSiO₅均不溶于水
(1)在 750°C下碱熔, ZrSiO₄全部转化为 Na₂ZrO₃,,该反应的化学方程式为 。
(2)“滤液1”中的溶质除含有 NaOH外,还含有 (化学式)。
(3)当碱熔的温度高于‘ 750°C时, Na₂ZrO₃中含有少量的 Na₂ZrSiO₅杂质,“转型”的主要目的是将Na₂ZrSiO₅转化 ZrOOH₂⋅SiO₂,则“滤液 2”中主要溶质为 。
(4)“酸分解”目的是将锆的化合物转化为 ZrOCl₂。,温度或盐酸浓度对“酸分解”的影响如下图所示:
从“酸分解”的效果考虑,宜采用的温度为 .°C,采用盐酸浓度为 ml·L⁻¹。
加入“絮凝剂”的目的是 。
(5)“操作 1”的主要步骤为 、 。
客观事实
化学用语
A
铁的金属活动性大于铜
2Fe³⁺+Cu=2Fe²⁺+Cu²⁺
B
铁和水蒸气能发生置换反应
2Fe+3H₂O高温Fe₂O₃+3H₂
C
配制 FeCl₃ 溶液时,将 FeCl₃ 固体加入浓盐酸中溶解后加水稀释
Fe³⁺+3H₂O⇌Fe(OH)₃+3H⁺
D
Fe³⁺的氧化性大于I₂
2Fe²⁺+I₂=2Fe³⁺+2I⁻
A.制备氧气并控制反应的发生和停止
B.测定中和反应的反应热
C.熔化 NaOH 固体
D.除去乙醇中少量的水
序号
操作
现象描述
I
加入一片光亮的铜片
无明显现象。10h后,取出铜片晾干,表面附着一层蓝色沉淀物
Ⅱ
加入一片光亮的铜片,并滴加少量稀硫酸
铜片表面产生少量的气泡,40 min后,溶液颜色为蓝色,取出铜片晾干,依然保持光亮
Ⅲ
加入一片光亮的铜片,并滴加少量氨水
立即产生大量气泡,气体可以使带火星的木条复燃。溶液颜色变为深蓝色。取出铜片晾干,表面附着一层蓝色沉淀物
Ⅳ
加入一片光亮的铜片,并滴加少量氨水,同时加入少量NH₄Cl固体
立即产生大量的气泡,溶液颜色变为深蓝色。取出铜片晾干,依然保持光亮
物质
性状
相对分子质量
沸点/℃
溶解性
正丁醛
无色液体,
密度 0.81g/cm³
72
75.0
微溶于水,
溶于有机溶剂
辛烯醛
无色液体,
密度 0.84g/cm³
126
177.0(略有分解)
不溶于水,
溶于有机溶剂
郑州市 2024年高中毕业年级第一次质量预测
化 学 参考答案
第Ⅰ卷 选择题 共45分
1. C 2. A 3. C 4. B 5. C 6. D 7. B 8. D 9. C 10. B 11. B 12. D 13. A 14. D 15. A第 Ⅱ卷( 共55分)
16.(6分)( 1SO₂+H₂O₂=H₂SO4(合理即可)(2分)
(2)有白色沉淀(1分)
(3) 吸水性 (1分) (4) 5: 2(2分)
17.(7分)(1) 氧化反应(1分) (2) 羟基 羧基(各1分)
18.(10分) 1Cu+H₂O₂=CuOH₂ (2分)
(2)酸性条件下,H₂O₂的氧化性增强,反应速率加快或酸性环境下无Cu(OH)₂生成,对后续反应无阻碍作用 (2分)
3Cu+H₂O₂+4NH₃⋅H₂O=CuNH₃₄²⁺+4H₂O+2OH (2分)
41.22×10⁻⁶ (2分) N H₄⁺结合O H⁻ 增大氨水浓度,使该平衡向右移动,促使Cu(OH)₂溶解 (2分)
19.(11分) (1)三颈烧瓶(三口烧瓶) (1分)
(2)水浴加热(1分) 减少正丁醛的挥发,提高产率(1分)
(3)分液漏斗、烧杯(2分)
取 pH试纸置于玻璃片上,用洁净干燥的玻璃棒蘸取最后一次水洗液滴在 pH 试纸上,变色后与标准比色卡对比,pH为7(2分)
(4)干燥剂(除去有机层中的水分) (1分) 防止温度过高,辛烯醛分解(或氧化) (1分)
(5)68.6 (2分)
20.(10分) (1) -283.1 (2分) 21.8P (2分)(3) ①4 (2分) CO∗+4OH∗+O∗=CO2∗+4OH∗CO∗+O∗=CO2∗(2分) ②BC (2分)
21.(11分) ( 1ZrSiO₄+6NaOH=Na₂ZrO₃+Na₄SiO₄+3H₂O
或 ZrSiO₄+4NaOH=Na₂ZrO₃+Na₂SiO₃+2H₂O (2分)
2NaAlOH₄、Na₄SiO₄(或 Na₂SiO₃) (2分)
(3) NaCl (2分)
(4)100 (1分) 6 (1分) 防止生成硅酸胶体, 利于生成硅酸沉淀(1分)
相关试卷
这是一份郑州市2024年高中毕业年级第一次质量预测(高三一模)化学参考答案,共2页。
这是一份河南省郑州市2023-2024学年高三上学期高中毕业年级第一次质量预测化学试题卷,共13页。
这是一份河南省郑州市2022届高三上学期第一次质量预测(一模)(1月)化学PDF版含答案,共9页。









