

专题七 选择题专攻 2.物质的分离、提纯及规范描述 课件-2024年高考化学二轮复习
展开
这是一份专题七 选择题专攻 2.物质的分离、提纯及规范描述 课件-2024年高考化学二轮复习,共42页。PPT课件主要包含了核心精讲,酸性KMnO4,灼热的铜网,NaOH,蒸发→结晶→过滤,沉淀剂,过滤器,自然流下,CO2,冷却结晶等内容,欢迎下载使用。
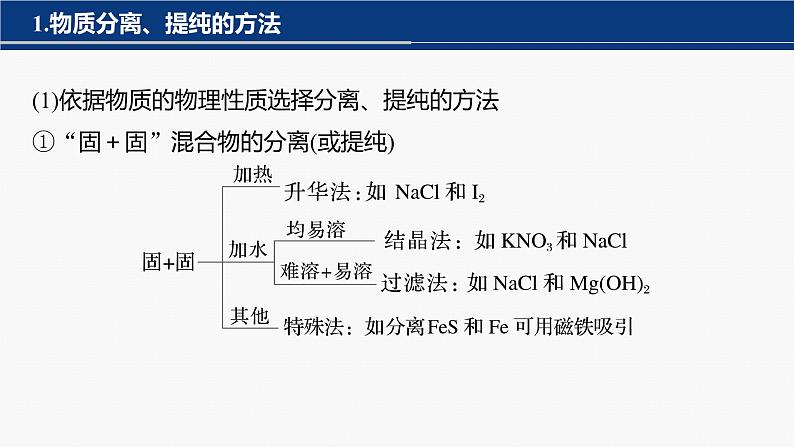
1.物质分离、提纯的方法
(1)依据物质的物理性质选择分离、提纯的方法①“固+固”混合物的分离(或提纯)
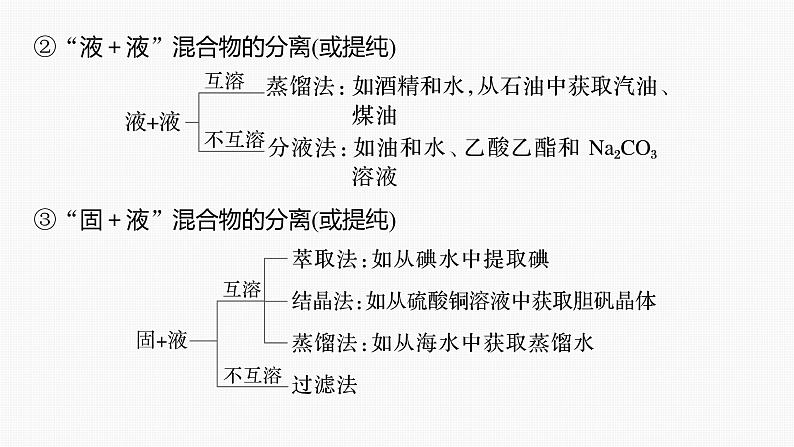
②“液+液”混合物的分离(或提纯)
③“固+液”混合物的分离(或提纯)
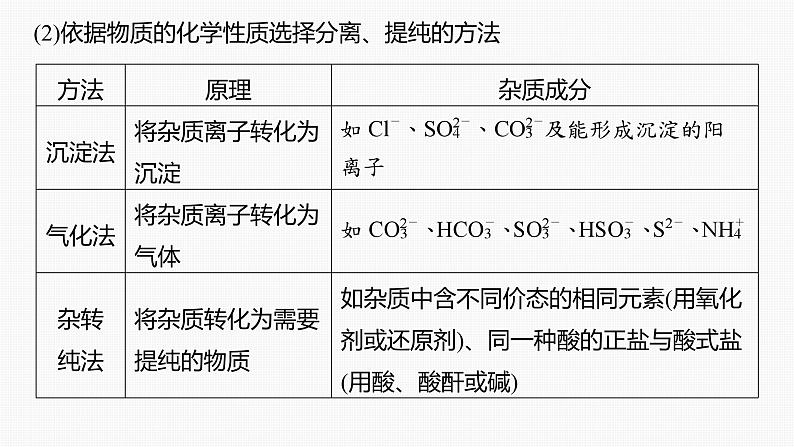
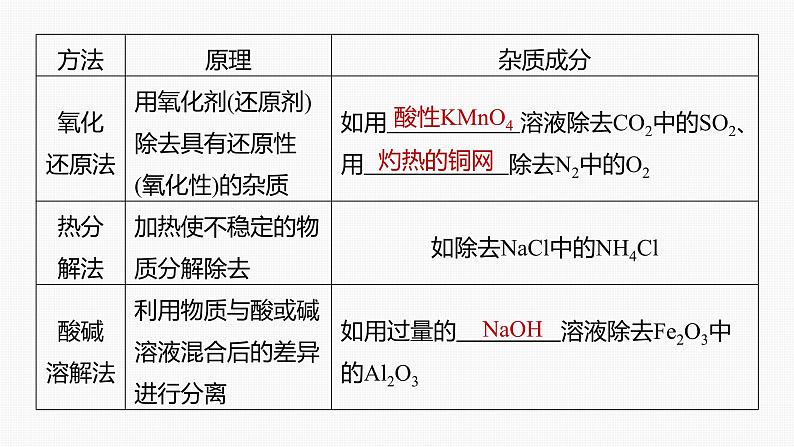
(2)依据物质的化学性质选择分离、提纯的方法
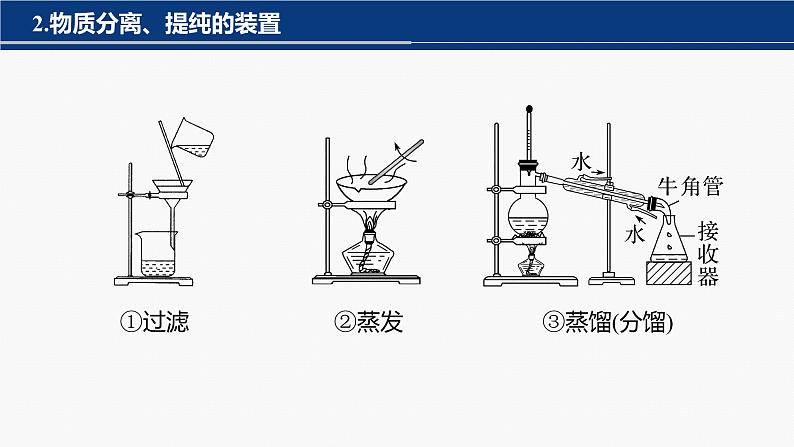
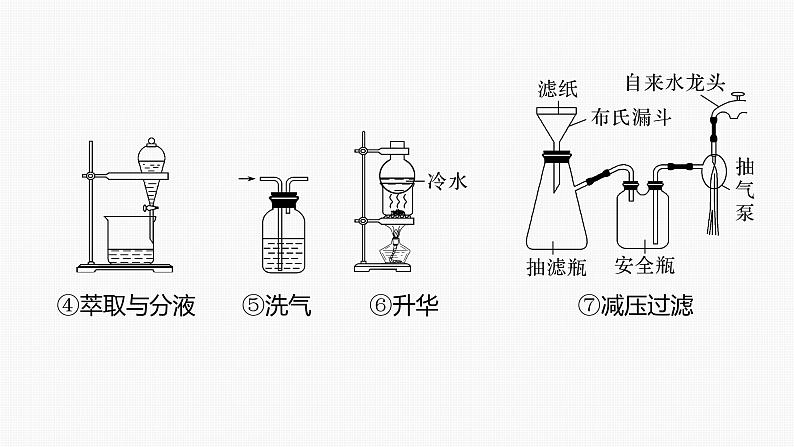
2.物质分离、提纯的装置
①过滤 ②蒸发 ③蒸馏(分馏)
④萃取与分液 ⑤洗气 ⑥升华 ⑦减压过滤
3.物质分离、提纯的精准描述
(1)粗盐的提纯①实验室提纯粗盐的实验操作依次为取样、 、 、 、 、_____。②若过滤时发现滤液中有少量浑浊,从实验操作的角度分析,可能的原因是过滤时漏斗中液面高出滤纸边缘、玻璃棒靠在单层滤纸一边弄破了滤纸。
(2)从某物质稀溶液中结晶的实验操作①物质溶解度受温度影响较小: 。②物质溶解度受温度影响较大或带结晶水:___________________________。(3)沉淀剂是否过量的判断方法①静置,取上层清液于一洁净的试管中,继续滴加少量 ,若无沉淀产生,则证明沉淀剂已过量,否则沉淀剂不过量。②静置,取适量上层清液于一洁净试管中,向其中加入少量与沉淀剂作用产生沉淀的试剂,若产生沉淀,则证明沉淀剂已过量,否则沉淀剂不过量。
蒸发浓缩→冷却结晶→过滤
(4)洗涤沉淀的操作将蒸馏水沿着玻璃棒注入 中至浸没沉淀,静置,待水 ,重复操作2~3次即可。(5)判断沉淀是否洗净的操作取最后一次洗涤液,滴加……(试剂),若没有……现象,证明沉淀已经洗净。
应用示例1.常见物质的除杂
2.常见混合气体的除杂
酸性高锰酸钾溶液和石灰乳
图Ⅳ为冷凝除杂,如除去SO2中的SO3气体,CO2中的H2C2O4气体等。
1.(2023·全国甲卷,9)实验室将粗盐提纯并配制0.100 0 ml·L-1的NaCl溶液。下列仪器中,本实验必须用到的有①天平 ②温度计 ③坩埚 ④分液漏斗 ⑤容量瓶 ⑥烧杯 ⑦滴定管 ⑧酒精灯A.①②④⑥ B.①④⑤⑥C.②③⑦⑧ D.①⑤⑥⑧
粗盐提纯涉及的操作及使用的仪器有溶解(⑥烧杯和玻璃棒)、除杂、过滤(漏斗、玻璃棒、⑥烧杯)、蒸发结晶(蒸发皿、⑧酒精灯、玻璃棒)。配制0.100 0 ml·L-1的NaCl溶液的操作步骤及使用的仪器是称量(①天平)→溶解(⑥烧杯和玻璃棒)→移液(⑥烧杯、玻璃棒、⑤容量瓶)→定容(胶头滴管),故本题选D。
2.(2022·广东,4)实验室进行粗盐提纯时,需除去Ca2+、Mg2+和 所用试剂包括BaCl2以及A.Na2CO3、NaOH、HClB.Na2CO3、HCl、KOHC.K2CO3、HNO3、NaOHD.Na2CO3、NaOH、HNO3
3.(2021·湖北,7)某兴趣小组为制备1-氯-2-甲基丙烷(沸点69 ℃),将2-甲基-1-丙醇和POCl3溶于CH2Cl2中,加热回流(伴有HCl气体产生)。反应完全后倒入冰水中分解残余的POCl3,分液收集CH2Cl2层,无水MgSO4干燥、过滤、蒸馏后得到目标产物。上述过程中涉及的装置或操作错误的是(夹持及加热装置略)
依题意,制备产品需要“搅拌、加热回流”,A项正确;副产物氯化氢极易溶于氢氧化钠溶液,不能直接将尾气通入氢氧化钠溶液中,这样易发生倒吸现象,B项错误;分液收集二氯甲烷层需用到分液漏斗,振荡时需将分液漏斗倒转过来放气,避免分液漏斗内气压过大,发生危险,C项正确;蒸馏时需要用温度计指示温度,冷凝水从下口进、上口出,提高冷凝效率,D项正确。
4.(2022·海南,3)下列实验操作规范的是
过滤时,漏斗下端应紧靠烧杯内壁,A操作不规范;CO2的密度大于空气且不与空气中的成分反应,可用向上排空气法收集,B操作规范;混合浓硫酸和乙醇时,应将浓硫酸缓慢倒入乙醇中,并用玻璃棒不断搅拌,C操作不规范;转移溶液时,应使用玻璃棒引流,D操作不规范。
酸性高锰酸钾溶液不仅能与H2S反应,而且也能与SO2反应,A项不能实现目的。
5.(2020·全国卷Ⅰ,9)下列气体去除杂质的方法中,不能实现目的的是
根据文中描述,将海水倒在锅中加热煮沸,看见白色的固体出现,就得到盐,操作方法为浓缩结晶,故D正确。
6.(2020·海南,2)古籍《天工开物》收录了井盐的生产过程。其中“汲水而上,入于釜中煎炼,顷刻结盐,色成至白”的描述,涉及的物质分离操作为A.趁热过滤 B.萃取分液C.常压蒸馏 D.浓缩结晶
已知Fe3+在浓盐酸中生成黄色配离子[FeCl4]-,该配离子在乙醚(Et2O,沸点34.6 ℃)中生成缔合物Et2O·H+·[FeCl4]-。下列说法错误的是A.萃取振荡时,分液漏斗下口应倾斜向下B.分液时,应先将下层液体由分液漏斗下口放出C.分液后水相为无色,说明已达到分离目的D.蒸馏时选用直形冷凝管
7.(2020·山东,8)实验室分离Fe3+和Al3+的流程如下:
萃取振荡时,分液漏斗下口应倾斜向上,A项错误;分液时先将下层液体从下口放出,B项正确;水相为无色说明黄色配离子基本被萃取出来,C项正确;直形冷凝管有利于液体流出,故蒸馏时选用直形冷凝管,D项正确。
物质分离与提纯的思维模型
1.下列除杂试剂和分离方法都正确的是
加热条件下镁和N2、O2均能反应,A错误;二氧化碳也可以和饱和碳酸钠溶液反应,应用饱和碳酸氢钠溶液洗气,B错误;氧化铁也可以和盐酸反应,应用NaOH溶液除杂,C错误;氯气难溶于饱和食盐水,HCl极易溶于水,可以用饱和食盐水除去氯气中的HCl气体,D正确。
2.下列气体去除杂质的方法中,能实现目的的是
SO2和HCl都可以和饱和亚硫酸钠溶液反应,故A不能实现目的;氨气为碱性气体,能被浓硫酸吸收,氧气不能被浓硫酸吸收,故B能实现目的;二氧化碳不能和氯化钡溶液反应,故C不能实现目的;水能和过氧化钠固体反应生成氧气,引入新杂质,故D不能实现目的。
3.下列实验能达到目的的是A.除去Na2CO3溶液中混有的NaHCO3,可用加热法B.除去乙烷中混有的乙烯,可将混合气体依次通入酸性KMnO4溶液、浓 硫酸C.除去CO2中混有的SO2,可通过饱和NaHCO3溶液D.除去乙醇中混有的乙酸,可用蒸馏法
除去Na2CO3固体中的NaHCO3可用加热法,溶液不能用加热法,A项错误;乙烯会被酸性高锰酸钾溶液氧化为二氧化碳,引入新的杂质,B项错误;乙醇和乙酸会形成共沸物,不能直接蒸馏分离,可以先加入氧化钙与乙酸反应,再进行蒸馏分离,D项错误。
4.工业电解精炼铜的溶液中含有Zn2+、Cu2+等离子,实验室设计分离出Zn2+并制取胆矾的流程如下: 已知:Zn2+与NaOH的反应与Al3+类似。下列说法错误的是A.滤液1与过量硫酸反应的离子方程式为B.操作①和②中用到的玻璃仪器完全相同C.系列操作②包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥D.可用无水乙醇洗涤胆矾晶体,除去表面的杂质
操作①是过滤,需要的玻璃仪器是漏斗、烧杯、玻璃棒;系列操作②包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥,需要的玻璃仪器是漏斗、烧杯、玻璃棒、酒精灯,故B错误、C正确;用无水乙醇洗涤晶体最主要的原因是除去晶体表面的水及杂质,而且不溶解晶体,同时易挥发,故D正确。
5.某同学采用工业大理石(含有少量SiO2、Al2O3、Fe2O3等杂质)制取CaCl2·6H2O,设计了如下流程:下列说法不正确的是A.固体Ⅰ中含有SiO2,固体 Ⅱ中含有Fe(OH)3、Al(OH)3B.加入石灰水时,要控制pH,防止固体Ⅱ中Al(OH)3转化为C.试剂a选用盐酸,从溶液Ⅲ得到CaCl2·6H2O产品的过程中,应控制条件防止 其分解D.若改变实验方案,在溶液Ⅰ中直接加氨水至沉淀完全,滤去沉淀,其溶液经 蒸发浓缩、冷却结晶也可得到纯净的CaCl2·6H2O
向工业大理石(含有少量SiO2、Al2O3、Fe2O3等杂质)中加足量酸,得到二氧化硅沉淀,所以固体Ⅰ中含有SiO2,溶液Ⅰ中加石灰水,控制pH,可以得到Al(OH)3、Fe(OH)3沉淀,即为固体Ⅱ,A项正确;
试剂a为盐酸,CaCl2·6H2O易分解,所以从溶液中获得氯化钙晶体时,要控制条件防止其分解,C项正确;若改变实验方案,在溶液Ⅰ中直接加氨水至沉淀完全,滤去沉淀,其溶液中含有氯化铵杂质,D项错误。
相关课件
这是一份专题七 选择题专攻 2.物质的分离、提纯及规范描述 2024年高考化学二轮复习课件+讲义,文件包含专题七选择题专攻2物质的分离提纯及规范描述pptx、专题七选择题专攻2物质的分离提纯及规范描述教师版docx、专题七选择题专攻2物质的分离提纯及规范描述docx等3份课件配套教学资源,其中PPT共42页, 欢迎下载使用。
这是一份专题三 选择题专攻 2.物质结构与性质 2024年高考化学二轮复习课件+讲义,文件包含专题三选择题专攻2物质结构与性质pptx、专题三选择题专攻2物质结构与性质教师版docx、专题三选择题专攻2物质结构与性质docx等3份课件配套教学资源,其中PPT共52页, 欢迎下载使用。
这是一份专题二 选择题专攻 2.化学与传统文化 2024年高考化学二轮复习课件+讲义,文件包含专题二选择题专攻2化学与传统文化pptx、专题二选择题专攻2化学与传统文化教师版docx、专题二选择题专攻2化学与传统文化docx等3份课件配套教学资源,其中PPT共39页, 欢迎下载使用。








