

所属成套资源:全套2023-2024学年高一上学期期中考试化学试卷含答案
河北省石家庄市正定一中、栾城中学、鹿泉区一中等校2023-2024学年高一上学期期中考试化学试题含答案
展开
这是一份河北省石家庄市正定一中、栾城中学、鹿泉区一中等校2023-2024学年高一上学期期中考试化学试题含答案,共17页。试卷主要包含了下列说法正确的是,下列离子反应方程式表达正确的是,下列实验现象和结论相符的是,下列实验中,能实现实验目的的是等内容,欢迎下载使用。
化学
本试卷共8页,满分100分,考试用时75分钟.
注意事项:
1.答卷前,考生务必将自己的姓名、班级、准考证号等填写在答题卡上.
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑.
如需改动,用橡皮擦干净后,再选涂其它答案标号.回答非选择题时,将答案写在答题卡上.写在本试卷上无效.
3.考试结束后,将本试卷和答题卡一并交回.
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Cu 64
一、选择题:本题共14小题,每小题3分,共42分.在每小题给出的四个选项中,只有一项是符合题目要求的.
1.化学与生活生产科技环境等关系密切.下列说法错误的是( )
A.蔗糖(纯净物)在水溶液和熔融状态下均不能导电,所以蔗糖属于非电解质
B.我国成功研制出纳米片,该化合物属于碱
C.钠着火可用干燥的沙土或石棉布盖灭
D.碳酸氢钠受热易分解,可用作焙制糕点的膨松剂
2.中国传统文化对人类文明贡献巨大.下列关于古代文献的表述不合理的是( )
A.《准南万毕术》中记载:“曾青得铁则化为铜”,铁为还原剂.
B.《天工开物》中记载:“凡铁分生熟,出炉未炒则生,既炒则熟”中,“炒”为氧化除碳过程.
C.《本草经集注》中记载:“强烧之,紫青烟起,云是硝石也”,利用的是焰色试验区分硝石()和朴硝().
D.《天工开物》中记载:“凡火药,硫为纯阳,硝为纯阴”,不涉及氧化还原反应.
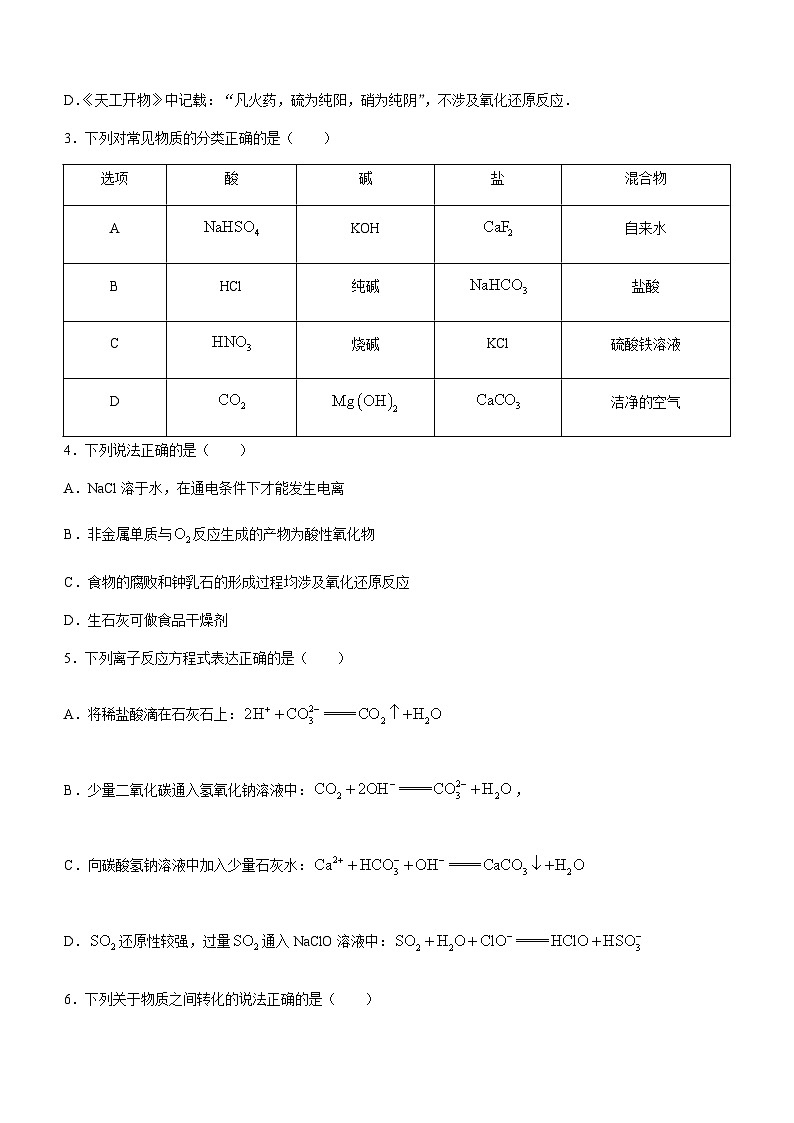
3.下列对常见物质的分类正确的是( )
4.下列说法正确的是( )
A.NaCl溶于水,在通电条件下才能发生电离
B.非金属单质与反应生成的产物为酸性氧化物
C.食物的腐败和钟乳石的形成过程均涉及氧化还原反应
D.生石灰可做食品干燥剂
5.下列离子反应方程式表达正确的是( )
A.将稀盐酸滴在石灰石上:
B.少量二氧化碳通入氢氧化钠溶液中:,
C.向碳酸氢钠溶液中加入少量石灰水:
D.还原性较强,过量通入NaClO溶液中:
6.下列关于物质之间转化的说法正确的是( )
A.转化为,需要加入氧化剂才能实现B.向NaClO溶液中加入还原剂可将其转化为NaCl
C.溶液中通入可将其转化为D.加入还原剂可实现的转化
7.下列实验现象和结论相符的是( )
8.设阿伏加德罗常数的值为,则下列说法正确的是( )
A.常温常压下,32g和的混合物中含有原子数为
B.常温下,7.8g固体中含有阴阳离子总数为
C.的溶液中所含阴离子数目为
D.标准状况下,11.2L中含有氢原子数为
9.将一定浓度的稀溶液分为两等份放入烧杯中,分别向其中滴入等浓度的稀和稀溶液,两份溶液导电能力随滴入溶液的体积变化曲线如图.下列分析正确的是( )
A.a→b发生的反应离子方程式为:
B.曲线②代表滴加溶液的变化曲线
C.a→c发生反应的离子方程式为:
D.a、c两点对应的溶液均为中性
10.下列实验中,能实现实验目的的是( )
11.对固体充分加热,产生的气体先通过足量浓硫酸,再通过足量,增重0.28g,则固体的质量为( )
A.0.42gB.1.68gC.0.84gD.3.36g
12.氯元素可形成多种物质,为了研究方便,绘制氯及其化合物的价类二维图如图所示,下列说法不正确的是( )
A.a溶液与e溶液混合一定条件下可发生氧化还原反应
B.可用pH试纸测定b的水溶液的pH值
C.c溶液中通入二氧化碳可增强其漂白、杀菌消毒的能力
D.d可用于自来水的杀菌消毒
13.某兴趣小组设计了如图所示实验装置,验证Na与能否发生反应.已知能被CO还原得到黑色的金属Pd.加热D装置中硬质玻璃管一段时间,观察到以下现象:
①钠块表面变黑,熔融成小球;
②继续加热,钠燃烧产生黄色火焰,硬质玻璃管中有大量黑色和白色固体产生;
③F中试管内壁有黑色沉淀产生.
下列说法不正确的是( )
A.B中盛放饱和NaCl溶液,C中盛放浓硫酸
B.连接装置,打开和,通入待E中出现白色沉淀后,再点燃酒精灯
C.D中产生的黑色固体为碳单质
D.F装置和气球的作用为检验并收集CO,防止CO污染空气
14.向浓度相等、体积均为50mL的A、B两份NaOH溶液中,分别通入一定量的后,再稀释到100mL.在稀释后的溶液中逐滴加入的盐酸,产生的体积(标准状况)与所加盐酸的体积关系如图所示.下列说法不正确的是( )
A.A曲线说明,A原溶液通的体积为0.112L(标准状况)
B.B曲线说明,B原溶液通入后,所得溶质成分为NaOH、
C.当所加盐酸体积为75mL时,A、B两溶液所含溶质相同,浓度不同
D.原NaOH溶液的物质的量浓度为
二、非选择题:本题共4个大题,共58分.
15.(14分)“分类”的思想在化学学习及化学学科发展中起着重要作用.现有下列物质:
①固体 ②熔融 ③淀粉溶液 ④液态氯化氢 ⑤NaCl溶液 ⑥ ⑦金属铜 ⑧ ⑨酒精 ⑩
回答下列问题:
(1)以上物质中属于电解质的是______(填序号,下同),属于非电解质的是______.
(2)②熔融能导电,其电离方程式为______.
(3)③淀粉溶液所属分散系为______,⑤NaCl溶液所属分散系为______,二者如果混合,可采用______方法分离.
(4)⑧与水的反应属于氧化还原反应,化学方程式为______,该反应中是______(“氧化剂”“还原剂”或“既是氧化剂又是还原剂”),每当有1ml参与反应,转移电子数为______(设为阿伏伽德罗常数的值).
(5)已知⑨(次磷酸)与足量KOH溶液反应的化学方程式为,属于______(填“正盐”或“酸式盐”).
16.(14分)纯碱在日常生活和工业生产中有着广泛的应用.化工专家侯德榜发明的“侯氏制碱法”为我国纯碱工业和国民经济发展做出了重要贡献.“侯氏制碱法”的反应原理是:,实验室先用下图装置模拟“侯氏制碱法”制备纯碱,然后再对纯碱样品进行含量测定和分离提纯.
请回答下列问题:
(1)在饱和食盐水中应该由先由______管通______、再由______管通______.
(2)将反应后溶液进行______,得到纯碱样品.
(3)经过分析,纯碱样品中可能含有的杂质为NaCl,如何证明含有NaCl,请写出检验方法______.
(4)为了测定纯碱样品中的质量分数,设计如下实验方案:称取6.0g纯碱样品,加入足量稀盐酸,将产生的气体通入碱石灰中进行吸收,测得碱石灰的质量增加2.4g,进而计算碳酸钠的质量分数.请问该实验方案是否可行______(“可行”或“不可行”),若可行,请计算出碳酸钠的质量分数______(保留小数点后一位).如果不可行,请写出改进方案:______.
(5)如图为NaCl、在水中的溶解度曲线.请结合溶解度曲线,分析除去纯碱样品中的氯化钠杂质的具体操作为______.
17.(15分)很多化学反应条件不同,产物不同,如与KOH反应,常温下生成KClO,加热生成.实验室利用下图装置制备,然后进一步探究其性质.
回答下列问题:
(1)装置a可用于实验室制,反应的化学方程式是______.
(2)装置b的作用是______,可选用______溶液.
(3)c中采用的加热方式是______,反应的离子方程式为______,该反应中氧化剂和还原剂的物质的量之比为______.
(4)若d装置中溶液是NaOH溶液,其作用是______.
(5)取c中溶液,滴加浓盐酸并加热,可产生黄绿色气体,结合上述的制备实验,可说明在碱性条件下氧化性:______(填“>”“<”或“=”,下同),酸性条件下氧化性:______.
18.(15分)实验室中配制一定物质的量浓度的溶液一般分为两种情况,用固体配制溶液或者用浓溶液配制稀溶液.请依据以下情况回答问题:
Ⅰ.实验室需要溶液480mL,即用胆矾()配制该溶液.
(1)配制溶液时需要的玻璃仪器有______.
(2)实验前需要对配制溶液所用容量瓶进行______.
(3)配制溶液的第一步是计算,若该实验用托盘天平称量,需要称取______g胆矾晶体.
(4)下列操作导致配制的溶液浓度偏大的是______.
A.称量时砝码和胆矾位置放反B.未洗涤烧杯和玻璃棒
C.定容时俯视容量瓶刻度线D.摇匀后发现液面低于刻度线
Ⅱ.“84消毒液”具有杀菌消毒、漂白的作用.已知某市售“84消毒液”瓶体部分标签如图所示.
(5)使用该“84消毒液”,需要事先进行稀释,现在实验室利用该“84消毒液”稀释配制成250mLNaClO溶液,需要用______mL该溶液,在量取时宜选用量筒的规格为______.
A.5mLB.10mLC.25mLD.50mL
(6)“84消毒液”与稀盐酸混合使用可增强其漂白效果,原因是______(用离子方程式表示,下同),但“84消毒液”却不能与“洁厕灵”(浓盐酸)混合使用,原因是______,对比以上情况可知,加入的酸的______不同,发生的反应不同.
石家庄市多校2023-2024学年高一上学期期中考试
化学答案与解析
1.【答案】B
【解析】在水溶液和熔融状态下均不能导电的化合物是非电解质,A正确;由、、构成,属于碱式盐,B错误;钠着火可用干燥的沙土或石棉布盖灭,C正确;碳酸氢钠受热分解产生,可用作焙制糕点的膨松剂,D正确;故选B.
2.【答案】D
【解析】“曾青得铁则化为铜”,发生反应,Fe元素的化合价升高,为氧化剂,A错误;生铁中含碳量较高,“炒”的过程使碳与氧气发生反应,是氧化除碳的过程,B错误;硝石和朴硝在灼烧时火焰颜色不同,硝石为紫色,朴硝为黄色,利用的就是焰色试验进行区分,C错误;火药爆炸发生反应,存在元素的化合价变化,属于氧化还原反应,D正确;故选D.
3.【答案】C
【解析】属于酸式盐,A错误;纯碱是,属于盐不是碱,B错误;属于酸性氧化物,D错误;故选C.
4.【答案】D
【解析】NaCl溶于水即可发生电离,无需通电,A错误;非金属单质与反应生成的产物不一定为酸性氧化物,B错误;钟乳石的形成过程不涉及氧化还原反应,C错误;生石灰可做食品干燥剂,D正确;故选D.
5.【答案】B
【解析】石灰石主要成分为,是难溶物,不能拆,方程式为,A错误;氢氧化钠溶液中通入少量的二氧化碳,离子方程式为,B正确;向碳酸氢钠溶液中加入少量石灰水反应的离子方程式为,C错误;过量通入NaClO溶液中,NaClO具有强氧化性,将+4价硫氧化为+6价:,D错误;故选B.
6.【答案】B
【解析】转化为,加入水或者即可实现,既是氧化剂又是还原剂,无需外加氧化剂,A错误;向NaClO溶液中加入还原剂可将其转化为,B正确;溶液与不反应,C错误;加入氧化剂可实现的转化,D错误;故选B.
7.【答案】D
【解析】碳酸氢根离子、碳酸根离子均与盐酸反应生成二氧化碳,则溶液中不一定含有,A错误;向某溶液中滴加氢氧化钠溶液,微热,应用湿润的红色石蕊试纸放在试管口检验,若试纸变蓝,则溶液中一定含有,B错误;焰色反应时火焰为黄色,说明有溶液中有,但不一定是钠盐溶液,可能是NaOH溶液,C错误;先加足量稀盐酸,排除碳酸根、银离子干扰,再加入氯化钡溶液检验硫酸根离子,D正确;故选D.
8.【答案】A
【解析】32g的氧气中含有的氧原子数,32g的臭氧中含有的氧原子数,所以32g与的混合物中含有个氧原子,A正确;固体中含有和,7.8g固体物质的量为0.1ml,含有阴阳离子总数为,B错误;C选项无体积,无法计算;D选项标准状况下,为液态;故选A.
9.【答案】B
【解析】向溶液中滴入硫酸溶液发生反应的化学方程式为,向溶液中滴入溶液,随着溶液的滴入依次发生反应a→c:、c→d:,溶液导电能力随离子浓度增大而增强,根据图示可知,曲线①在b点溶液导电能力接近0,说明该点溶液离子浓度最小,应该为溶液和的反应,则曲线②为溶液和溶液的反应,据此分析作答.a→b发生的反应离子方程式为,A错误;由以上分析可知曲线②代表滴加溶液的变化曲线,B正确;a→c发生的反应离子方程式为,C错误;b点时稀硫酸和稀氢氧化钡溶液恰好完全反应,溶液呈中性,d点时溶液中氢氧根离子恰好被中和,溶液为硫酸钠溶液,呈中性,D错误;故选B.
10.【答案】A
【解析】在坩埚中进行钠的燃烧反应,能实现实验目的,A正确;浓硫酸不能直接倒入容量瓶,应该稀释冷却后再转移入容量瓶,B错误;制备氢氧化铁胶体应将饱和溶液滴入沸水中,而非NaOH溶液中,C错误;二氧化碳也能和氢氧化钠溶液反应,不能用氢氧化钠溶液除去中少量HCl,应用饱和碳酸氢钠溶液,D错误;故选A.
11.【答案】B
【解析】①对固体充分加热,产生二氧化碳和水蒸气,反应的化学方程式为:将气体先通过足量浓硫酸,吸收水蒸气,再通过足量,与二氧化碳反应生成碳酸钠和氧气,化学方程式为:,用差量法计算可知,当增重0.28g时,消耗的二氧化碳的质量为,其物质的量为,根据关系式可知,消耗的的物质的量为,所以固体的质量为;故选B.
12.【答案】B
【解析】根据氧化还原规律,―1价的氯和+5价的氯在一定条件下可发生氧化还原反应,A正确;氯水具有漂白性,不能用pH试纸测定其pH,B错误;向次氯酸盐中通入,根据强酸制弱酸的原理,可生成HClO,可增强其漂白、杀菌消毒的能力,C正确;d为,可用于自来水的杀菌消毒,D正确;故选B.
13.【答案】A
【解析】中应盛放饱和溶液,目的是吸收中的HCl,C中盛放浓硫酸,目的是除水,A错误;连接装置,打开和,通入待E中出现白色沉淀后,再点燃酒精灯,B正确;化合价变化可知,D中残留的固体只能碳单质,C正确;F装置和气球的作用为检验并收集CO,防止CO污染空气,D正确;故选A.
14.【答案】C
【解析】先向氢氧化钠溶液中通入二氧化碳,再向反应后的溶液中滴加稀盐酸,二氧化碳气体完全放出,故通入与放出的物质的量相同,当生成气体时,发生反应,A曲线生成消耗盐酸的体积,则A曲线产生的最大体积是:,A正确;B曲线中0~50mL没有气体生成,50~75mL有气体生成,没有气体发生的反应消耗HCl多,B溶液通入后,溶质成分为NaOH、,B正确;先向氢氧化钠溶液中通入二氧化碳,后向通入二氧化碳的氢氧化钠溶液中滴加盐酸,当二氧化碳气体完全放出时,溶液的溶质是氯化钠,根据氯离子、钠离子守恒,当所加盐酸体积为75mL时,A、B两溶液所含溶质相同,浓度也相同,C错误;所以,,D正确;故选C.
15.(14分)
【答案】(1)①②④⑧⑩(2分)⑥⑨(2分)
(2)(2分)
(3)胶体(1分)溶液(1分)渗析(1分)
(4)(2分)既是氧化剂又是还原剂(1分)(1分)
(5)正盐(1分)
【解析】(1)电解质是指在水溶液或熔融状态下能导电的化合物,主要物质种类包括酸、碱、盐、金属氧化物、等,属于电解质的是①②④⑧⑩,非电解质是指在水溶液和熔融状态下均不能导电的化合物,主要物质类别包括大多数的有机物、非金属氧化物、等,属于非电解质的是⑥⑨,故答案为①②④⑧⑩、⑥⑨.
(2)在熔融状态电离的方程式为.
(3)淀粉溶液为胶体,NaCl溶液为溶液,胶体粒子不能透过半透膜,溶液中离子可以透过半透膜,可采用渗析的方法进行分离,故答案为胶体,溶液,渗析.
(4)与水的反应的化学方程式为,该反应为中―1价O化合价即升高又降低,故既是氧化剂又是还原剂,每当有1ml参与反应,转移1ml电子,数目为,故答案为,既是氧化剂又是还原剂,.
(5)与足量KOH溶液反应生成,所以不能再电离除,为正盐.
16.(14分)
【答案】(1)a(1分) (1分) b(1分) (1分)
(2)过滤、洗涤、干燥、加热(灼烧)(2分)
(3)取少量样品溶于水,加足量稀硝酸酸化,再滴加少量硝酸银溶液,若出现白色沉淀,说明含有NaCl(2分)
(4)不可行(2分) 把稀盐酸换成稀硫酸,并且将生成的气体先用浓硫酸干燥,再通入碱石灰中(2分)
(5)加水溶解,蒸发浓缩,冷却结晶,过滤,干燥(2分)
【解析】(1)由于在水中的溶解度远大于在水中的溶解度,故通时需要防倒吸,不能伸到液面以下,故应从a管通入,且需要先通入,形成碱性环境,有利于的吸收,故答案为先由a管通入,再由b管通入.
(2)在相同温度条件下,溶解度较小的从水中析出,然后过滤,洗涤,干燥,加热,使的受热分解得到纯碱样品,故答案为过滤、洗涤、干燥、加热(灼烧).
(3)检验出氯离子,则证明含有NaCl杂质,故答案为取少量样品溶于水,加足量稀硝酸酸化,再入硝酸银溶液,若出现白色沉淀,说明含有NaCl.
(4)稀盐酸具有挥发性,故生成的中含有HCl和,这两种杂质也可被碱石灰吸收,故测出的质量偏大,方案不可行.改进方案为把稀盐酸换成稀硫酸,并且将生成的气体先用浓硫酸干燥后再通入碱石灰中.故答案为不可行,把稀盐酸换成稀硫酸,并且将生成的气体先用浓硫酸干燥,再通入碱石灰中.
(5)由图可知,的溶解度随温度升高急剧增大,而NaCl几乎没有变化,故可采用冷却结晶的方式除去NaCl,故答案为加水溶解,蒸发浓缩,冷却结晶,过滤.
17.(15分)
【答案】(1)(2分)
(2)除去中的HCl(2分) 饱和NaCl(2分)
(3)水浴加热(1分) (2分)5:1(2分)
(4)吸收多余的,防止污染空气(2分)
(5)>(1分) <(1分)
【解析】(1)实验室制氯气的化学方程式为:.
(2)中含有挥发出来的HCl,HCl与KOH溶液反应,影响的产率,故应该用饱和食盐水除去HCl,故答案为除去中的HCl,饱和NaCl.
(3)c中采用的水浴加热的方式,反应方程式为,该反应中既是氧化剂又是还原剂,氧化剂和还原剂物质的量之比为5∶1,故答案为水浴加热,,5∶1.
(4)属于污染性气体,不能直接排放,可用NaOH溶液吸收,进行尾气处理,故答案为吸收多余的,防止污染空气.
(5)取c中溶液,滴加浓盐酸并加热,和浓盐酸发生氧化还原反应生成,反应的离子方程式是,通过对比可知,溶液酸碱性影响物质氧化性、还原性的强弱,根据氧化还原反应规律,氧化剂的氧化性大于氧化产物,在碱性条件下氧化性大于,酸性条件下氧化性小于,故答案为>,<.
18.(15分)
【答案】(1)500mL容量瓶、烧杯、玻璃棒、胶头滴管、量筒(3分)
(2)检漏(1分) (3)18.8(1分) (4)C(1分) (5)9.4(2分) B(2分)
(6)(2分) (2分) 浓度(1分)
【解析】(1)配制一定物质的量浓度的溶液需要用到的玻璃仪器为容量瓶(用来配制溶液)、烧杯(溶解)、玻璃棒(用来搅拌和引流)、胶头滴管(用来引流)、量筒(可不写),但容量瓶必须指出所需规格,实验室没有480mL的容量瓶,可采用500mL的容量瓶.
(2)配制溶液最后一步需要盖上瓶塞,上下颠倒摇匀,故容量瓶不能漏液,在使用之前需要检查是否漏液,故答案为检漏.
(3)用托盘天平称量,精确到0.1g,故称量的胆矾晶体的质量为,故答案为18.8.
(4)A项,如果称量时砝码和胆矾位置放反,称得的胆矾质量偏小,配制溶液浓度偏小;B项,未洗涤烧杯和玻璃棒,则溶质会有损失,配制溶液浓度偏小;C项,定容时俯视容量瓶刻度线,其实液面还未到刻度线处,水加少了,配制溶液浓度偏大;D项,摇匀后液面低于刻度线属于正常现象,无影响,故答案为C.
(5)根据物质的量浓度和质量分数之间的转化公式,可知该“84消毒液”的物质的量浓度,再根据溶液稀释前后溶质的物质的量不变,,故配制250mLNaClO溶液所用“84消毒液”的体积为,应选取10mL的量筒,故答案为9.4,B.
(6)向“84消毒液”中加入稀盐酸,强酸制弱酸,和反应生成HClO可增强漂白效果,向“84消毒液”中加入浓盐酸,和在强酸性条件下发生归中反应生成有毒气体,所以“84消毒液”不能与“洁则灵”(浓盐酸)混合使用,由此可知酸的浓度不同,发生的反应不同,故答案为,,浓度.选项
酸
碱
盐
混合物
A
KOH
自来水
B
HCl
纯碱
盐酸
C
烧碱
KCl
硫酸铁溶液
D
洁净的空气
操作及现象
结论
A
某溶液中加入盐酸,产生能使澄清石灰水变浑浊的无色无味气体
溶液中一定含有
B
向某溶液中滴加氢氧化钠溶液,微热,将湿润的蓝色石蕊试纸放在试管口,试纸变红
溶液中一定含有
C
用洁净铂丝蘸取某溶液在火焰上灼烧,火焰呈黄色
该溶液一定为钠盐溶液
D
向某溶液中先加足量稀盐酸,无沉淀,再加入溶液,有白色沉淀生成
溶液中一定含有
选项
A
B
C
D
实验
目的
Na在空气中燃烧
配制100mL稀硫酸
制备氢氧化铁胶体
除去中少量HCl
84消毒液
[有效成分]NaClO
[规格]1000mL
[质量分数]25%
[密度]
相关试卷
这是一份甘肃省武威市天祝一中、民勤一中、古浪一中等四校联考2023-2024学年高一上学期11月期中考试化学试题,共9页。试卷主要包含了本卷主要考查内容等内容,欢迎下载使用。
这是一份2022-2023学年湖北省宜城一中、枣阳一中等六校联考高一上学期期中考试化学试题PDF版含答案,文件包含湖北省宜城一中枣阳一中等六校联考2022-2023学年高一上学期期中考试化学试题pdf、高一化学答案及评分标准pdf等2份试卷配套教学资源,其中试卷共8页, 欢迎下载使用。
这是一份2022-2023学年湖北省宜城一中、枣阳一中等六校联考高一上学期期中考试化学试题PDF版含答案,文件包含湖北省宜城一中枣阳一中等六校联考2022-2023学年高一上学期期中考试化学试题pdf、高一化学答案及评分标准pdf等2份试卷配套教学资源,其中试卷共8页, 欢迎下载使用。








