




河南省环际大联考“逐梦计划”2023-2024学年高二上学期期中考试化学Word版含答案
展开高二化学试题
(试卷总分:100分 考试时间:75分钟)
注意事项:
1.答卷前,考生务必将自己的学校、班级、姓名、准考证号填写在答题卡上.
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑.如需改动,用橡皮擦干净后,再选涂其他答案标号.回答非选择题时,将答案写在答题卡上.写在本试卷上无效.
3.考试结束后,将本试卷和答题卡一并交回.
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Ca-40 Cl-35.5 K-39 S-32
一、选择题:本题共15小题,每小题3分,共45分,每小题只有一个选项符合题意.
1.中华传统文化蕴含着丰富的化学知识,下列诗句中主要涉及吸热反应的是( )
A.白居易《赋得古原草送别》:“野火烧不尽,春风吹又生.”
B.苏轼《石炭》:“投泥泼水愈光明,烁玉流金见精悍.”
C.于谦《咏煤炭》:“爝火燃回春浩浩,烘炉照破夜沉沉.”
D.李商隐《无题·相见时难别亦难》:“春蚕到死丝方尽,蜡炬成灰泪始干.”
2.密闭容器中反应达到平衡.其他条件不变时,不能使正反应速率加快的措施是( )
A.通入水蒸气B.缩小容器体积C.分离出D.升高温度
3.下列能用勒夏特列原理解释的有几个( )
①溶液中加入固体后颜色变深②棕红色加压后颜色先变深后变浅 ③氯水宜保存在低温、避光条件下④实验室用排饱和食盐水的方法收集氯气⑤由、、组成的平衡体系加压(缩小体积)后颜色变深⑥合成氨时将氨液化分离,可提高原料的利用率
A.6B.5C.4D.3
4.在密闭容器中的一定量混合气体发生反应:,平衡时测得C的浓度为.保持温度不变,将容器的容积压缩到原来的一半,再达到平衡时,测得C的浓度变为.下列有关判断不正确的是( )
A.C的体积分数增大了B.A的转化率降低了
C.平衡向逆反应方向移动D.
5.下列叙述正确的是( )
A.已知,,则;
B.已知,则含的稀溶液与足量稀醋酸完全中和,放出的热量等于;
C.已知P(白磷,s)=P(红磷,s),,则白磷比红磷稳定;
D.已知,向密闭容器中加入和,充分反应后放出的热量小于.
6.已知:,若反应速率分别用、、、[单位为]表示,则正确的关系式是( )
A.B.
C.D.
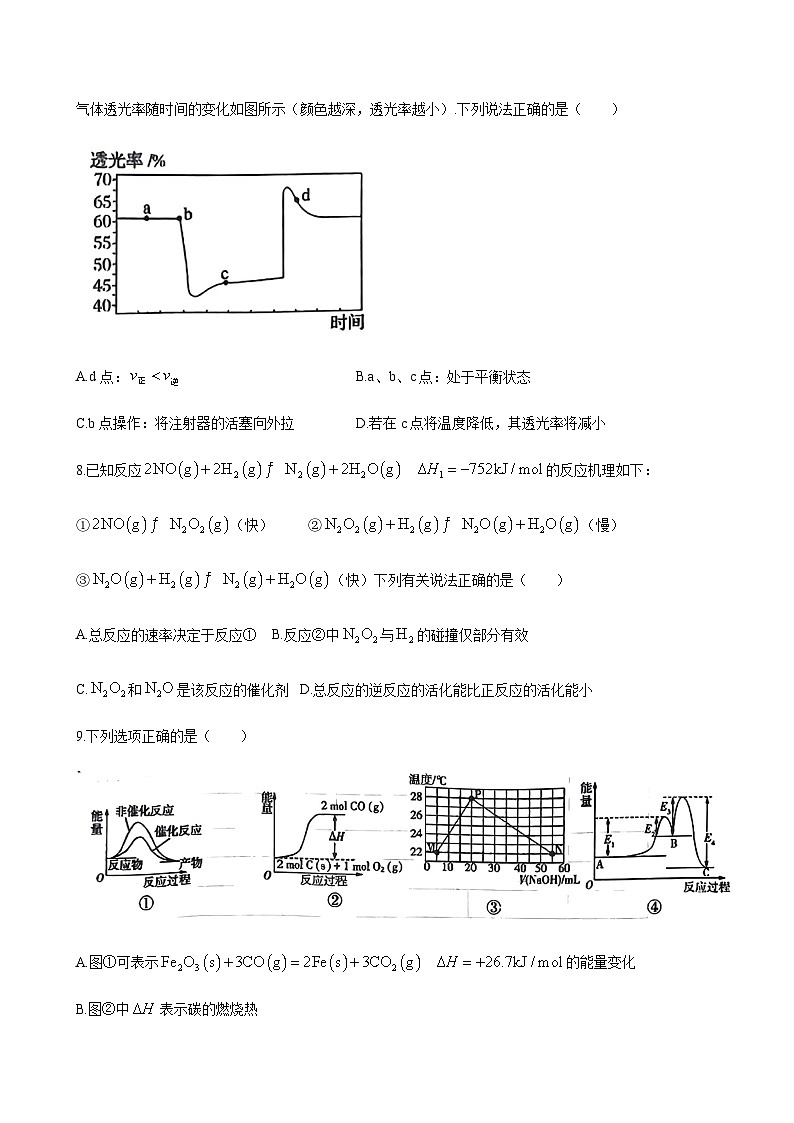
7.(红棕色)(无色) .将一定是的充入注射器中并密封,改变活塞位置,气体透光率随时间的变化如图所示(颜色越深,透光率越小).下列说法正确的是( )
A.d点:B.a、b、c点:处于平衡状态
C.b点操作:将注射器的活塞向外拉D.若在c点将温度降低,其透光率将减小
8.已知反应的反应机理如下:
①(快) ②(慢)
③(快)下列有关说法正确的是( )
A.总反应的速率决定于反应①B.反应②中与的碰撞仅部分有效
C.和是该反应的催化剂D.总反应的逆反应的活化能比正反应的活化能小
9.下列选项正确的是( )
A.图①可表示的能量变化
B.图②中表示碳的燃烧热
C.实验的环境温度为20℃,将物质的量浓度相等、体积分别为、的、溶液混合,测得混合液最高温度如图③(已知)
D.已知稳定性:,某反应由两步构成,反应过程中的能量变化如图④
10.500℃时,某反应达到平衡,平衡常数.恒容时升高温度,浓度增大.下列说法正确的是( )
A.该反应的,降低温度将缩短反应达到平衡的时间
B.恒温恒容下,充入惰性气体,转化率增大
C.增大反应体系的压强,正反应速率增大,逆反应速率减小
D.在、时刻,的浓度分别是、,则时间间隔内,生成的平均速率为
11.反应可用于纯硅的制备.下列有关该反应的说法正确的是( )
A.该反应、
B.该反应的平衡常数
C.高温下反应每生成需消耗
D.用表示键能,该反应
12.我国科研人员提出了由和转化为高附加值产品的催化反应历程,该历程如图所示,下列说法正确的是( )
A.该反应为吸热反应
B.反应过程中,只有键发生断裂
C.状态①②之间的能量差即该反应的焓变
D.合适的催化剂可有效降低活化能
13.反应,在不同温度下的平衡体系中物质Y的体积分数随压强变化的曲线如图所示.下列说法错误的是( )
A.该反应的B.
C.B、C两点化学平衡常数:D.A、C两点的反应速率
14.下图所示为工业合成氨的流程图.下列有关说法错误的是( )
A.步骤①中“净化”可以防止催化剂中毒
B.步骤②中“加压”既可以提高原料的转化率,又可以加快反应速率
C.步骤③、④、⑤均有利于提高原料的平衡转化率
D.产品液氨除可生产化肥外,还可用作制冷剂
15.温度为时,将1.6ml气体X和1.6ml气体Y充入10L恒容密闭容器中,发生反应,一段时间后达到平衡.反应过程中测定的数据如表,下列说法正确的是( )
A.内的平均反应速率
B.时,反应的平衡常数
C.其他条件不变,后,向容器中再充入,平衡向正反应方向移动,与改变条件前相比再次达到平衡时X的浓度减小,Y的转化率增大
D.其他条件不变,降温到达到化学平衡时,平衡常数,则该反应为放热反应
二、非选择题:本题共4小题,共55分.
16.(每空2分,共16分)某实验小组用溶液和硫酸溶液进行中和热的测定.
(一)配制溶液.
(1)若实验中大约要使用溶液,至少需要称量固体___________g.
(2)从下图中选择称量固体所需要的仪器(填字母).
(二)测定稀硫酸和稀氢氧化钠反应的中和热的实验装置如图所示.
(3)写出该反应的热化学方程式(中和热)
___________________________________________________________.
(4)取溶液和硫酸溶液进行实验,实验数据如下表.
①请填写表中的空白:
②近似认为溶液和硫酸溶液的密度都是,中和后生成溶液比热容.则测得中和热_________(取小数点后一位).
③上述实验数值结果与有偏差,产生偏差的原因可能是___________(填字母).
A.实验装置保温、隔热效果差
B.分多次把溶液倒入盛有硫酸的小烧杯中
C.用温度计测定溶液起始温度后直接测定硫酸溶液的温度
(5)现将一定量的稀溶液、稀溶液、稀氨水分别和的稀盐酸恰好完全反应,其反应热分别为、、,则、、的大小关系为________________.
(6)下列变化过程属于吸热反应的是___________(填序号).
①浓硫酸稀释 ②酸碱中和反应 ③木炭在中燃烧 ④煅烧石灰石 ⑤C与水蒸气反应制取水煤气 ⑥锌和稀硫酸反应制取⑦C还原
17.(每空2分,共14分)回答下列问题:
(1)微生物作用下,经过两步反应被氧化成.两步反应的能量变化示意图如图:
全部氧化成的热化学方程式是__________________.
(2)高能燃料肼,俗称联氨.在工业生产中用途广泛.已知,计算燃烧生成氮气和液态水(反应①)时放出的热量为___________.相同条件下,若生成氮气和水蒸气(反应②),则反应②放出的热量比①____________(填“多”或“少”).
(3)甲醇是一种重要的化工原料,可用于合成甲醇,发生反应:.在一容积可变的密闭容器中充有与,在催化剂作用下发生反应生成甲醇.的平衡转化率与温度、压强的关系如图所示.
①________(填“>”“<”或“=”)
②A、B、C三点的平衡常数(、、)大小关系为__________(用“>”“<”或“=”连接,下同)
③A、B、C三点容器内混合气体的平均摩尔质量(、、)大小关系为______________.
④下列可作为反应达到化学平衡状态的标志的是___________(填字母)
A.、的物质的量之比保持不变
B.生成的同时生成
C.、、的物质的量之比为
D.的体积分数不再变化
18.(除注明外,每空2分,共13分)某课外兴趣小组用实验探究影响化学反应速率的因素、化学平衡状态.
(1)探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如表系列实验:
①写出该反应的离子方程式___________________________.
②该实验1和3可探究_____________对反应速率的影响,因此_________mL.实验1和2可探究温度对反应速率的影响,因此___________mL.
(2)为更精确地研究浓度对反应速率的影响,小组同学利用压强传感器(测体系压强变化)等数字化实验设备,探究镁与不同浓度硫酸的反应速率,两组实验所用药品如表:
实验结果如图所示:
①实验Ⅰ对应图中曲线___________(填字母).
②随着反应的不断进行,化学反应速率减慢,主要原因是____________________.
(3)探究反应“”为可逆反应.
试剂:溶液,溶液,淀粉溶液,溶液,溶液.实验如图:
甲同学认为通过试管i中现象可证明该反应为可逆反应,理由是_______________________.
乙同学认为依据ii中现象无法证明该反应为可逆反应,原因为_______________________.
19.(除注明外,每空2分,共12分)甲烷水蒸气重整制取合成气的反应如下:.请回答下列问题:
(1)上述反应能自发进行的理由是_______________,条件是____________(填“低温”“高温”或“任何条件”).
(2)向容积为2L的密闭容器中,按投料,
a.保持温度为时,测得的浓度随时间变化曲线如图1所示.
b.其他条件相同时,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,反应相同时间后,的转化率随反应温度的变化如图2所示.
图1 图2
①结合图1,写出反应达到平衡的过程中的能量变化:吸收___________用含有、的代数式表示).
②在图1中画出:起始条件相同,保持温度为时,随时间的变化曲线.
③根据图2判断:的转化率:,原因是____________________.
(3)①设起始,在恒压下,平衡时与和(温度)的关系如图3所示:[其中为的体积分数]
图3
比较图3中、与3的大小关系_____________(请按从大到小的顺序书写).
②对于气相反应,用某组分B的平衡压强代替物质的量浓度也可表示平衡常数,记作,如,为平衡总压强,为平衡系统中B的物质的量分数.则图3中X点时,____________.
2
4
7
9
1.2
1.1
1.0
1.0
序号
a
b
c
d
e
f
仪器
实验次数
起始温度
终止温度
温度差平均值
平均值
1
26.2
26.0
26.1
30.1
_______________________________
2
27.0
27.4
27.2
33.3
3
25.9
25.9
25.9
29.8
4
26.4
26.2
26.3
30.4
实验序号
反应温度
浓度
稀硫酸
1
20
10.0
0.10
10.0
0.50
0
2
40
0.10
0.50
3
20
0.10
4.0
0.50
序号
镁条的质量(大小相同)/g
硫酸
物质的量浓度
体积/mL
实验Ⅰ
10
1.0
2
实验Ⅱ
10
0.5
2
河南省驻马店市环际大联考“逐梦计划”2023-2024学年高一上学期12月阶段考试(三)化学试题含答案: 这是一份河南省驻马店市环际大联考“逐梦计划”2023-2024学年高一上学期12月阶段考试(三)化学试题含答案,共31页。试卷主要包含了5 Fe, 下列离子方程式正确是等内容,欢迎下载使用。
河南省驻马店市“逐梦计划”环际大联考2023-2024学年高一上学期12月阶段考试(三)化学试题含答案: 这是一份河南省驻马店市“逐梦计划”环际大联考2023-2024学年高一上学期12月阶段考试(三)化学试题含答案,共13页。试卷主要包含了5 Fe, 下列离子方程式正确的是等内容,欢迎下载使用。
河南省驻马店市环际大联考“逐梦计划”2023-2024学年高一上学期12月阶段考试(三)化学(Word版附解析): 这是一份河南省驻马店市环际大联考“逐梦计划”2023-2024学年高一上学期12月阶段考试(三)化学(Word版附解析),共24页。试卷主要包含了5 Fe, 下列离子方程式正确是等内容,欢迎下载使用。












