

人教版九年级下册第九单元 溶液课题2 溶解度完美版教学ppt课件
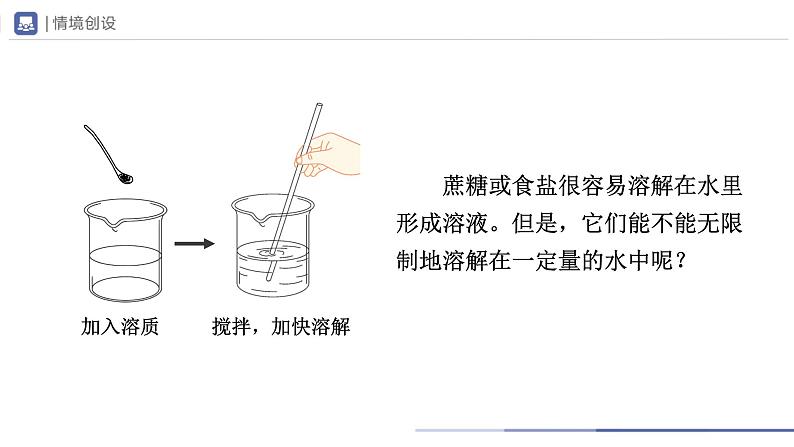
展开蔗糖或食盐很容易溶解在水里形成溶液。但是,它们能不能无限制地溶解在一定量的水中呢?
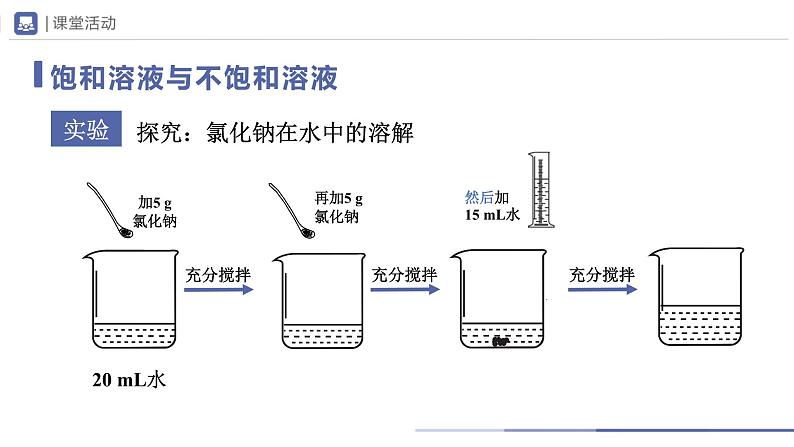
探究:氯化钠在水中的溶解
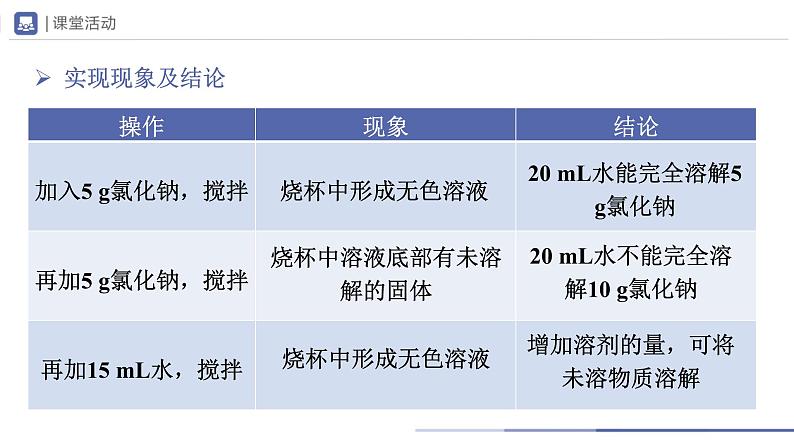
烧杯中溶液底部有未溶解的固体
20 mL水能完全溶解5 g氯化钠
20 mL水不能完全溶解10 g氯化钠
增加溶剂的量,可将未溶物质溶解
在一定温度下,一定量的水中,氯化钠溶解的质量是有限度的,不能无限溶解。增加水的量,可以使氯化钠继续溶解。
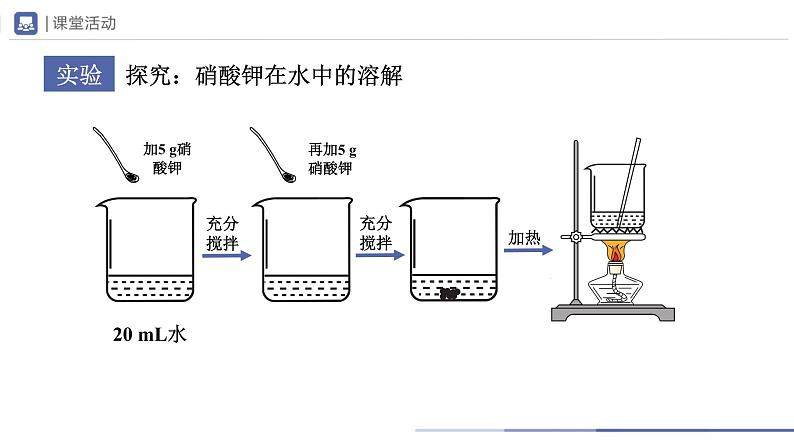
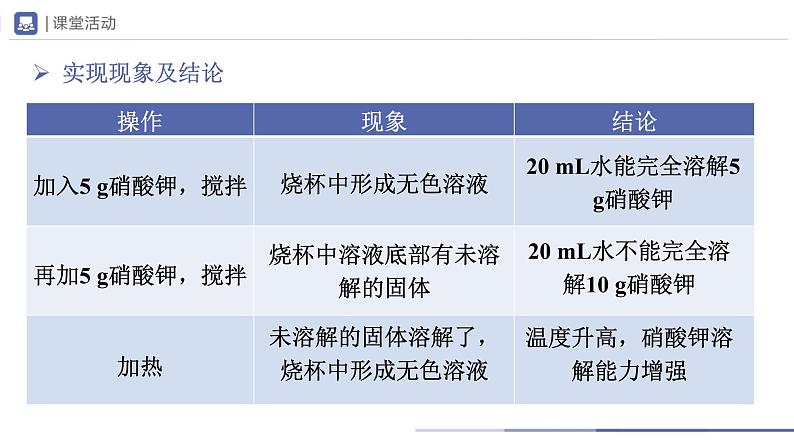
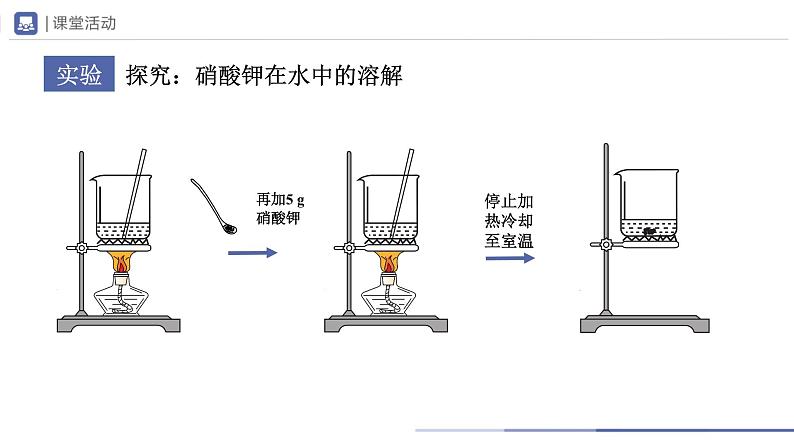
探究:硝酸钾在水中的溶解
20 mL水能完全溶解5 g硝酸钾
20 mL水不能完全溶解10 g硝酸钾
未溶解的固体溶解了,烧杯中形成无色溶液
温度升高,硝酸钾溶解能力增强
温度降低,硝酸钾溶解能力降低
在一定温度下,一定量的水中,硝酸钾溶解的质量是有限度的,不能无限溶解。升高温度,可以使硝酸钾继续溶解,降低温度时,溶液中析出晶体。
饱和溶液与不饱和溶液的概念
在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解时,所得到的溶液叫做这种溶质的饱和溶液。
在一定温度下,向一定量溶剂里加入某种溶质,当溶质还能继续溶解时,该溶液叫做这种溶质的不饱和溶液。
当描述某“饱和溶液”时,要明确以下三点: ①“一定温度”:在不同温度下,物质在一定量溶剂中的溶解限度是不同的。在某温度下的“饱和溶液”,改变温度后可能就变成了不饱和溶液。 ②“一定量溶剂”:在一定温度下,物质在一定量溶剂中的溶解的量是有限的,可以形成饱和溶液。增加溶剂的量,饱和溶液变成不饱和溶液。 ③“这种溶质”:一定温度和一定量溶剂中,A物质不能继续溶解,但不一定所有物质都不能继续溶解,可能B物质还能继续溶解。则该溶液对A物质而言是饱和溶液,对B物质而言则是不饱和溶液。
饱和溶液一定是浓溶液吗?不饱和溶液一定是稀溶液吗?
溶液是否饱和与溶液的浓稀没有必然联系,浓溶液不一定是饱和溶液,也可能是不饱和溶液;稀溶液不一定是不饱和溶液,也可能是饱和溶液,如氢氧化钙的饱和溶液就为稀溶液。
饱和溶液与不饱和溶液的相互转化
(2)硝酸钾继续溶解→不饱和溶液硝酸钾不能继续溶解而有剩余→饱和溶液升高温度硝酸钾继续溶解→不饱和溶液降低温度时溶液中析出晶体→饱和溶液
(1)氯化钠继续溶解→不饱和溶液氯化钠不能继续溶解而有剩余→饱和溶液加水,剩余的氯化钠固体继续溶解→不饱和溶液。
一般情况下,饱和溶液与不饱和溶液之间的相互转化关系如下:
增加溶质、蒸发溶剂或降低温度
在通过升温和降温实现饱和与不饱和溶液转化中,要特别注意氢氧化钙溶液的特殊性:
Ca(OH)2饱和溶液
Ca(OH)2不饱和溶液
当热的硝酸钾溶液冷却以后,烧杯底部出现了固体。这是因为在冷却过程中,硝酸钾不饱和溶液变成了饱和溶液;温度继续降低,过多的硝酸钾会从溶液中以晶体的形式析出,这一过程叫做结晶。
你知道海水晒盐吗?了解海水晒盐的过程,与同学交流。
(1)原理:利用阳光和风力使水分蒸发,食盐结晶出来。(2)条件:溶液达到饱和;温度改变或溶剂减少。(3)方法:①冷却热的饱和溶液法;②蒸发溶剂法。
初中化学人教版九年级下册课题2 溶解度课堂教学ppt课件: 这是一份初中化学人教版九年级下册<a href="/hx/tb_c9866_t3/?tag_id=26" target="_blank">课题2 溶解度课堂教学ppt课件</a>,共12页。PPT课件主要包含了学习目标,重难点,引入新课,教学过程,讲授新课,一定温度下,g溶剂,溶质的质量,达到饱和状态等内容,欢迎下载使用。
初中化学人教版九年级下册课题2 溶解度优秀教学课件ppt: 这是一份初中化学人教版九年级下册<a href="/hx/tb_c9866_t3/?tag_id=26" target="_blank">课题2 溶解度优秀教学课件ppt</a>,共23页。PPT课件主要包含了温度不同,溶剂量不同,固体溶解度,四要素,条件一定温度,状态饱和状态,单位g,概念的理解,刚好形成饱和溶液,溶解性与溶解度的关系等内容,欢迎下载使用。
初中化学课题2 溶解度教学课件ppt: 这是一份初中化学课题2 溶解度教学课件ppt,共26页。PPT课件主要包含了饱和溶液与不饱和溶液,氯化钠完全溶解,有部分氯化钠未溶,硝酸钾完全溶解,部分硝酸钾未溶,升高温度,降低温度,饱和溶液,概念总结,不饱和溶液等内容,欢迎下载使用。













