
河南省安阳市林州市第一中学2023-2024学年高一上学期1月期末化学试题
展开
这是一份河南省安阳市林州市第一中学2023-2024学年高一上学期1月期末化学试题,共8页。
注意事项:
1.答卷前,考生务必将自己的姓名和座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡的相应位置上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 18 Na 23 S 32 Cu 64
第Ⅰ卷 选择题(共45分)
选择题(本题包括15小题,每题3分,共45分,每小题只有一个选项符合题意)
1.下列事实的解释正确的是( )
A.蘸有浓硫酸和蘸有浓氨水的玻璃棒靠近没有白烟,说明硫酸与氨气不反应
B.向50mL 18ml·L-1的H2SO4溶液中加入足量的铜片加热充分反应后,被还原的H2SO4的物质的量等于0.45ml
C.医疗上可用硫酸钡作X射线透视肠胃的内服药,是因为硫酸钡难溶于酸 ,且不易被X射线穿透
D.常温下,浓H2SO4可以用铝制容器贮存,说明铝与浓硫酸不反应
2.NA为阿伏伽德罗常数的值。下列说法正确的是( )
A.标准状况下,3.36L氧气与3.2g硫反应,生成SO2分子数为0.1NA
B.1L0.1 ml·L-1氨水中NH3·H2O分子数为0.1NA
C.标准状况下,0.5ml NO和0.5ml O2组成的混合气体,体积约为22.4L
D.46gNO2和N2O4混合气体中氧原子总数为3NA
3.只用一种试剂,将氯化铵,硫酸铵,氯化钠,硫酸钠四种溶液区分开,这种试剂是( )
A.氢氧化钠溶液 B.硝酸银溶液
C.氯化钡溶液 D.氢氧化钡溶液
4.对于某些物质或离子的检验及结论正确的是( )
A.向某溶液中滴加NaOH溶液后,加热,用湿润蓝色石蕊试纸检验发现变红,该溶液中一定含有NH4+
B.向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,则原溶液一定含有Fe2+
C.向某溶液中加足量盐酸,产生无色无味气体能使澄清石灰水变浑浊,该溶液一定含有CO32-
D.某气体能使湿润淀粉碘化钾试纸变蓝,则该气体一定是氯气
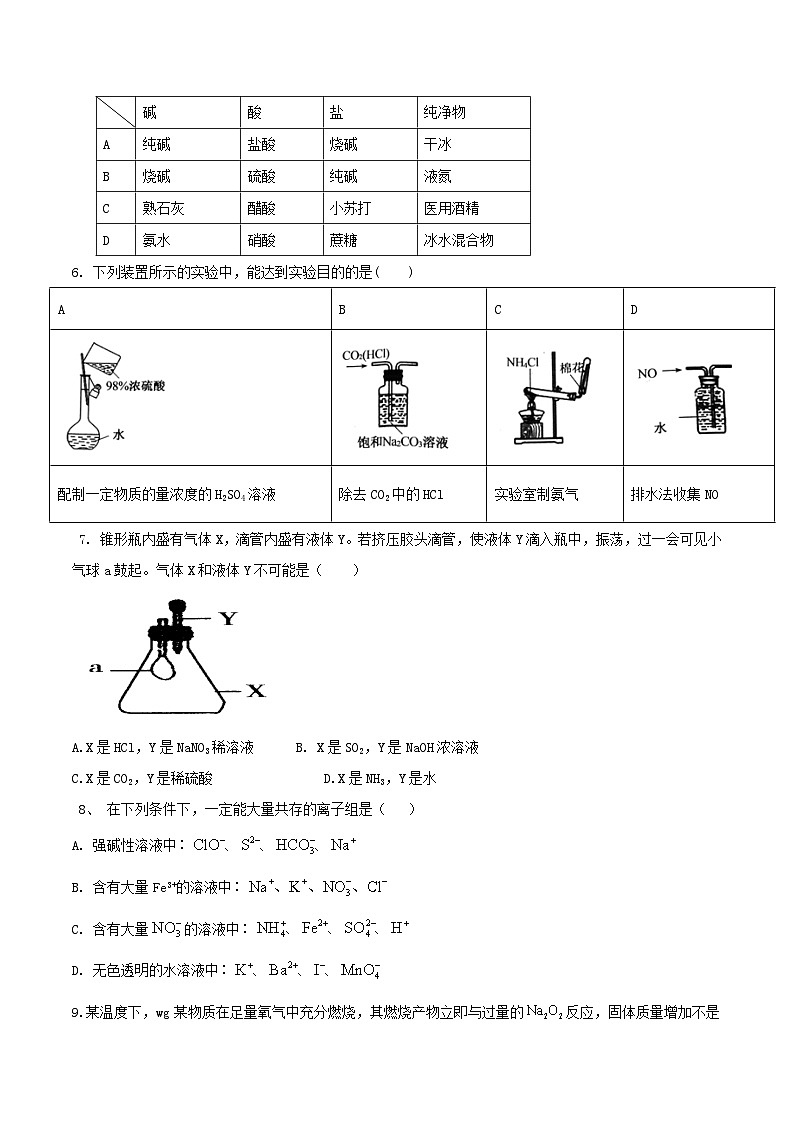
5.下列物质分类的正确组合是( )
6. 下列装置所示的实验中,能达到实验目的的是( )
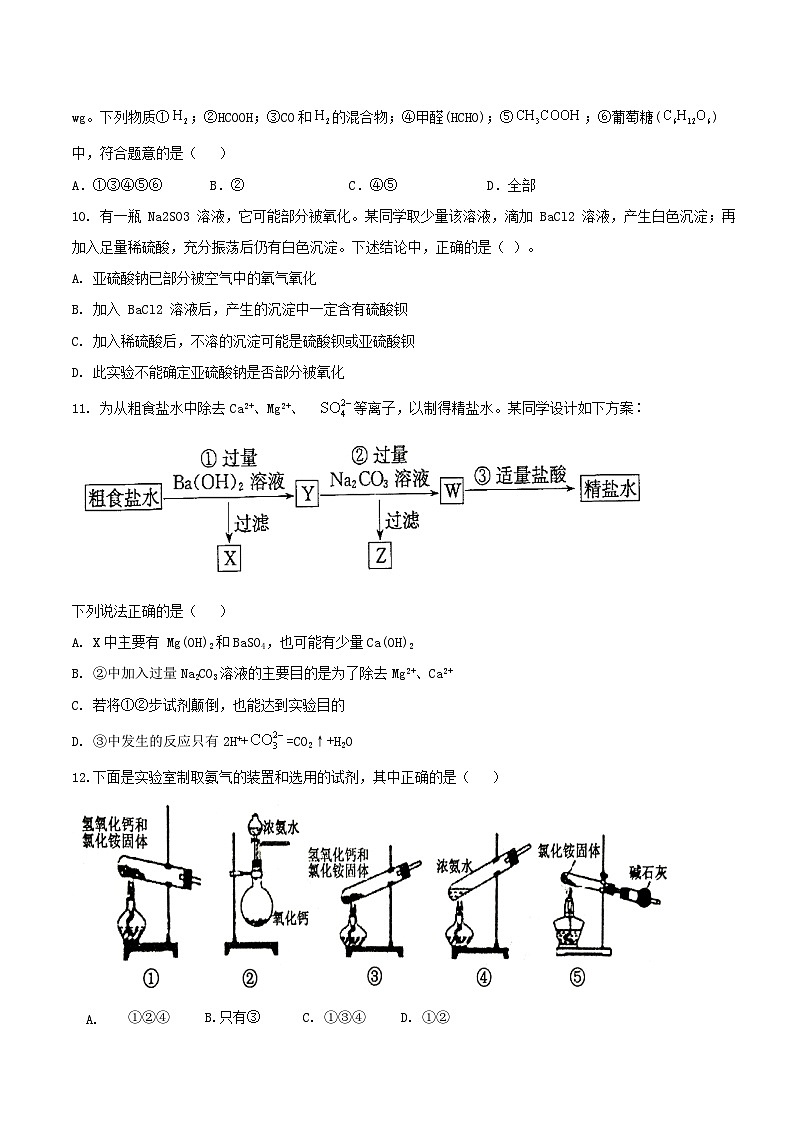
7. 锥形瓶内盛有气体X,滴管内盛有液体Y。若挤压胶头滴管,使液体Y滴入瓶中,振荡,过一会可见小气球a鼓起。气体X和液体Y不可能是( )
A.X是HCl,Y是NaNO3稀溶液 B. X是SO2,Y是NaOH浓溶液
C.X是CO2,Y是稀硫酸 D.X是NH3,Y是水
8、 在下列条件下,一定能大量共存的离子组是( )
A. 强碱性溶液中∶
B. 含有大量Fe3+的溶液中∶
C. 含有大量的溶液中∶
D. 无色透明的水溶液中∶
9.某温度下,wg某物质在足量氧气中充分燃烧,其燃烧产物立即与过量的反应,固体质量增加不是wg。下列物质①;②HCOOH;③CO和的混合物;④甲醛(HCHO);⑤;⑥葡萄糖()中,符合题意的是( )
A.①③④⑤⑥B.②C.④⑤D.全部
10. 有一瓶 Na2SO3 溶液,它可能部分被氧化。某同学取少量该溶液,滴加 BaCl2 溶液,产生白色沉淀;再加入足量稀硫酸,充分振荡后仍有白色沉淀。下述结论中,正确的是( )。
A. 亚硫酸钠已部分被空气中的氧气氧化
B. 加入 BaCl2 溶液后,产生的沉淀中一定含有硫酸钡
C. 加入稀硫酸后,不溶的沉淀可能是硫酸钡或亚硫酸钡
D. 此实验不能确定亚硫酸钠是否部分被氧化
11. 为从粗食盐水中除去Ca2+、Mg2+、 等离子,以制得精盐水。某同学设计如下方案∶
下列说法正确的是( )
A. X中主要有 Mg(OH)2和BaSO4,也可能有少量Ca(OH)2
B. ②中加入过量Na2CO3溶液的主要目的是为了除去Mg2+、Ca2+
C. 若将①②步试剂颠倒,也能达到实验目的
D. ③中发生的反应只有2H++=CO2↑+H2O
12.下面是实验室制取氨气的装置和选用的试剂,其中正确的是( )
①②④ B.只有③ C. ①③④ D. ①②
13. 1.92 g铜投入到一定量浓硝酸中,铜完全溶解,生成气体颜色越来越淡,共收集到标准状况下672mL气体,将盛此气体的容器倒扣在水槽中,通入标准状况下一定体积的氧气,恰好使气体完全溶于水,则通入氧气的体积为 ( )
A、504mL B、336mL C、224mL D、168mL
14.某溶液中可能含有H+,Na+,NH4+、Cl-、SO42-、CO32-中的若干种,现取100mL该溶液进行实验:
第一步:向其中加入足量NaOH溶液并加热,收集到448mL气体(标准状况);
第二步:再向第一步反应后的溶液中加入稀盐酸酸化,有无色气体逸出,接着加入足量BaCl2溶液,得到白色沉淀2.33g。
已知NH4++OH - NH3↑+H2O,结合实验分析下列说法正确的是( )
A.可能存在H+ B.不可能存在Cl-
C.不一定存在Na+ D.该溶液中至少存在四种离子
15.下列离子方程式书写正确的是( )
A. 溶液中加入足量氨水:
B.足量的铁与稀硝酸反应:Fe + 4H+ + NO3-=Fe3+ + NO↑+ 2H2O
C.氢氧化钡溶液中加入少量硫酸氢钠:Ba2++OH—+H++SO42-= BaSO4+H2O
D.NH4HCO3溶液与过量KOH浓溶液共热:NH4++ OH-NH3↑+ H2O
第Ⅱ卷(非选择题,共55分)
填空题
16.(13分) 化学链燃烧是利用载氧体将空气中的氧传输至燃料的新技术。基于载氧体的丙烷化学链燃烧技术原理如图所示。
根据所学知识,回答下列问题:
(1)上述转化图涉及的物质中,属于酸性氧化物的是___________(填化学式)。
(2)标准状况下,与___________的体积相等。同温同压下,等体积的下列气体,和的物质的量之比___________,N2和O2的密度之比___________。
(3)在酸性条件下,可与稀硫酸发生歧化反应生成和单质,写出反应的离子方程式:___________。用胆矾配制240ml物质的量浓度为的溶液,需要称量的胆矾的质量为___________g,配制实验中除需要量筒、烧杯、玻璃棒之外,还需要的玻璃仪器有___________。
17.(16分) 学习常见物质时,会从“价”和“类”两个方面进行学习。如图表示铁元素的常见化合价与含铁物质类别的关系。
(1)X的物质类别是______________。
(2)铁和硫单质反应生成的含铁化合物属于如图中的___________(填序号)。若不引入杂质,将FeCl3溶液转化FeCl2溶液的离子方程式为: 。
(3)某同学弄清了氨的喷泉实验原理后,探究X与浓硝酸反应生成的气体能否用来做喷泉实验:标准状况下,用一充满该气体的烧瓶来做喷泉实验,实验结果水只能充到烧瓶体积的________处,所得溶液的浓度为________ ml·L-1。
(4)某同学欲用物质a制取物质b,设计了如图实验步骤:
物质a与稀盐酸反应的离子方程式为__________________________。
如果向盛有溶液甲的烧杯中滴加NaOH溶液至过量,下面图象能正确表示烧杯中溶液质量变化的是_____(填序号)。
c点对应的阳离子用_______试剂检验(写出化学名称);现象是_______;写出对应的离子方程式_______。
18.(14分)某钢铁厂废水中含有、、、、。某兴趣小组进行如下实验:
回答下列问题:
(1)“沉淀1”的成分是_______(填化学式)。
(2)生成“气体1”的离子方程式为_______,“气体1”的检验方法为_______。
(3)生成“气体2”的离子方程式为_______。
(4)生成“沉淀2”的离子方程式为_______。该步骤_______(填“可以”或“不可以”)证明废水中是否含有“沉淀2”的阴离子。
(5)设计实验证明废水中是否含有:_______。
19.(12分)氨既是一种重要的化工产品,又是一种重要的化工原料。如图为合成氨以及氨催化氧化制硝酸的流程示意图。请回答下列问题。
①N2常用作保护气(如填充灯泡、焊接保护等),原因是_______。
②氧化炉中发生反应的方程式为_______。
③A为_______(填化学式),向吸收塔中持续通入A的作用为_______。
④为避免硝酸工业尾气中氮的氧化物(以NO2为例)污染环境,可在“尾气处理装置”中盛装NaOH溶液(生成产物之一为NaNO2),相关反应的化学方程式为_______。
也可以用碳酸钠溶液吸收NO2,放出无色无味的气体,试写出对应的化学方程式_______。
⑤汽车尾气中含有NO,NO产生的原因是_______(用化学方程式表示)。
高一化学答案
1-5 CADBB 6-10 DCBBD 11-15 AABDC
(13分,除标注外每空2分)
(1)CO2 (1分) (2)①88 ②1:1 ③7:8
(3)① ②12.5 ③250mL容量瓶、胶头滴管
17.(16分,除标注外每空2分)(1)单质(1分) (2)d(1分) 2Fe3++Fe=3Fe2+
(3) 0.045或1/22.4
(4)Fe2O3+6H+=2Fe3++3H2O D
(5)硫氰酸钾或硫氰化钾(1分) 溶液变红色(1分)
18(14分,除标注外每空2分)(1) (1分)
用湿润的红色石蕊试纸检验,试纸变蓝,证明有
不可以 (1分)
(5)取少量废水,加入足量硝酸钡溶液,再取上清液,加入硝酸酸化的硝酸银溶液,有白色沉淀生成,证明废水中有
19.(12分,除标注外每空2分)
① N2中存在N≡N,所以N2的化学性质稳定常用作保护气(1分)
②
③ O2 (1分)
氧气与NO和水发生化学反应生成HNO3,目的是氧化NO,使NO尽量充分转化为HNO3
④
⑤ N2+O2 2NO
碱
酸
盐
纯净物
A
纯碱
盐酸
烧碱
干冰
B
烧碱
硫酸
纯碱
液氮
C
熟石灰
醋酸
小苏打
医用酒精
D
氨水
硝酸
蔗糖
冰水混合物
A
B
C
D
配制一定物质的量浓度的H2SO4溶液
除去CO2中的HCl
实验室制氨气
排水法收集NO
相关试卷
这是一份河南省南阳市部分中学2023-2024学年高一上学期期末联考化学试题(含答案),共9页。试卷主要包含了单选题,非单选题等内容,欢迎下载使用。
这是一份河南省安阳市2023-2024学年高三上学期第一次调研考试化学试题,共16页。试卷主要包含了工业上冶炼钙的原理如下等内容,欢迎下载使用。
这是一份河南省安阳市2023-2024学年高三上学期第一次调研考试化学试题,共8页。







