资料中包含下列文件,点击文件名可预览资料内容








还剩23页未读,
继续阅读
成套系列资料,整套一键下载
- 人教版化学九年级下册10.2《酸和碱的中和反应》第一课时 课件+教案+导学案+分层练习(含答案解析) 课件 22 次下载
- 人教版化学九年级下册10.2《酸和碱的中和反应》第二课时 课件+教案+导学案+分层练习(含答案解析) 课件 21 次下载
- 人教版化学九年级下册11.1《生活中常见的盐》第一课时 课件+教案+导学案+分层练习(含答案解析) 课件 18 次下载
- 人教版化学九年级下册11.1《生活中常见的盐》第二课时 课件+教案+导学案+分层练习(含答案解析) 课件 17 次下载
- 人教版化学九年级下册11.1《生活中常见的盐》第三课时 课件+教案+导学案+分层练习(含答案解析) 课件 16 次下载
人教版化学九年级下册第10单元《酸和碱》复习课件+知识清单+单元测试(含答案解析)
展开
这是一份人教版化学九年级下册第10单元《酸和碱》复习课件+知识清单+单元测试(含答案解析),文件包含人教版化学九年级下册《酸和碱》复习课件pptx、人教版化学九年级下册《酸和碱》单元测试原卷版docx、人教版化学九年级下册《酸和碱》单元测试解析版docx、人教版化学九年级下册《酸和碱》知识清单docx等4份课件配套教学资源,其中PPT共31页, 欢迎下载使用。
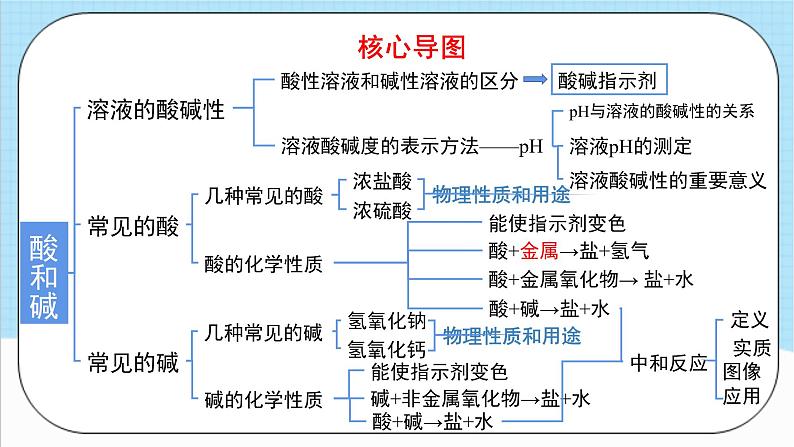
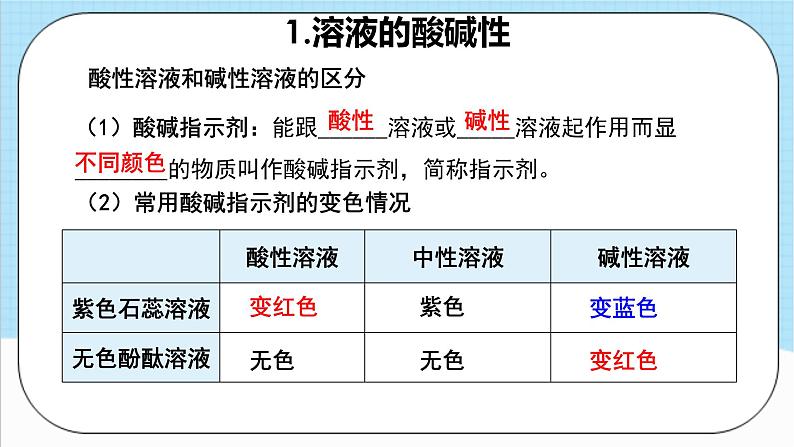
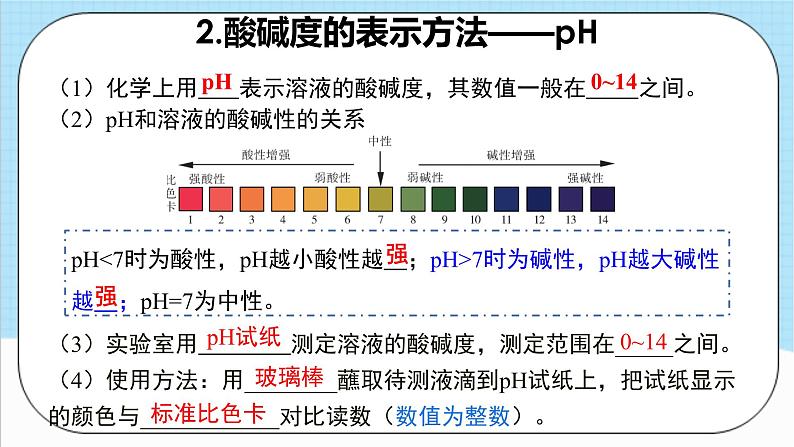
人教版化学九年级下册第10单元《酸和碱》复习目录一 、核心导图二 、复习目录三 、核心考点四、巩固提升酸和碱溶液的酸碱性常见的碱酸性溶液和碱性溶液的区分溶液酸碱度的表示方法——pH几种常见的碱碱的化学性质pH与溶液的酸碱性的关系溶液pH的测定溶液酸碱性的重要意义常见的酸几种常见的酸酸的化学性质物理性质和用途酸碱指示剂浓盐酸浓硫酸能使指示剂变色酸+金属→盐+氢气酸+金属氧化物→ 盐+水酸+碱→盐+水氢氧化钠氢氧化钙物理性质和用途能使指示剂变色碱+非金属氧化物→盐+水酸+碱→盐+水中和反应定义实质图像应用核心导图复习目录溶液的酸碱性和pH核心考点1.溶液的酸碱性酸性溶液和碱性溶液的区分(1)酸碱指示剂:能跟______溶液或_____溶液起作用而显________的物质叫作酸碱指示剂,简称指示剂。酸性碱性不同颜色(2)常用酸碱指示剂的变色情况变红色变蓝色无色紫色变红色无色2.酸碱度的表示方法——pH(1)化学上用 表示溶液的酸碱度,其数值一般在 之间。pH0~14(2)pH和溶液的酸碱性的关系pH<7时为酸性,pH越小酸性越 ;pH>7时为碱性,pH越大碱性越 ;pH=7为中性。强强(3)实验室用 测定溶液的酸碱度,测定范围在_____之间。(4)使用方法:用________蘸取待测液滴到pH试纸上,把试纸显示的颜色与____________对比读数(数值为整数)。0~14玻璃棒标准比色卡pH试纸1.一次性将石灰水、食盐水、稀硫酸鉴别开来,可以选用( )A.紫色石蕊试液 B.无色酚酞试液 C.盐酸 D.二氧化碳A2.人体内的一些液体的正常pH范围如下,其中酸性最强的是( )A.唾液(6.6~7.1) B.血浆(7.35~7.45) C.胃液(0.9~1.5) D.胰液(7.5~8.0)C巩固提升 3.一些物质的近似pH如图所示,下列有关说法正确的是( )A.鸡蛋清的碱性比肥皂水的碱性强 B.厕所清洁剂不会腐蚀大理石地面 C.人被蚊虫叮咬后,在肿包处涂抹牛奶就可减轻痛痒 D.厕所清洁剂与炉具清洁剂不能混合使用D常见的酸核心考点1.几种常见的酸酸的构成: + 。盐酸和硫酸的物理性质及用途H2SO4HCl有刺激性气味吸水性H+ 酸根挥发性2.浓硫酸的腐蚀性和稀释(1)浓硫酸能夺取纸张、木材等中的水,生成黑色的碳,具有强脱水性,有强烈的________,如不慎将浓硫酸沾在衣服或皮肤上,立即用__________,然后再涂上3%~5%的碳酸氢钠溶液。腐蚀性大量水冲洗(2)浓硫酸的稀释:把________沿容器内壁慢慢注入水中,并用玻璃棒不断______,切不可把水倒入浓硫酸中。浓硫酸搅拌3.浓硫酸和浓盐酸的性质大溶质质量减少小溶剂质量增加密封小浓硫酸和浓盐酸敞口久置后的变化4.酸的化学性质紫色石蕊溶液遇酸变 ,无色酚酞溶液遇酸 。(2)酸+金属=__________酸具有相似化学性质的原因: .(3)酸+金属氧化物=_______红盐+氢气盐+水不变色(1)酸与指示剂的作用Fe2O3 +6HCl=2FeCl3 +3H2OFe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2OMg + H2SO4 = MgSO4+H2↑Mg + 2HCl = MgCl2 + H2↑(4)酸+碱→盐+水NaOH+HCl=NaCl+ H2OH2SO4 +2NaOH=Na2SO4 +2 H2O溶液中都含有H+1. 下列有关酸的说法错误的是( )A.浓硫酸要密封保存,这与浓硫酸的挥发性有关 B.浓硫酸、浓盐酸都具有强烈的腐蚀性 C.浓盐酸在空气中会形成白雾 D.浓盐酸和浓硫酸敞口放置,溶质质量分数均减小A巩固提升2.氢溴酸(HBr)的化学性质与盐酸非常相似,下列物质中不可与氢溴酸发生的反应的是( )A.Fe B.CuO C.Ag D.Fe2O3C3.一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的( )A.NaOH溶液 B.NaCl溶液 C.KCl固体 D.硝酸银溶液B4.某同学在实验探究中发现了一些物质之间发生化学反应的颜色变化,如图所示。(1)编号①反应的指示剂是 ;编号②反应的金属单质是 。(2)根据如图可以总结出稀盐酸的化学性质,其中编号②反应的基本反应类型是 反应。(3)请你写出符合编号③反应的化学方程式 。(4)假设编号④反应的盐是AgNO3,则编号④对应方框中的现象是 。紫色石蕊溶液铁置换Fe2O3+6HCl═2FeCl3+3H2O产生白色沉淀常见的碱核心考点1.几种常见的碱1.碱的构成: + 。2.氢氧化钠和氢氧化钙的物理性质及用途金属离子 OH-烧碱苛性钠熟石灰易减小Na2CO3+Ca(OH)2 =CaCO3↓+2NaOHCaO+H2O = Ca(OH)22.碱的化学性质碱具有相似化学性质的原因: .蓝红Na2CO3+H2OCaCO3↓+H2ONa2SO4+2H2OCaCl2+2H2OCu(OH)2↓+Na2SO4Cu(OH)2↓+CaSO4溶液中都含有OH-2.碱的化学性质化学 2NaOH + CO2 = Na2CO3 + H2O大大化学Ca(OH)2+CO2=CaCO3↓+ H2O4410080106下列物质敞口放置后的变化小大小大化学化学1.物质的性质决定其用途。固体氢氧化钠可用作干燥剂,是利用了它的哪种性质( )A.白色固体 B.吸水性 C.腐蚀性 D.能与空气中的二氧化碳反应B2.下列有关氢氧化钠的描述中,正确的是( )A.氢氧化钠在空气中放置会潮解 B.氢氧化钠溶液能使紫色石蕊溶液变红 C.氢氧化钠溶于水吸热 D.氢氧化钠俗称烧碱、火碱、纯碱A巩固提升3.下列有关氢氧化钠性质探究实验的叙述中,错误的是( )A.甲向接近沸腾的水中加入一定量NaOH固体,液体迅速沸腾 B.乙将少量头发加入到热的浓NaOH溶液中,头发逐渐溶解消失 C.丙向氢氧化钠溶液中滴加紫色石蕊试液,观察到溶液变红色 D.丁向盛满CO2气体的集气瓶中加入适量浓烧碱溶液,鸡蛋被吞入瓶中C4.对知识的归纳和总结是学好科学的重要方法。在学习了碱的性质后,小科总结了氢氧化钠的四条化学性质(如图),即氢氧化钠与图中四类物质能够发生化学反应。(1)为了验证氢氧化钠与酸碱指示剂反应,小科将无色酚酞试液滴入氢氧化钠溶液中,溶液由无色变成 色。(2)利用氢氧化钠与酸反应的性质,可以除去氯化钠溶液中少量氢氧化钠杂质,请写出该酸的名称 。 红稀盐酸中和反应及其应用核心考点1.中和反应及其利用1.中和反应:酸+碱→盐+水2.实质:酸中 的和碱中的 结合生成水。 用离子方程式表示为 。3.应用(1)用________改良酸性土壤(2)处理工厂废水(3)用肥皂水治疗蚊虫叮咬(4)用含碱药物治疗胃酸过多H++OH-=H2OH+OH-熟石灰Al(OH)3 + 3HCl=AlCl3 + 3H2OMg(OH)2 + 2HCl=MgCl2 + 2H2O2.中和反应的图像问题向稀盐酸中逐滴滴加NaOH溶液至过量,画出溶液pH随加入NaOH溶液的变化图像。 化学方程式: ; A点:溶质为: (盐酸过量) B点:溶质为: (恰好完全反应)C点:溶质为: ( NaOH过量)NaOH + HCl = NaCl + H2ONaCl和HClNaClNaCl和NaOH·A·B·C1.下列没有运用中和反应原理的是( )A.用熟石灰改良酸性土壤 B.用氢氧化钠溶液洗涤石油产品中的残留硫酸 C.不能用浓硫酸干燥湿润的氨气 D.用生石灰作干燥剂D2. 有关中和反应的说法一定正确的是( )A.反应物均须溶于水 B.有沉淀生成 C.有气体生成 D.有盐生成D巩固提升3.某校化学小组在利用盐酸和氢氧化钠两溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象如图1所示,二者恰好完全反应的微观示意图如图2所示。下列说法不正确的是( )A.该实验是将稀盐酸逐滴滴入到盛有氢氧化钠溶液的烧杯中 B.图1中a点所示溶液中含有的溶质是NaCl和HCl C.图1中由c点到d点的变化过程中没有发生化学反应 D.该反应的实质是H+和OH﹣结合生成H2OB4.如图为向NaOH溶液中加入不同物质时微观粒子变化情况,请分析以下说法正确的是( )A.图甲与图乙涉及的变化都是化学变化 B.KOH与H2SO4反应实质与图乙反应实质相同 C.加入物质后图甲溶液pH不变,图乙溶液pH变小D.该变化前后Na+、OH﹣数量均不会变化B课程结束
人教版化学九年级下册第10单元《酸和碱》复习目录一 、核心导图二 、复习目录三 、核心考点四、巩固提升酸和碱溶液的酸碱性常见的碱酸性溶液和碱性溶液的区分溶液酸碱度的表示方法——pH几种常见的碱碱的化学性质pH与溶液的酸碱性的关系溶液pH的测定溶液酸碱性的重要意义常见的酸几种常见的酸酸的化学性质物理性质和用途酸碱指示剂浓盐酸浓硫酸能使指示剂变色酸+金属→盐+氢气酸+金属氧化物→ 盐+水酸+碱→盐+水氢氧化钠氢氧化钙物理性质和用途能使指示剂变色碱+非金属氧化物→盐+水酸+碱→盐+水中和反应定义实质图像应用核心导图复习目录溶液的酸碱性和pH核心考点1.溶液的酸碱性酸性溶液和碱性溶液的区分(1)酸碱指示剂:能跟______溶液或_____溶液起作用而显________的物质叫作酸碱指示剂,简称指示剂。酸性碱性不同颜色(2)常用酸碱指示剂的变色情况变红色变蓝色无色紫色变红色无色2.酸碱度的表示方法——pH(1)化学上用 表示溶液的酸碱度,其数值一般在 之间。pH0~14(2)pH和溶液的酸碱性的关系pH<7时为酸性,pH越小酸性越 ;pH>7时为碱性,pH越大碱性越 ;pH=7为中性。强强(3)实验室用 测定溶液的酸碱度,测定范围在_____之间。(4)使用方法:用________蘸取待测液滴到pH试纸上,把试纸显示的颜色与____________对比读数(数值为整数)。0~14玻璃棒标准比色卡pH试纸1.一次性将石灰水、食盐水、稀硫酸鉴别开来,可以选用( )A.紫色石蕊试液 B.无色酚酞试液 C.盐酸 D.二氧化碳A2.人体内的一些液体的正常pH范围如下,其中酸性最强的是( )A.唾液(6.6~7.1) B.血浆(7.35~7.45) C.胃液(0.9~1.5) D.胰液(7.5~8.0)C巩固提升 3.一些物质的近似pH如图所示,下列有关说法正确的是( )A.鸡蛋清的碱性比肥皂水的碱性强 B.厕所清洁剂不会腐蚀大理石地面 C.人被蚊虫叮咬后,在肿包处涂抹牛奶就可减轻痛痒 D.厕所清洁剂与炉具清洁剂不能混合使用D常见的酸核心考点1.几种常见的酸酸的构成: + 。盐酸和硫酸的物理性质及用途H2SO4HCl有刺激性气味吸水性H+ 酸根挥发性2.浓硫酸的腐蚀性和稀释(1)浓硫酸能夺取纸张、木材等中的水,生成黑色的碳,具有强脱水性,有强烈的________,如不慎将浓硫酸沾在衣服或皮肤上,立即用__________,然后再涂上3%~5%的碳酸氢钠溶液。腐蚀性大量水冲洗(2)浓硫酸的稀释:把________沿容器内壁慢慢注入水中,并用玻璃棒不断______,切不可把水倒入浓硫酸中。浓硫酸搅拌3.浓硫酸和浓盐酸的性质大溶质质量减少小溶剂质量增加密封小浓硫酸和浓盐酸敞口久置后的变化4.酸的化学性质紫色石蕊溶液遇酸变 ,无色酚酞溶液遇酸 。(2)酸+金属=__________酸具有相似化学性质的原因: .(3)酸+金属氧化物=_______红盐+氢气盐+水不变色(1)酸与指示剂的作用Fe2O3 +6HCl=2FeCl3 +3H2OFe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2OMg + H2SO4 = MgSO4+H2↑Mg + 2HCl = MgCl2 + H2↑(4)酸+碱→盐+水NaOH+HCl=NaCl+ H2OH2SO4 +2NaOH=Na2SO4 +2 H2O溶液中都含有H+1. 下列有关酸的说法错误的是( )A.浓硫酸要密封保存,这与浓硫酸的挥发性有关 B.浓硫酸、浓盐酸都具有强烈的腐蚀性 C.浓盐酸在空气中会形成白雾 D.浓盐酸和浓硫酸敞口放置,溶质质量分数均减小A巩固提升2.氢溴酸(HBr)的化学性质与盐酸非常相似,下列物质中不可与氢溴酸发生的反应的是( )A.Fe B.CuO C.Ag D.Fe2O3C3.一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的( )A.NaOH溶液 B.NaCl溶液 C.KCl固体 D.硝酸银溶液B4.某同学在实验探究中发现了一些物质之间发生化学反应的颜色变化,如图所示。(1)编号①反应的指示剂是 ;编号②反应的金属单质是 。(2)根据如图可以总结出稀盐酸的化学性质,其中编号②反应的基本反应类型是 反应。(3)请你写出符合编号③反应的化学方程式 。(4)假设编号④反应的盐是AgNO3,则编号④对应方框中的现象是 。紫色石蕊溶液铁置换Fe2O3+6HCl═2FeCl3+3H2O产生白色沉淀常见的碱核心考点1.几种常见的碱1.碱的构成: + 。2.氢氧化钠和氢氧化钙的物理性质及用途金属离子 OH-烧碱苛性钠熟石灰易减小Na2CO3+Ca(OH)2 =CaCO3↓+2NaOHCaO+H2O = Ca(OH)22.碱的化学性质碱具有相似化学性质的原因: .蓝红Na2CO3+H2OCaCO3↓+H2ONa2SO4+2H2OCaCl2+2H2OCu(OH)2↓+Na2SO4Cu(OH)2↓+CaSO4溶液中都含有OH-2.碱的化学性质化学 2NaOH + CO2 = Na2CO3 + H2O大大化学Ca(OH)2+CO2=CaCO3↓+ H2O4410080106下列物质敞口放置后的变化小大小大化学化学1.物质的性质决定其用途。固体氢氧化钠可用作干燥剂,是利用了它的哪种性质( )A.白色固体 B.吸水性 C.腐蚀性 D.能与空气中的二氧化碳反应B2.下列有关氢氧化钠的描述中,正确的是( )A.氢氧化钠在空气中放置会潮解 B.氢氧化钠溶液能使紫色石蕊溶液变红 C.氢氧化钠溶于水吸热 D.氢氧化钠俗称烧碱、火碱、纯碱A巩固提升3.下列有关氢氧化钠性质探究实验的叙述中,错误的是( )A.甲向接近沸腾的水中加入一定量NaOH固体,液体迅速沸腾 B.乙将少量头发加入到热的浓NaOH溶液中,头发逐渐溶解消失 C.丙向氢氧化钠溶液中滴加紫色石蕊试液,观察到溶液变红色 D.丁向盛满CO2气体的集气瓶中加入适量浓烧碱溶液,鸡蛋被吞入瓶中C4.对知识的归纳和总结是学好科学的重要方法。在学习了碱的性质后,小科总结了氢氧化钠的四条化学性质(如图),即氢氧化钠与图中四类物质能够发生化学反应。(1)为了验证氢氧化钠与酸碱指示剂反应,小科将无色酚酞试液滴入氢氧化钠溶液中,溶液由无色变成 色。(2)利用氢氧化钠与酸反应的性质,可以除去氯化钠溶液中少量氢氧化钠杂质,请写出该酸的名称 。 红稀盐酸中和反应及其应用核心考点1.中和反应及其利用1.中和反应:酸+碱→盐+水2.实质:酸中 的和碱中的 结合生成水。 用离子方程式表示为 。3.应用(1)用________改良酸性土壤(2)处理工厂废水(3)用肥皂水治疗蚊虫叮咬(4)用含碱药物治疗胃酸过多H++OH-=H2OH+OH-熟石灰Al(OH)3 + 3HCl=AlCl3 + 3H2OMg(OH)2 + 2HCl=MgCl2 + 2H2O2.中和反应的图像问题向稀盐酸中逐滴滴加NaOH溶液至过量,画出溶液pH随加入NaOH溶液的变化图像。 化学方程式: ; A点:溶质为: (盐酸过量) B点:溶质为: (恰好完全反应)C点:溶质为: ( NaOH过量)NaOH + HCl = NaCl + H2ONaCl和HClNaClNaCl和NaOH·A·B·C1.下列没有运用中和反应原理的是( )A.用熟石灰改良酸性土壤 B.用氢氧化钠溶液洗涤石油产品中的残留硫酸 C.不能用浓硫酸干燥湿润的氨气 D.用生石灰作干燥剂D2. 有关中和反应的说法一定正确的是( )A.反应物均须溶于水 B.有沉淀生成 C.有气体生成 D.有盐生成D巩固提升3.某校化学小组在利用盐酸和氢氧化钠两溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象如图1所示,二者恰好完全反应的微观示意图如图2所示。下列说法不正确的是( )A.该实验是将稀盐酸逐滴滴入到盛有氢氧化钠溶液的烧杯中 B.图1中a点所示溶液中含有的溶质是NaCl和HCl C.图1中由c点到d点的变化过程中没有发生化学反应 D.该反应的实质是H+和OH﹣结合生成H2OB4.如图为向NaOH溶液中加入不同物质时微观粒子变化情况,请分析以下说法正确的是( )A.图甲与图乙涉及的变化都是化学变化 B.KOH与H2SO4反应实质与图乙反应实质相同 C.加入物质后图甲溶液pH不变,图乙溶液pH变小D.该变化前后Na+、OH﹣数量均不会变化B课程结束
相关资料
更多









