






还剩15页未读,
继续阅读
所属成套资源:科粤版化学九年级下册 全册课件+内嵌视频
成套系列资料,整套一键下载
科粤版九年级下册8.2 常见的酸和碱课文配套课件ppt
展开
这是一份科粤版九年级下册8.2 常见的酸和碱课文配套课件ppt,共23页。PPT课件主要包含了人的胃液里含有盐酸,汽车电瓶里含有硫酸,学习目标,新知学习,常见的酸,H2SO4,HCl,HNO3,食品化工生产,燃料炸药等内容,欢迎下载使用。
1.人的胃液里含有什么酸?2.汽车电瓶里含有什么酸?
它们有哪些性质吗?它们在生产、生活中又有哪些应用?
1.知道常见的酸,掌握硫酸、盐酸、硝酸的物理性质及用途,了解浓硫酸的特性与稀释方法。2.掌握稀酸的化学通性。
盐酸、硫酸、硝酸都是常见的重要的酸
车用电池、化肥、农药、精炼石油
瓶口出现白雾,这是因为浓盐酸挥发出来的氯化氢气体跟空气中的水蒸气接触,形成盐酸小液滴的缘故。
盐酸:将氯化氢气体(HCl)溶于水后可以形成盐酸,是一种溶液,溶质是氯化氢气体(HCl),溶剂是水。
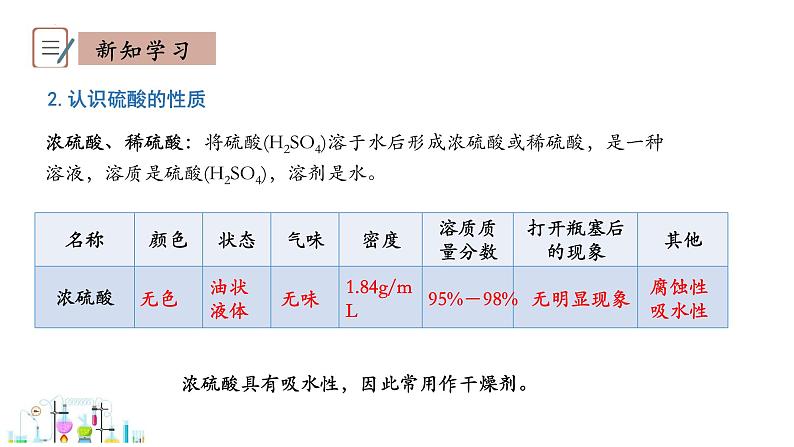
浓硫酸、稀硫酸:将硫酸(H2SO4)溶于水后形成浓硫酸或稀硫酸,是一种溶液,溶质是硫酸(H2SO4),溶剂是水。
浓硫酸具有吸水性,因此常用作干燥剂。
小木条蘸有浓硫酸的部位变黑
实验表明:浓硫酸很快使蔗糖、纸张等脱水,变成碳,可见它有强脱水性。
浓硫酸对衣物、皮肤等有强腐蚀性,如果不慎沾上硫酸,应立即用大量水冲洗,然后涂上3%〜5%的碳酸氢钠溶液。
浓硫酸是危险品,保管和使用都要格外小心。
将浓硫酸沿器壁慢慢注入水里,并用玻璃棒不断搅拌。
将水倒入浓硫酸的过程中,由于浓硫酸密度比水大,把水倒入浓硫酸中,水浮在浓硫酸上面,浓硫酸溶于水放出大量的热使水剧烈沸腾,热的强酸性液滴飞溅,十分危险。
1.酸与酸碱指示剂反应
结论:盐酸和硫酸都可以使石蕊试液变红,使无色酚酞试液不变色。
2.酸与较活泼金属反应
有气泡产生,反应速率:镁>铝>锌>铁
较活泼金属+ 酸 ↓ 盐 + 氢气
①Zn + 2HCl === ZnCl2 + H2↑ ②Mg + 2HCl === MgCl2 + H2↑③2Al + 6HCl === 2AlCl3 + 3H2↑④Fe + 2HCl === FeCl2 + H2↑
盐:由金属阳离子和酸根阴离子构成的化合物
3.酸与金属氧化物反应
金属氧化物+ 酸 ↓ 盐 + 氢气
Fe2O3+3H2SO4 == Fe2(SO4)3 + 3H2O
盐+ 酸 ↓ 新盐 + 新酸
AgNO3+HCl == AgCl ↓+ HNO3
注意:反应生成的氯化银呈白色沉淀,且不溶于稀硝酸,是检验氯离子的试剂。
1.能使紫色石蕊试液变红;2.能与某些金属氧化物反应,生成盐和水;3.能与某些金属反应,生成盐和氢气;4.能与部分盐反应,生成新盐和新酸。
1.列物质不属于酸类的是( )A. H2S B. HCl C. NaHSO4 D. H2CO3
2.下列变化中有一种变化与其它三种变化不同的是( )A.浓盐酸打开瓶塞,瓶口形成白雾 B.浓硫酸敞口放置,溶液质量增加C.盛石灰水的试剂瓶壁产生一层白膜D.滴有酚酞试液的氢氧化钠溶液中加入木炭后红色消失
3.如图是稀释浓硫酸实验的示意图.( 1 )写出图中a、b 两种仪器的名称:______、______( 2 ) b 容器所盛的试剂是 (填“水”或“浓硫酸”);( 3 )稀释时,若两种试剂添加顺序颠倒,将会发生 ;( 4 )[联系与拓展]据媒体报道,2019 年5 月有一村民在家里误将装在酒瓶中的稀硫酸当成白酒喝下,造成食道和胃严重损伤,这是因为稀硫酸具有 ;这一事件警示我们,家中存放或使用药物时应注意 。
4.下列不能直接由金属与稀盐酸反应制得的是( )A.氯化镁 B.氯化亚铁 C.氯化铁 D.氯化铝
5.将一枚生锈的铁钉(主要成份是Fe2O3)放入试管中,滴入足量稀盐酸,发现________消失,并产生_________,化学方程式表示可用_____________________________、_______________________。
6HCl + Fe2O3=2FeCl3 +3H2O
2HCl + Fe=FeCl2+H2↑
1.人的胃液里含有什么酸?2.汽车电瓶里含有什么酸?
它们有哪些性质吗?它们在生产、生活中又有哪些应用?
1.知道常见的酸,掌握硫酸、盐酸、硝酸的物理性质及用途,了解浓硫酸的特性与稀释方法。2.掌握稀酸的化学通性。
盐酸、硫酸、硝酸都是常见的重要的酸
车用电池、化肥、农药、精炼石油
瓶口出现白雾,这是因为浓盐酸挥发出来的氯化氢气体跟空气中的水蒸气接触,形成盐酸小液滴的缘故。
盐酸:将氯化氢气体(HCl)溶于水后可以形成盐酸,是一种溶液,溶质是氯化氢气体(HCl),溶剂是水。
浓硫酸、稀硫酸:将硫酸(H2SO4)溶于水后形成浓硫酸或稀硫酸,是一种溶液,溶质是硫酸(H2SO4),溶剂是水。
浓硫酸具有吸水性,因此常用作干燥剂。
小木条蘸有浓硫酸的部位变黑
实验表明:浓硫酸很快使蔗糖、纸张等脱水,变成碳,可见它有强脱水性。
浓硫酸对衣物、皮肤等有强腐蚀性,如果不慎沾上硫酸,应立即用大量水冲洗,然后涂上3%〜5%的碳酸氢钠溶液。
浓硫酸是危险品,保管和使用都要格外小心。
将浓硫酸沿器壁慢慢注入水里,并用玻璃棒不断搅拌。
将水倒入浓硫酸的过程中,由于浓硫酸密度比水大,把水倒入浓硫酸中,水浮在浓硫酸上面,浓硫酸溶于水放出大量的热使水剧烈沸腾,热的强酸性液滴飞溅,十分危险。
1.酸与酸碱指示剂反应
结论:盐酸和硫酸都可以使石蕊试液变红,使无色酚酞试液不变色。
2.酸与较活泼金属反应
有气泡产生,反应速率:镁>铝>锌>铁
较活泼金属+ 酸 ↓ 盐 + 氢气
①Zn + 2HCl === ZnCl2 + H2↑ ②Mg + 2HCl === MgCl2 + H2↑③2Al + 6HCl === 2AlCl3 + 3H2↑④Fe + 2HCl === FeCl2 + H2↑
盐:由金属阳离子和酸根阴离子构成的化合物
3.酸与金属氧化物反应
金属氧化物+ 酸 ↓ 盐 + 氢气
Fe2O3+3H2SO4 == Fe2(SO4)3 + 3H2O
盐+ 酸 ↓ 新盐 + 新酸
AgNO3+HCl == AgCl ↓+ HNO3
注意:反应生成的氯化银呈白色沉淀,且不溶于稀硝酸,是检验氯离子的试剂。
1.能使紫色石蕊试液变红;2.能与某些金属氧化物反应,生成盐和水;3.能与某些金属反应,生成盐和氢气;4.能与部分盐反应,生成新盐和新酸。
1.列物质不属于酸类的是( )A. H2S B. HCl C. NaHSO4 D. H2CO3
2.下列变化中有一种变化与其它三种变化不同的是( )A.浓盐酸打开瓶塞,瓶口形成白雾 B.浓硫酸敞口放置,溶液质量增加C.盛石灰水的试剂瓶壁产生一层白膜D.滴有酚酞试液的氢氧化钠溶液中加入木炭后红色消失
3.如图是稀释浓硫酸实验的示意图.( 1 )写出图中a、b 两种仪器的名称:______、______( 2 ) b 容器所盛的试剂是 (填“水”或“浓硫酸”);( 3 )稀释时,若两种试剂添加顺序颠倒,将会发生 ;( 4 )[联系与拓展]据媒体报道,2019 年5 月有一村民在家里误将装在酒瓶中的稀硫酸当成白酒喝下,造成食道和胃严重损伤,这是因为稀硫酸具有 ;这一事件警示我们,家中存放或使用药物时应注意 。
4.下列不能直接由金属与稀盐酸反应制得的是( )A.氯化镁 B.氯化亚铁 C.氯化铁 D.氯化铝
5.将一枚生锈的铁钉(主要成份是Fe2O3)放入试管中,滴入足量稀盐酸,发现________消失,并产生_________,化学方程式表示可用_____________________________、_______________________。
6HCl + Fe2O3=2FeCl3 +3H2O
2HCl + Fe=FeCl2+H2↑














