







高中化学人教版 (2019)选择性必修1整理与复习图文课件ppt
展开
这是一份高中化学人教版 (2019)选择性必修1整理与复习图文课件ppt,文件包含人教A版选择性必修第一册高二化学同步精品课件讲义第17讲溶液的酸碱性与pH的计算PPT课件pptx、人教A版选择性必修第一册高二化学同步讲义第17讲溶液的酸碱性与pH的计算学生版+教师版docx等2份课件配套教学资源,其中PPT共33页, 欢迎下载使用。
水煮沸后,竟然变成酸性了??
一、溶液的酸碱性与c(H+)、c(OH-)的关系溶液的酸碱性取决于c(H+)和c(OH-)的相对大小
"pH值”由丹麦化学家彼得·索伦森在1909年提出的。索伦森当时在一家啤酒厂工作,经常要化验啤酒中所含的氢离子浓度。每次化验结果都要记载许多个零,这使他感到很麻烦。经过长期潜心研究,他发现用氢离子浓度的负对数来表示氢离子浓度非常方便,并把它称为溶液的pH值。就这样"pH值”成为表述溶液酸碱度的一种重要数据。
二、pH与c(H+)的关系溶液的pH是c(H+)的负对数,即 pH =_____________。1. pH 越大,溶液的碱性越强;pH越小,溶液的酸性越强。2. 常温下,pH<7,为酸性溶液;pH=7,为中性溶液;pH>7,为碱性溶液。
c(H+)=0.1 ml/L, pH=-lg0.1=1
c(H+)=0.001 ml/L, pH=-lg0.001=3
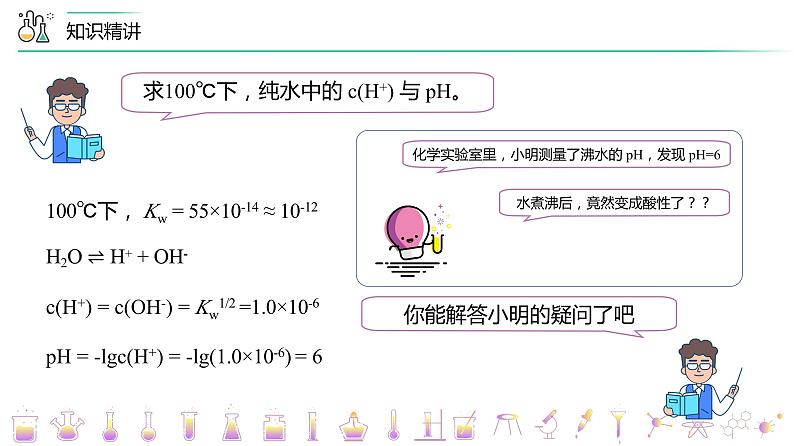
100℃下, Kw = 55×10-14 ≈ 10-12
c(H+) = c(OH-) = Kw1/2 =1.0×10-6
pH = -lgc(H+) = -lg(1.0×10-6) = 6
如100℃下,pH=6为中性,pH6显碱性,故使用pH时需注明温度。
三、pH的测定1.pH试纸(1)使用方法取一小块pH试纸于干燥洁净的玻璃片或表面皿上,用干燥洁净的玻璃棒蘸取试液点在试纸上,当试纸颜色变化稳定后迅速与标准比色卡对照,读出pH。(2)分类① 广泛pH试纸:其pH范围是 1~14 (最常用),可以识别的pH差约为1。② 精密pH试纸:可判别0.2或0.3的pH差值。③ 专用pH试纸:用于酸性、中性或碱性溶液的专用pH试纸。
三、pH的测定2.pH计pH计,又叫酸度计,可精密测量溶液的pH,其量程为0~14。
四、pH的计算2.混合溶液pH的计算(1)强酸混合,先求 ,再计算pH = -lgc(H+)
四、pH的计算2.混合溶液pH的计算(2)强碱混合,先求 ,再求c(H+) ,最后计算pH = -lgc(H+)
3.酸、碱稀释时 pH 变化规律(1)pH = a 的强酸溶液,稀释10m 倍,pH = a + m(室温下,a+ m<7)pH = a 的弱酸溶液,稀释10m 倍,a<pH<a + n(室温下,a+ m<7)(2)pH = b 的强碱溶液,稀释10n 倍,pH = b - n(室温下,b - n>7)pH = b 的弱酸溶液,稀释10n 倍,b - n<pH<b(室温下,b - n>7)
3.酸、碱稀释时 pH 变化规律(3)pH = a 的强酸溶液,稀释一倍(或与可忽略的酸/碱等体积混合), pH = a + 0.3(室温下,a+0.3<7)(4)pH = b 的强碱溶液,稀释一倍(或与可忽略的酸/碱等体积混合), pH = b - 0.3(室温下,b - 0.3>7)
(1)如果c(H+)≠c(OH-),则溶液一定呈一定的酸碱性________;(2)任何水溶液中都有c(H+)和c(OH-)________;(3)c(H+)等于10-6 ml·L-1的溶液一定呈现酸性________;(4)25 ℃时,纯水和烧碱溶液中水的离子积常数不相等________;(5)在100 ℃时,纯水的pH>7________;(6)如果c(H+)/ c(OH-)的值越大,则酸性越强 ________;
正确 正确 错误 错误 错误 正确
(7)升高温度,水的电离程度增大,酸性增强 ________;(8)25 ℃时,0.01 ml·L-1的KOH溶液的pH=12________;(9)pH减小,溶液的酸性一定增强________;(10)100 ℃时,0.01 ml·L-1盐酸的pH=2,0.01 ml·L-1的NaOH溶液的pH=10_____;(11)1.0×10-3 ml·L-1盐酸的pH=3,1.0×10-8 ml·L-1盐酸的pH=8 ______;(12)pH=a的醋酸溶液稀释一倍后,溶液的pH=b,则a>b________。
错误 正确 错误 正确 错误 错误
【变1-1】下列溶液一定呈酸性的是A.含有H+离子的溶液B.c(H+)>(Kw)1/2C.pH小于7的溶液D.使石蕊试液显紫色的溶液
题型一:溶液酸碱性的判断
【例2】pOH也可以表示溶液的酸碱度,已知pOH=-lgc(OH-),常温下,0.1 ml·L-1的下列溶液中pOH最大的是A.HClB.NaOHC.CH3COOHD.NH3·H2O
题型二:pH的类似物理量
【例3】90 ℃时,水的离子积Kw=3.8×10-13,则此温度时纯水的pH是A.等于7B.大于7C.小于7D.等于8
题型三:单一溶液pH的相关计算
【例5】常温下,将pH=12的NaOH溶液Va L与pH=1的稀盐酸Vb L混合,所得溶液呈中性,则Va ∶Vb 为A.1 : 1B.1 : 10C.10 : 1D.1 : 100
题型四:混合溶液pH的相关计算
【变6-3】常温下,pH=10的X、Y两种碱溶液各1mL,分别加水稀释到100mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是A.稀释前,两种碱溶液中溶质的物质的量浓度一定相等B.稀释后,X溶液的碱性比Y溶液的碱性强C.完全中和X、Y溶液时,消耗同浓度盐酸的体积:VX>VYD.若8
相关课件
这是一份人教版 (2019)第四节 化学反应的调控图文ppt课件,文件包含人教A版选择性必修第一册高二化学同步精品课件讲义第12讲化学反应的调控PPT课件pptx、人教A版选择性必修第一册高二化学同步讲义第12讲化学反应的调控学生版+教师版docx等2份课件配套教学资源,其中PPT共22页, 欢迎下载使用。
这是一份人教版 (2019)选择性必修1第二章 化学反应速率与化学平衡第三节 化学反应的方向教课课件ppt,文件包含人教A版选择性必修第一册高二化学同步精品课件讲义第11讲化学反应的方向PPT课件pptx、人教A版选择性必修第一册高二化学同步讲义第11讲化学反应的方向学生版+教师版docx等2份课件配套教学资源,其中PPT共23页, 欢迎下载使用。
这是一份高中化学人教版 (2019)选择性必修1第二节 化学平衡背景图课件ppt,文件包含人教A版选择性必修第一册高二化学同步精品课件讲义第09讲化学平衡常数PPT课件pptx、人教A版选择性必修第一册高二化学同步讲义第09讲化学平衡常数学生版+教师版docx等2份课件配套教学资源,其中PPT共24页, 欢迎下载使用。









