初中化学知识点笔记整理归纳
展开2、常用于炼铁的铁矿石有三种:
(1)赤铁矿(主要成分为Fe2O3);
(2)磁铁矿(Fe3O4);
(3)菱铁矿(FeCO3)。
3、炼钢的主要设备有三种:转炉、电炉、平炉。
4、常与温度有关的三个反应条件是:点燃、加热、高温。
5、不饱和溶液变饱和溶液有三种方法:降温、加溶质、恒温蒸发溶剂; 饱和溶液变不饱和溶液有两种方法:
(1)升温。
(2)加溶剂; (注意:溶解度随温度而变小的物质如:氢氧化钙溶液由饱和溶液变不饱和溶液:降温、加溶剂;不饱和溶液变饱和溶液有三种方法:升温、加溶质、恒温蒸发溶剂)。
6、收集气体一般有三种方法:排水法、向上排空法、向下排空法。
7、水污染的三个主要原因:
(1)工业生产中的废渣、废气、废水;
(2)生活污水的任意排放;
(3)农业生产中施用的农药、化肥随雨水流入河中。
8、通常使用的灭火器有三种:泡沫灭火器;干粉灭火器;液态二氧化碳灭火器。
9、固体物质的溶解度随温度变化的情况可分为三类:
(1)大部分固体物质溶解度随温度的升高而增大;
(2)少数物质溶解度受温度的影响很小;
(3)极少数物质溶解度随温度的升高而减小。
10、CO2可以灭火的原因有三个:不能燃烧、不能支持燃烧、密度比空气大。
11、单质可分为三类:金属单质;非金属单质;稀有气体单质。
12、当今世界上最重要的三大矿物燃料是:煤、石油、天然气。
13、应记住的三种黑色氧化物是:氧化铜、二氧化锰、四氧化三铁。
14、氢气和碳单质有三个相似的化学性质:常温下的稳定性、可燃性、还原性。
15、教材中出现的三次淡蓝色:
(1)液态氧气是淡蓝色;
(2)硫在空气中燃烧有微弱的淡蓝色火焰;
(3)氢气 在空气中燃烧有淡蓝色火焰。
16、与铜元素有关的三种蓝色:
(1)硫酸铜晶体;
(2)氢氧化铜沉淀;
(3)硫酸铜溶液。
17、过滤操作中有“三靠”:
(1)漏斗下端紧靠烧杯内壁;
(2)玻璃棒的末端轻靠在滤纸三层处;
(3)盛待过滤液的烧杯边缘紧靠在玻璃捧引流。
18、三大气体污染物:SO2、CO、NO2。
19、酒精灯的火焰分为三部分:外焰、内焰、焰心,其中外焰温度最高。
20、取用药品有“三不”原则:
(1)不用手接触药品;
(2)不把鼻子凑到容器口闻气体的气味;
(3)不尝药品的味道。
第二部分
1、木炭在氧气中燃烧:C+O2点燃CO2
2、硫在氧气中燃烧:S+O2点燃SO2
3、镁在空气中燃烧:2Mg+O2点燃2MgO
4、铁在氧气中燃烧:3Fe+2O2点燃Fe3O4
5、磷在氧气中燃烧:4P+5O2点燃2P2O5
6、铜在空气中加热:2Cu+O2加热2CuO
7、氢气在氧气中燃烧:2H2+O2点燃2H2O
8、一氧化碳在空气中燃烧:2CO+O2点燃2CO2
9、碳不充分燃烧:2C+O2(不充分)点燃2CO
10、二氧化碳通过灼热的碳层:CO2+C高温2CO
11、二氧化碳与水反应:CO2+H2O=H2CO3
12、生石灰和水化合:CaO+H2O=Ca(OH)2
13、氯酸钾与二氧化锰共热(实验室制O2):
14、加热高锰酸钾:
2KMnO4加热K2MnO4+MnO2+O2↑
15、电解水:2H2O通电2H2↑+O2↑
16、碳酸不稳定分解:H2CO3=H2O+CO2↑
17、高温煅烧石灰石:CaCO3高温CaO+CO2↑
18、锌和稀硫酸反应(实验室制H2):
Zn+H2SO4=ZnSO4+H2↑
19、锌和盐酸的反应:Zn+2HCl=ZnCl2+H2↑
20、铁和盐酸:Fe+2HCl=FeCl2+H2↑
第三部分
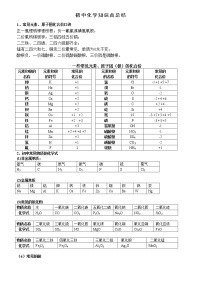
1、 常见物质的颜色:多数气体为无色,多数固体化合物为白色,多数溶液为无色。
2、 一些特殊物质的颜色:
黑色:MnO2、CuO、Fe3O4、C、FeS(硫化亚铁)
蓝色:CuSO4·5H2O、Cu(OH)2、CuCO3、含Cu2+溶液、
液态固态O2(淡蓝色)
红色:Cu(亮红色)、Fe2O3(红棕色)、红磷(暗红色)
黄色:硫磺(单质S)、含Fe3+的溶液(棕黄色)
绿色:FeSO4·7H2O、含Fe2+ 的溶液(浅绿色)、碱式碳酸铜[Cu2(OH)2CO3]
无色气体:N2、CO2、CO、O2、H2、CH4
有色气体:Cl2(黄绿色)、NO2(红棕色)
有刺激性气味的气体:NH3(此气体可使湿润pH试纸变蓝色)、SO2
有臭鸡蛋气味:H2S
3、 常见一些变化的判断:
① 白色沉淀且不溶于稀硝酸或酸的物质有:BaSO4、AgCl(就这两种物质)
② 蓝色沉淀:Cu(OH)2、CuCO3
③ 红褐色沉淀:Fe(OH)3
Fe(OH)2为白色絮状沉淀,但在空气中很快变成灰绿色沉淀,再变成Fe(OH)3红褐色沉淀
④沉淀能溶于酸并且有气体(CO2)放出的:不溶的碳酸盐
⑤沉淀能溶于酸但没气体放出的:不溶的碱
4、 酸和对应的酸性氧化物的联系:
① 酸性氧化物和酸都可跟碱反应生成盐和水:
CO2+ 2NaOH == Na2CO3+ H2O
(H2CO3+ 2NaOH == Na2CO3+ 2H2O)
SO2+ 2KOH == K2SO3+ H2O
H2SO3+ 2KOH == K2SO3+ 2H2O
SO3+ 2NaOH == Na2SO4+ H2O
H2SO4+ 2NaOH == Na2SO4+ 2H2O
② 酸性氧化物跟水反应生成对应的酸:(各元素的化合价不变)
CO2+ H20 == H2CO3
SO2+ H2O == H2SO3
SO3+ H2O == H2SO4
N2O5+ H2O == 2HNO3
(说明这些酸性氧化物气体都能使湿润pH试纸变红色)
5、 碱和对应的碱性氧化物的联系:
① 碱性氧化物和碱都可跟酸反应生成盐和水:
CuO + 2HCl == CuCl2+ H2O
Cu(OH)2+ 2HCl == CuCl2+ 2H2O
CaO + 2HCl == CaCl2+ H2O
Ca(OH)2 + 2HCl == CaCl2+ 2H2O
②碱性氧化物跟水反应生成对应的碱:(生成的碱一定是可溶于水,否则不能发生此反应)
K2O + H2O == 2KOH
Na2O +H2O == 2NaOH
BaO + H2O == Ba(OH)2
CaO + H2O == Ca(OH)2
③不溶性碱加热会分解出对应的氧化物和水:
Mg(OH)2== MgO + H2O
Cu(OH)2== CuO + H2O
2Fe(OH)3== Fe2O3 + 3H2O
2Al(OH)3 == Al2O3+ 3H2O
6、实验用到的气体要求是比较纯净,除去常见杂质具体方法:
① 除水蒸气可用:浓流酸、CaCl2固体、碱石灰、无水CuSO4(并且可以检验杂质中有无水蒸气,有则颜色由白色→蓝色)、生石灰等
② 除CO2可用:澄清石灰水(可检验出杂质中有无CO2)、NaOH溶液、
KOH溶液、碱石灰等
③ 除HCl气体可用:AgNO3溶液(可检验出杂质中有无HCl)、石灰水、NaOH溶液、KOH溶液
除气体杂质的原则:用某物质吸收杂质或跟杂质反应,但不能吸收或跟有效成份反应,或者生成新的杂质。
7、实验注意的地方:
①防爆炸:点燃可燃性气体(如H2、CO、CH4)或用CO、H2还原CuO、Fe2O3之前,要检验气体纯度。
②防暴沸:稀释浓硫酸时,将浓硫酸倒入水中,不能把水倒入浓硫酸中。
③防中毒:进行有关有毒气体(如:CO、SO2、NO2)的性质实验时,在通风厨中进行;并要注意尾气的处理:CO点燃烧掉;
SO2、NO2用碱液吸收。
④防倒吸:加热法制取并用排水法收集气体,要注意熄灯顺序。
8、常见意外事故的处理:
①酸流到桌上,用NaHCO3冲洗;碱流到桌上,用稀醋酸冲洗。
② 沾到皮肤或衣物上:
Ⅰ、酸先用水冲洗,再用3-5% NaHCO3冲洗;
Ⅱ、碱用水冲洗,再涂上硼酸;
Ⅲ、浓硫酸应先用抹布擦去,再做第Ⅰ步。
9、实验室制取三大气体中常见的要除的杂质:
①制O2要除的杂质:水蒸气(H2O)
②用盐酸和锌粒制H2要除的杂质:水蒸气(H2O)、氯化氢气体(HCl,盐酸酸雾)(用稀硫酸没此杂质)
③制CO2要除的杂质:水蒸气(H2O)、氯化氢气体(HCl)
除水蒸气的试剂:浓流酸、CaCl2固体、碱石灰(主要成份是NaOH和CaO)、生石灰、无水CuSO4(并且可以检验杂质中有无水蒸气,有则颜色由白色→蓝色)等
除HCl气体的试剂:AgNO3溶液(并可检验出杂质中有无HCl)、澄清石灰水、NaOH溶液(或固体)、KOH溶液(或固体)
[生石灰、碱石灰也可以跟HCl气体反应]
10、有CO的验证方法:(先验证混合气体中是否有CO2,有则先除掉)
将混合气体通入灼热的CuO,再将经过灼热的CuO的混合气体通入澄清石灰水。现象:黑色CuO变成红色,且澄清石灰水要变浑浊。
2024初中化学知识点归纳汇总: 这是一份2024初中化学知识点归纳汇总,共48页。学案主要包含了基本概念,基本知识,常见物质的颜色的状态,物质的溶解性,化学之最,初中化学中的“三”等内容,欢迎下载使用。
初中化学典型实验知识点笔记整理归纳: 这是一份初中化学典型实验知识点笔记整理归纳,共6页。
初中化学知识点整理归纳学案: 这是一份初中化学知识点整理归纳学案,共5页。