

北京市昌平区2023-2024学年高一上学期期末考试化学试题(含答案)
展开可能用到的相对原子质量:H 1 C 12 O 16 Na 23 S 32 Fe 56
1.近年来我国科学家在诸多科技领域取得新突破,下列成果所涉及的材料为金属材料的是
A.可应用于电化学能量储存和转换的新型全碳材料——石墨炔
B.单孔腔镜手术机器人蛇形手术臂使用的形状记忆合金——镍钛合金
C.大型客机C919的发动机涡轮部件——陶瓷基复合材料
D.“长征五号”运载火箭使用的高效燃料——液氢
2.当光束通过下列物质时,会出现丁达尔效应的是
A.胶体B.NaOH溶液C.蔗糖溶液D.溶液
3.下列气体难溶于水的是
A.B.C.NOD.
4.常温下,下列物质中易溶于水的是
A.AgClB.C.NaClD.
5.下列气体为红棕色的是
A.NOB.C.D.
6.下列有关物质分类的叙述中,正确的是
A.属于酸B.属于碱
C.属于酸性氧化物D.属于碱性氧化物
7.下列关于的说法中,不正确的是
A.无色无味气体B.易液化
C.可用作制氮肥D.可以与HCl反应
8.下列关于钠与水反应的说法中,不正确的是
A.钠浮在水面上说明金属钠的密度小于水
B.钠熔化成小球说明金属钠的熔点低且该反应放热
C.将酚酞滴入反应后的溶液,溶液变红说明有碱性物质产生
D.从化合价角度推测反应中产生的气体可能是氧气
9.下列物质不导电的是
A.Na单质B.NaCl固体C.熔融NaClD.NaCl溶液
10.下列反应不属于氧化还原反应的是
A.
B.
C.
D.
11.下列变化需要加入还原剂才能实现的是
A.B.
C.D.
12.下列变化与氧化还原反应无关的是
A.切开金属钠表面失去金属光泽
B.氯气使湿润的红纸条褪色
C.向硫酸亚铁溶液中滴加氢氧化钠溶液出现白色沉淀
D.氢氧化亚铁在空气中迅速变成灰绿色,最后变为红褐色
13.下列说法不正确的是
A.Fe的摩尔质量是56g/ml
B.常温常压下,的物质的量为1ml
C.中含有的分子数约为
D.溶液中含有
14.下列离子方程式不正确的是
A.石灰石与稀盐酸反应制二氧化碳:
B.稀盐酸除去铁制品表面的铁锈:
C.硝酸银溶液与盐酸生成白色沉淀:
D.铜粉与浓硝酸生成红棕色气体:
15.与水的反应为,下列说法不正确的是
A.是淡黄色固体
B.可做供氧剂
C.该反应中既不是氧化剂也不是还原剂
D.该反应中每生成转移
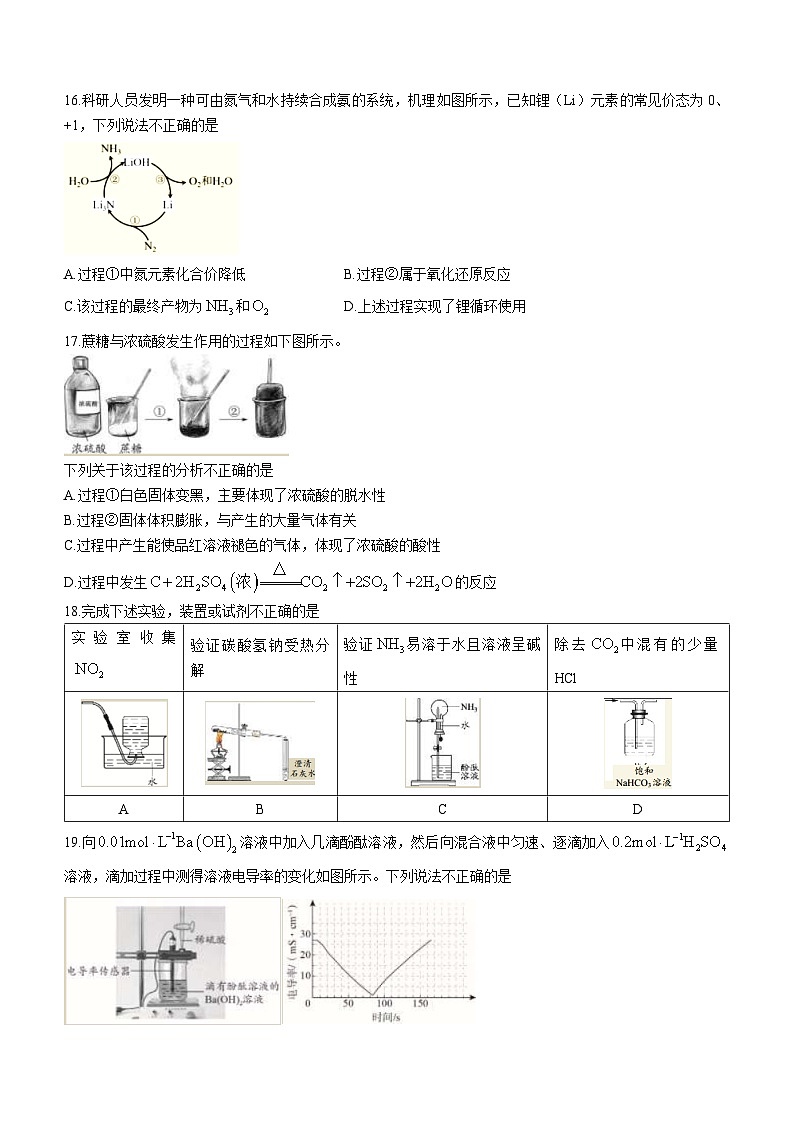
16.科研人员发明一种可由氮气和水持续合成氨的系统,机理如图所示,已知锂(Li)元素的常见价态为0、+1,下列说法不正确的是
A.过程①中氮元素化合价降低B.过程②属于氧化还原反应
C.该过程的最终产物为和D.上述过程实现了锂循环使用
17.蔗糖与浓硫酸发生作用的过程如下图所示。
下列关于该过程的分析不正确的是
A.过程①白色固体变黑,主要体现了浓硫酸的脱水性
B.过程②固体体积膨胀,与产生的大量气体有关
C.过程中产生能使品红溶液褪色的气体,体现了浓硫酸的酸性
D.过程中发生的反应
18.完成下述实验,装置或试剂不正确的是
19.向溶液中加入几滴酚酞溶液,然后向混合液中匀速、逐滴加入溶液,滴加过程中测得溶液电导率的变化如图所示。下列说法不正确的是
A.烧杯中红色逐渐变浅直至完全褪去
B.电导率减小的过程中,发生反应:
C.电导率增大的过程中,主要是
D.用同浓度的溶液代替稀硫酸重复上述实验,电导率变化图与原实验图相同
20.为除去粗盐水中含有的杂质、和,得到精制食盐,设计了如下实验流程
下列说法不正确的是
A.NaOH溶液的作用是除去
B.步骤i、ii的顺序可以互换
C.滤液2中有四种离子:、、、
D.步骤iv中发生的离子反应为:、
21.新型绿色水处理剂高铁酸钾()的制备方法如下图所示(部分步骤已略去)。
下列说法不正确的是
A.中Fe元素价态为+6价
B.过程I中发生
C.由过程II可知,在碱性溶液中的溶解度:
D.可将氨氮废水中的转化为除去,过程中被还原
第II部分(非选择题 共58分)
22.(4分)实验室有以下三种溶液:① ② ③HCl,将部分溶液两两混合,进行以下实验:
(1)将表格补充完整。a.__________________;b.__________________。
(2)除酸、碱外,②试剂还可能与______类(物质类别)反应,任选其中一种物质写出对应反应的离子方程式__________________。
23.(7分)自然界的氮循环如下图所示:
回答下列问题:
(1)大气固氮过程中氮元素被______(填“氧化”或“还原”)。
(2)工业固氮过程中的工业合成氨化学方程式为__________________。
(3)工业固氮过程中由NO转化为过程中还需要添加的物质是______。
(4)生物固氮过程中铵盐可通过硝化细菌转化为硝酸盐,生成时转移______ml电子。
24.(11分)实验室利用下面的装置(夹持装置已略去)探究不同价态硫元素之间的转化:
(1)装置A实现+6价S向+4价S转化,反应的化学方程式为__________________。
(2)装置B实现+4价S向+6价S转化,可选用的试剂有______。
A.溶液B.酸性溶液C.氯水D.KI溶液
(3)设计实验补充证明装置B中硫元素价态确实发生了转化,实验方案及现象为:取少量反应后的B中溶液于试管中,__________________。
(4)装置C中试剂为溶液,有淡黄色沉淀产生,反应的化学方程式为__________________,体现了______(填“氧化”或“还原”)性。
(5)D装置吸收少量后可通过加入CaO使NaOH溶液再生,则再生的化学方程式为__________________。
25.(14分)硫酸渣是硫酸生产过程中产生的固体废料,主要化学成分有、FeO、等。
I.研究人员可利用硫酸渣制备高纯度硫酸亚铁晶体,流程如下图所示:
已知:是难溶于水的酸性氧化物。
(1)操作1是______。
(2)步骤ii中涉及反应的离子方程式有__________________、__________________。
(3)步骤iii中的的作用是________________________。
(4)取少量高纯度晶体配成溶液,__________________(操作和现象),证明该晶体中不含。
II.研究人员还可利用硫酸渣与含氯废气(和HCl混合气)来制备絮凝剂聚合氯化铁,流程如下图所示:
已知:聚合氯化铁的一种形式为。
(5)在括号中写出以下几种物质中加点元素的化合价。
( )( )
··
(6)下列关于步骤iv中含氯废气作用的说法中,不正确的是______。
a.盐酸中作用是使FeO、溶解
b.氯气参与反应的离子方程式为
c.盐酸与氯气中的氯元素均转移到中
(7)补全步骤v中涉及到反应的化学方程式
26.(15分)研究小组制备次氯酸钠(NaClO)、探究其性质并测定其物质的量浓度。
I.制备NaClO
实验装置如下图:
(1)A为氯气发生装置,反应为,氧化剂与还原剂物质的量之比为______。
(2)B中饱和NaCl溶液的作用是________________________。
(3)C为NaClO制备装置,反应的离子方程式为__________________。
II.探究NaClO的性质
(4)从物质类别看,NaClO属于______,可能与某些酸反应。小组同学将红色纸条浸入NaClO溶液后,纸条褪色,向溶液中通入后,褪色更加明显,说明NaClO与和生成______(写化学式)。
(5)NaClO具有氧化性,预测依据是________________________。小组同学向NaClO溶液中加入过量的KI溶液,加入适量稀硫酸,加入淀粉,溶液变蓝,无黄绿色气体产生。该反应的离子方程式为__________________。
III.测定NaClO溶液的物质的量浓度
步骤i:配制(摩尔质量为158g/ml)标准溶液。
(6)计算需要固体的质量是______g。
(7)用到的仪器有:天平、药匙、量筒、烧杯、玻璃棒、胶头滴管和______。
(8)下列情况中,会使所配溶液浓度偏小的是______(填字母)。
a.配制溶液所用的容器中有蒸馏水
b.转移时,未洗涤烧杯和玻璃棒
c.定容时,眼睛仰视刻度线
d.摇匀后发现凹液面最低处低于刻度线
步骤ii:用标准溶液通过实验测得250mLNaClO溶液与足量KI反应生成的物质的量为0.05ml。
(9)计算NaClO溶液的物质的量浓度______ml/L。
27.(7分)某小组探究铜粉与溶液(其中)反应可能的化学过程。
【预测】
(1)甲同学认为该体系只发生氧化Cu单质的反应,离子方程式为________________________。
(2)乙同学认为该体系只发生在酸性条件()下氧化Cu单质的反应,离子方程式为__________________。
丙同学认为该体系为、共同与Cu参与反应过程。
【验证】
【分析】
(3)丙同学分析上述三个实验现象认为参与反应,其实验证据是________________________。经实验测定浓度降低,证实参与反应过程。
(4)进一步寻找实验iii反应后溶液呈深棕色的原因,丙同学查阅资料得知呈棕色,会缓慢分解,推测深棕色产生的反应离子方程式为
□______□______+□______。
【结论】
Cu与溶液体系首先发生氧化Cu的过程,产生,然后氧化体系中的,的还原产物主要以形式存在。
参考答案
第一部分 选择题(共42分)
选择题(每小题2分,共42分)
第二部分 非选择题(共58分)
23.(4分)
(1)a. b.产生气体
(2)盐,(其他答案合理即可)
24.(7分)
(1)氧化
(2)
(3)和
(4)8
25.(11分)
(1)
(2)BC
(3)先向其中加入过量HCl,再加入溶液,产生白色沉淀
(4) 氧化
(5)
26.(14分)
(1)过滤
(2)、
(3)防止蒸馏过程中被空气中的氧气氧化为
(4)加入KSCN溶液,无现象
(5)+4 +3
(6)bc
(7)
26.(15分)
(1)1∶2
(2)除去氯气中的HCl
(3)
(4)盐 HClO
(5)NaClO中Cl元素化合价为+1价,可降低;
(6)3.95
(7)250mL容量瓶
(8)bc
(9)0.2
27.(7分)
(1)
(2)
(3)实验i与实验iii现象不同
(4)
实验室收集
验证碳酸氢钠受热分解
验证易溶于水且溶液呈碱性
除去中混有的少量HCl
A
B
C
D
序号
操作
现象
离子方程式
i
①+②
产生白色沉淀
a
ii
②+③
b
实验序号
操作
现象
i
向100mL0.6ml/L的溶液中加入3g铜粉,振荡静置
蓝色溶液
ii
向溶液中加入3g铜粉,在密闭容器中反应
无明显现象
iii
向100mL0.6ml/L的溶液()中加入3g铜粉,振荡静置
深棕色溶液
题号
1
2
3
4
5
6
7
8
9
10
答案
B
A
C
C
B
C
A
D
B
D
题号
11
12
13
14
15
16
17
18
19
20
答案
A
C
B
A
D
B
C
A
D
C
题号
21
答案
B
北京市昌平区第一中学+2023-2024学年高一上学期期末考试化学试题: 这是一份北京市昌平区第一中学+2023-2024学年高一上学期期末考试化学试题,共9页。
北京市昌平区2023-2024学年高二上学期期末考试化学试题: 这是一份北京市昌平区2023-2024学年高二上学期期末考试化学试题,共14页。试卷主要包含了00等内容,欢迎下载使用。
2023-2024学年北京市昌平区高三上学期期末考试化学试题及答案: 这是一份2023-2024学年北京市昌平区高三上学期期末考试化学试题及答案,文件包含1_昌平高三化学期末试题及答案20241docx、2024北京昌平高三上期末化学教师版pdf等2份试卷配套教学资源,其中试卷共21页, 欢迎下载使用。












