




还剩23页未读,
继续阅读
成套系列资料,整套一键下载
人教版化学九年级下册 第十单元《酸和碱》复习课件
展开
这是一份人教版化学九年级下册 第十单元《酸和碱》复习课件,共31页。
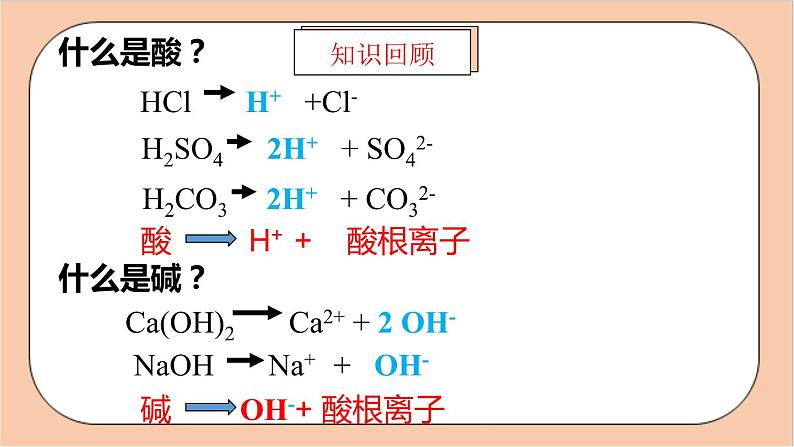
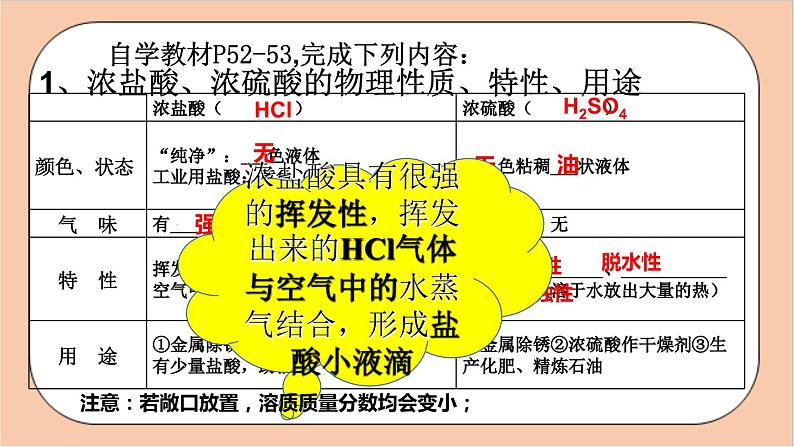
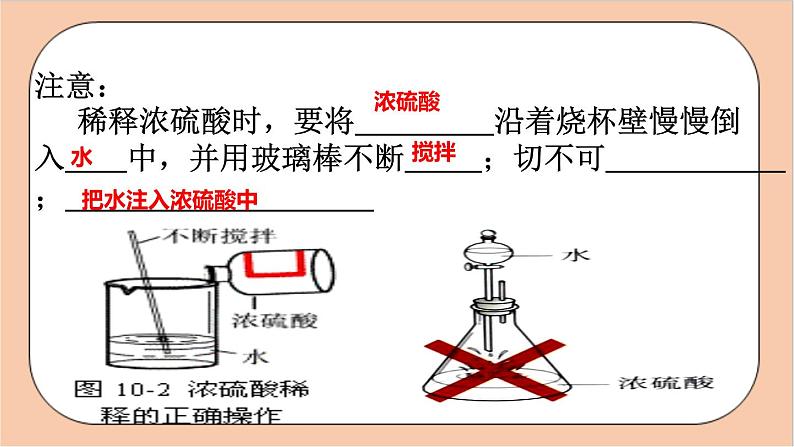
人教版化学九年级下册第十单元《酸和碱》复习1.掌握盐酸、硫酸的物理性质和化学性质2.掌握氢氧化钠、氢氧化钙的物理和化学性质3.掌握酸和碱的通性及有关化学方程式什么是酸?什么是碱? 1、浓盐酸、浓硫酸的物理性质、特性、用途 自学教材P52-53,完成下列内容:HCl无强烈刺激性氯化氢白雾H2SO4无油吸水性脱水性强腐蚀性浓盐酸具有很强的挥发性,挥发出来的HCl气体与空气中的水蒸气结合,形成盐酸小液滴注意:若敞口放置,溶质质量分数均会变小;注意: 稀释浓硫酸时,要将 沿着烧杯壁慢慢倒入 中,并用玻璃棒不断 ;切不可 ; 浓硫酸水搅拌把水注入浓硫酸中现有下列几种物质:Zn、CuO、CO2、NaOH、CaCO3、CuSO4 中能与HCl发生反应的有哪些?并归纳酸能与哪几类物质发生反应? 活泼金属 Zn金属氧化物 CuO碱 NaOH盐 CaCO32、酸的化学性质(具有通性的原因:酸解离时所生成的阳离子全部是 )(1)与酸碱指示剂的作用 酸能使石蕊试液变 色,使酚酞试液 ;(2)与活泼金属反应:规律: ; [条件:指排在H前面的活泼金属 反应类型 ]镁与稀盐酸反应: ;铁与稀硫酸反应: ,现象: ;自学教材P54,完成下列内容H+红不变色酸+活泼金属=盐+氢气置换反应Fe +H2SO4=FeSO4+H2↑Mg+2HCl=MgCl2+H2↑ 铁钉表面有气泡产生, 溶液由无色变为浅绿色(3)与金属氧化物反应:规律 ; [此反应常用于 ]Ø 氧化铜与稀硫酸反应: ;现象: ;氧化铁与稀硫酸反应: ;现象: ;思考:将生锈的铁钉放在足量的稀盐酸中,开始观察到的现象是 发生反应的方程式 ,过一段时间后又观察到 ,化学方程式是 。酸+金属氧化物=盐+水除铁锈CuO+H2SO4=CuSO4+H2O黑色固体逐渐消失,溶液由无色逐渐变成蓝色。Fe2O3+3H2SO4=Fe2(SO4)3+3H2O 铁锈逐渐消失,溶液由无色逐渐变成黄色Fe2O3+6HCl=2FeCl3+3H2OFe+2HCl=FeCl2+H2↑ 铁锈逐渐消失,溶液逐渐由无色变为黄色铁钉表面有气泡产生(4)与碱反应:规律 ;[这类反应叫 反应实质 ]Ø 氢氧化钠与稀盐酸反应: ; Ø 氢氧化钙与稀盐酸反应: ;思考:此反应若无明显现象,如何判断反应是否发生? 碳酸钙与稀盐酸的反应: ;氯化钡与硫酸反应: ;(5)与某些盐反应:酸+碱=盐+水中和反应H++OH-=H2ONaOH+HCl=NaCl+H2O Ca(OH)2+2HCl=CaCl2+2H2O用酸碱指示剂CaCO3+2HCl=CaCl2 + H2O + CO2↑BaCl2+H2SO4=BaSO4+2HCl 利用所学知识,我们可以如何证明溶液呈酸性?(H+)写出相应的物质,并尝试描述实验现象。1.取样品,滴加紫色石蕊试液,变红色,证明溶液呈酸性。2.用活泼金属,如锌,铁等;3.用金属氧化物,如氧化铁,氧化铜;4.用碳酸盐,如碳酸钠,碳酸钙等;5.用pH试纸测pH. “探险队员”—盐酸,不小心走进了化学迷宫(如图所示),迷宫中有许多“吃人的野兽”(即能与盐酸发生反应的质),盐酸必须避开它 ,请你帮助它走出迷宫(写序号)________ 二、碱(具有通性的原因:碱解离时所生成的阴离子全部是 )1、常见的碱:氢氧化钠、氢氧化钙的物理性质和用途 自学教材P55-56,完成下列内容:OH-NaOH火碱、烧碱、苛性钠白块易放出潮解Ca(OH)2消石灰、熟石灰白微CaO+H2O=Ca(OH)2 现有下列几种物质:Zn、CuO、CO2、H2SO4 、BaCl2、CuSO4 中能与NaOH发生反应的有哪些?并归纳出酸能与哪些物质发生反应?非金属氧化物CO2酸H2SO4盐CuSO42、碱的化学性质(1)与酸碱指示剂的作用 碱能使石蕊试液变 色,使酚酞试液变 色 ;思考:如何检验酸性、碱性、中性三种无色溶液?能否用酚酞溶液?若能怎么操作? 自学教材P56-58,完成下列内容:蓝红无色酚酞ABC装入C试管内液体是NaOH溶液装入A试管内的 液体是NaCl装入B试管内的液体是H2SO4NaOH HCl H2SO4(2)与非金属氧化物反应规律 : ; 氢氧化钠与二氧化碳反应: ,此反应常用于 CO2。因为氢氧化钠极易溶于水,吸收二氧化碳的能力更强;氢氧化钙与二氧化碳反应: ,此反应常用于 CO2。因为二氧化碳与澄清石灰水反应溶液变浑浊; 碱+非金属氧化物=盐+水 2NaOH + CO2 = Na2CO3 + H2O 吸收Ca(OH)2 + CO2 = CaCO3 ↓ + 2H2O 检验(3)与酸反应:规律 ; [这类反应叫 反应实质 ](4)与某些盐反应: 规律: ;条件:(1)生成物中有↑ 或↓或水 (2)反应物均可溶硫酸铜与氢氧化钠的反应: ;氢氧化钙与碳酸钠的反应: ;自学教材P56-58,完成下列内容:碱+盐=新碱+新盐中和反应H++OH-=H2O碱+酸=盐+水CuSO4 + 2NaOH = Cu(OH)2 ↓ + Na2SO4Ca(OH)2 + Na2CO3 = CaCO3 ↓ + 2NaOH三、溶液的酸碱性、酸碱度〖中和反应〗1.定义: ; 2.应用:⑴调节土壤的 ⑵处理工厂的 ; ⑶用于 ,氢氧化铝中和胃酸(化学方程式)__________________;2、溶液酸碱度的表示法—pH(1)pH<7时,溶液显 性,且pH值 ,溶液的酸性越强;pH=7时,溶液呈 性pH>7时,溶液显 性,且pH值 ,溶液的碱性越强; 自学教材P60-64,完成下列内容:酸和碱作用生成盐和水的反应 酸碱性 废水 医药Al(OH)3+3HCl=AlCl3+3H2O 酸 越小 中碱 越大(2)pH的测定:最简单的方法是使用_______。在白瓷板或玻璃片上放一小块 ,用 蘸取待测试液少许,滴在pH试纸上,把试纸显示的颜色与 比较,可测出被测液的pH。注意:①不得直接将pH试纸直接浸入待测液; ②不得先用水将pH试纸润湿;(3)酸雨:正常雨水的pH约为 (因为溶有CO2); 的雨水为酸雨; pH试纸 pH试纸 玻璃棒标准比色卡 5.6 pH<5.6如何鉴别实验室失去标签的稀盐酸和氢氧化钙两瓶无色溶液 ?如何鉴别实验室失去标签的稀盐酸和氢氧化钙两瓶无色溶液 ?分别取待检样品少量于试管中, 并分别通入二氧化碳气体 变浑浊的液体是氢氧化钙溶液,不变浑浊的液体是稀盐酸 分别放入锌粒于2个试管中, 并向其中分别加入少量待检样品 有气泡产生的液体稀盐酸,无气泡产生的液体是氢氧化钙溶液分别放入生锈的铁钉, 于试管中,并向其中加入少量待检样品铁锈消失,溶液变黄色的液体是稀盐酸, 铁锈不消失的液体是氢氧化钙溶液 分别取待检样品少量于试管中, 并滴入1-2滴酚酞试液 不变色的液体是稀盐酸, 变红色的液体是氢氧化钙溶液 分别用滴管滴一滴待检样品于pH试纸上,并与标准比色卡对照. PH<7的液体稀盐酸PH>7的的液体是氢氧化钙溶液 分别放入一粒石灰石于试管中,并向其中加入少量待检样品 有气泡产生的液体稀盐酸无气泡产生的液体是氢氧化钙溶液 紫色石蕊溶液也能鉴别吗?吸水性、脱水性、腐蚀性固体易潮解; 强腐蚀性H++酸根离子Ca(OH)2H2SO4HCl常用浓盐酸:挥发性、 腐蚀性与金属氧化物作用与酸作用与金属作用与碱作用性 质酸碱金属离子+OH-盐中和反应金属离子+酸根离子H++OH- =H2ONaOH常用与指示剂作用与指示剂作用与非金属氧化物作用 性质有腐蚀性 与盐作用1、用下列四种元素(O、H、Ca、S)写出符合要求的化学式:(1)酸________;碱________, 非金属氧化物 ,金属氧化物 。(2)写出上述酸与碱发生反应的化学方程式: ;2、下列物质长时间盛放在敞口容器里,质量会减少的是( ) A、浓硫酸 B、浓盐酸 C、石灰水 D、烧碱固体[来H2SO4Ca(OH)2SO2CaOH2SO4+Ca(OH)2=CaSO4+2H2OB3.下列气体中,既可以用浓硫酸干燥,又可用氢氧化钠固体干燥的是( ) A、CO2 B、NH3 C、H2 D、HCl4、实验室有两瓶失去标签的溶液,一瓶是稀盐酸,另一瓶是氢氧化钠溶液,下列试剂中不能将它们鉴别出来的是 ( ) A.酚酞试液 B.镁条 C.氯化钾溶液 D.氯化铜溶液CC5、在装有下列固体的烧杯中,加入过量的稀硫酸,能得到澄清无色溶液的是( )A、Cu(OH)2 B、Zn C、Fe2O3 D、BaCl2 6、将一包氢氧化铜、氧化铜和锌粒组成的混合物,投入过量的稀硫酸中充分反应后,发现有少量的不溶物,这种不溶物是 ,写出上述反应的化学方程 (1) ; (2) , (3) , (4) 。 BCuCu(OH)2+H2SO4=CuSO4+2H2OCuO+H2SO4=CuSO4+H2OZn+H2SO4=ZnSO4+H2Zn+CuSO4=ZnSO4+Cu7、下图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线。(1)氢氧化钠和盐酸恰好完全反应时,溶液pH 7 (填“>”或“<”或“=”)(2)根据曲线判断,该反应中向一定量的某物质中逐滴加入是 (填“氢氧化钠溶液”或“盐酸”),理由是 ;=氢氧化钠溶液开始溶液呈酸性,随着液体加入,溶液pH逐渐增大(3)当滴入溶液的体积为5mL时,所得溶液中的溶质为 (写化学式),若在此溶液中滴入石蕊试液,溶液显 色。 (4)右图是氢氧化钠与盐酸反应的微观示意图,请仔细观察、分析此图,写出一条你从图中获取的信息(用文字或化学用语表述) ; 中和反应的实质是氢离子与氢氧根离子反应生成水红Nacl、HCl课程结束
人教版化学九年级下册第十单元《酸和碱》复习1.掌握盐酸、硫酸的物理性质和化学性质2.掌握氢氧化钠、氢氧化钙的物理和化学性质3.掌握酸和碱的通性及有关化学方程式什么是酸?什么是碱? 1、浓盐酸、浓硫酸的物理性质、特性、用途 自学教材P52-53,完成下列内容:HCl无强烈刺激性氯化氢白雾H2SO4无油吸水性脱水性强腐蚀性浓盐酸具有很强的挥发性,挥发出来的HCl气体与空气中的水蒸气结合,形成盐酸小液滴注意:若敞口放置,溶质质量分数均会变小;注意: 稀释浓硫酸时,要将 沿着烧杯壁慢慢倒入 中,并用玻璃棒不断 ;切不可 ; 浓硫酸水搅拌把水注入浓硫酸中现有下列几种物质:Zn、CuO、CO2、NaOH、CaCO3、CuSO4 中能与HCl发生反应的有哪些?并归纳酸能与哪几类物质发生反应? 活泼金属 Zn金属氧化物 CuO碱 NaOH盐 CaCO32、酸的化学性质(具有通性的原因:酸解离时所生成的阳离子全部是 )(1)与酸碱指示剂的作用 酸能使石蕊试液变 色,使酚酞试液 ;(2)与活泼金属反应:规律: ; [条件:指排在H前面的活泼金属 反应类型 ]镁与稀盐酸反应: ;铁与稀硫酸反应: ,现象: ;自学教材P54,完成下列内容H+红不变色酸+活泼金属=盐+氢气置换反应Fe +H2SO4=FeSO4+H2↑Mg+2HCl=MgCl2+H2↑ 铁钉表面有气泡产生, 溶液由无色变为浅绿色(3)与金属氧化物反应:规律 ; [此反应常用于 ]Ø 氧化铜与稀硫酸反应: ;现象: ;氧化铁与稀硫酸反应: ;现象: ;思考:将生锈的铁钉放在足量的稀盐酸中,开始观察到的现象是 发生反应的方程式 ,过一段时间后又观察到 ,化学方程式是 。酸+金属氧化物=盐+水除铁锈CuO+H2SO4=CuSO4+H2O黑色固体逐渐消失,溶液由无色逐渐变成蓝色。Fe2O3+3H2SO4=Fe2(SO4)3+3H2O 铁锈逐渐消失,溶液由无色逐渐变成黄色Fe2O3+6HCl=2FeCl3+3H2OFe+2HCl=FeCl2+H2↑ 铁锈逐渐消失,溶液逐渐由无色变为黄色铁钉表面有气泡产生(4)与碱反应:规律 ;[这类反应叫 反应实质 ]Ø 氢氧化钠与稀盐酸反应: ; Ø 氢氧化钙与稀盐酸反应: ;思考:此反应若无明显现象,如何判断反应是否发生? 碳酸钙与稀盐酸的反应: ;氯化钡与硫酸反应: ;(5)与某些盐反应:酸+碱=盐+水中和反应H++OH-=H2ONaOH+HCl=NaCl+H2O Ca(OH)2+2HCl=CaCl2+2H2O用酸碱指示剂CaCO3+2HCl=CaCl2 + H2O + CO2↑BaCl2+H2SO4=BaSO4+2HCl 利用所学知识,我们可以如何证明溶液呈酸性?(H+)写出相应的物质,并尝试描述实验现象。1.取样品,滴加紫色石蕊试液,变红色,证明溶液呈酸性。2.用活泼金属,如锌,铁等;3.用金属氧化物,如氧化铁,氧化铜;4.用碳酸盐,如碳酸钠,碳酸钙等;5.用pH试纸测pH. “探险队员”—盐酸,不小心走进了化学迷宫(如图所示),迷宫中有许多“吃人的野兽”(即能与盐酸发生反应的质),盐酸必须避开它 ,请你帮助它走出迷宫(写序号)________ 二、碱(具有通性的原因:碱解离时所生成的阴离子全部是 )1、常见的碱:氢氧化钠、氢氧化钙的物理性质和用途 自学教材P55-56,完成下列内容:OH-NaOH火碱、烧碱、苛性钠白块易放出潮解Ca(OH)2消石灰、熟石灰白微CaO+H2O=Ca(OH)2 现有下列几种物质:Zn、CuO、CO2、H2SO4 、BaCl2、CuSO4 中能与NaOH发生反应的有哪些?并归纳出酸能与哪些物质发生反应?非金属氧化物CO2酸H2SO4盐CuSO42、碱的化学性质(1)与酸碱指示剂的作用 碱能使石蕊试液变 色,使酚酞试液变 色 ;思考:如何检验酸性、碱性、中性三种无色溶液?能否用酚酞溶液?若能怎么操作? 自学教材P56-58,完成下列内容:蓝红无色酚酞ABC装入C试管内液体是NaOH溶液装入A试管内的 液体是NaCl装入B试管内的液体是H2SO4NaOH HCl H2SO4(2)与非金属氧化物反应规律 : ; 氢氧化钠与二氧化碳反应: ,此反应常用于 CO2。因为氢氧化钠极易溶于水,吸收二氧化碳的能力更强;氢氧化钙与二氧化碳反应: ,此反应常用于 CO2。因为二氧化碳与澄清石灰水反应溶液变浑浊; 碱+非金属氧化物=盐+水 2NaOH + CO2 = Na2CO3 + H2O 吸收Ca(OH)2 + CO2 = CaCO3 ↓ + 2H2O 检验(3)与酸反应:规律 ; [这类反应叫 反应实质 ](4)与某些盐反应: 规律: ;条件:(1)生成物中有↑ 或↓或水 (2)反应物均可溶硫酸铜与氢氧化钠的反应: ;氢氧化钙与碳酸钠的反应: ;自学教材P56-58,完成下列内容:碱+盐=新碱+新盐中和反应H++OH-=H2O碱+酸=盐+水CuSO4 + 2NaOH = Cu(OH)2 ↓ + Na2SO4Ca(OH)2 + Na2CO3 = CaCO3 ↓ + 2NaOH三、溶液的酸碱性、酸碱度〖中和反应〗1.定义: ; 2.应用:⑴调节土壤的 ⑵处理工厂的 ; ⑶用于 ,氢氧化铝中和胃酸(化学方程式)__________________;2、溶液酸碱度的表示法—pH(1)pH<7时,溶液显 性,且pH值 ,溶液的酸性越强;pH=7时,溶液呈 性pH>7时,溶液显 性,且pH值 ,溶液的碱性越强; 自学教材P60-64,完成下列内容:酸和碱作用生成盐和水的反应 酸碱性 废水 医药Al(OH)3+3HCl=AlCl3+3H2O 酸 越小 中碱 越大(2)pH的测定:最简单的方法是使用_______。在白瓷板或玻璃片上放一小块 ,用 蘸取待测试液少许,滴在pH试纸上,把试纸显示的颜色与 比较,可测出被测液的pH。注意:①不得直接将pH试纸直接浸入待测液; ②不得先用水将pH试纸润湿;(3)酸雨:正常雨水的pH约为 (因为溶有CO2); 的雨水为酸雨; pH试纸 pH试纸 玻璃棒标准比色卡 5.6 pH<5.6如何鉴别实验室失去标签的稀盐酸和氢氧化钙两瓶无色溶液 ?如何鉴别实验室失去标签的稀盐酸和氢氧化钙两瓶无色溶液 ?分别取待检样品少量于试管中, 并分别通入二氧化碳气体 变浑浊的液体是氢氧化钙溶液,不变浑浊的液体是稀盐酸 分别放入锌粒于2个试管中, 并向其中分别加入少量待检样品 有气泡产生的液体稀盐酸,无气泡产生的液体是氢氧化钙溶液分别放入生锈的铁钉, 于试管中,并向其中加入少量待检样品铁锈消失,溶液变黄色的液体是稀盐酸, 铁锈不消失的液体是氢氧化钙溶液 分别取待检样品少量于试管中, 并滴入1-2滴酚酞试液 不变色的液体是稀盐酸, 变红色的液体是氢氧化钙溶液 分别用滴管滴一滴待检样品于pH试纸上,并与标准比色卡对照. PH<7的液体稀盐酸PH>7的的液体是氢氧化钙溶液 分别放入一粒石灰石于试管中,并向其中加入少量待检样品 有气泡产生的液体稀盐酸无气泡产生的液体是氢氧化钙溶液 紫色石蕊溶液也能鉴别吗?吸水性、脱水性、腐蚀性固体易潮解; 强腐蚀性H++酸根离子Ca(OH)2H2SO4HCl常用浓盐酸:挥发性、 腐蚀性与金属氧化物作用与酸作用与金属作用与碱作用性 质酸碱金属离子+OH-盐中和反应金属离子+酸根离子H++OH- =H2ONaOH常用与指示剂作用与指示剂作用与非金属氧化物作用 性质有腐蚀性 与盐作用1、用下列四种元素(O、H、Ca、S)写出符合要求的化学式:(1)酸________;碱________, 非金属氧化物 ,金属氧化物 。(2)写出上述酸与碱发生反应的化学方程式: ;2、下列物质长时间盛放在敞口容器里,质量会减少的是( ) A、浓硫酸 B、浓盐酸 C、石灰水 D、烧碱固体[来H2SO4Ca(OH)2SO2CaOH2SO4+Ca(OH)2=CaSO4+2H2OB3.下列气体中,既可以用浓硫酸干燥,又可用氢氧化钠固体干燥的是( ) A、CO2 B、NH3 C、H2 D、HCl4、实验室有两瓶失去标签的溶液,一瓶是稀盐酸,另一瓶是氢氧化钠溶液,下列试剂中不能将它们鉴别出来的是 ( ) A.酚酞试液 B.镁条 C.氯化钾溶液 D.氯化铜溶液CC5、在装有下列固体的烧杯中,加入过量的稀硫酸,能得到澄清无色溶液的是( )A、Cu(OH)2 B、Zn C、Fe2O3 D、BaCl2 6、将一包氢氧化铜、氧化铜和锌粒组成的混合物,投入过量的稀硫酸中充分反应后,发现有少量的不溶物,这种不溶物是 ,写出上述反应的化学方程 (1) ; (2) , (3) , (4) 。 BCuCu(OH)2+H2SO4=CuSO4+2H2OCuO+H2SO4=CuSO4+H2OZn+H2SO4=ZnSO4+H2Zn+CuSO4=ZnSO4+Cu7、下图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线。(1)氢氧化钠和盐酸恰好完全反应时,溶液pH 7 (填“>”或“<”或“=”)(2)根据曲线判断,该反应中向一定量的某物质中逐滴加入是 (填“氢氧化钠溶液”或“盐酸”),理由是 ;=氢氧化钠溶液开始溶液呈酸性,随着液体加入,溶液pH逐渐增大(3)当滴入溶液的体积为5mL时,所得溶液中的溶质为 (写化学式),若在此溶液中滴入石蕊试液,溶液显 色。 (4)右图是氢氧化钠与盐酸反应的微观示意图,请仔细观察、分析此图,写出一条你从图中获取的信息(用文字或化学用语表述) ; 中和反应的实质是氢离子与氢氧根离子反应生成水红Nacl、HCl课程结束
相关资料
更多










