

14, 山东省烟台市2023-2024学年高二上学期期末考试化学试题(1)
展开注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 B 11 C 12 N 14 K 39 Fe 56 Se 79
选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.下列说法错误的是
A.“雪花六出”体现了晶体的自范性
B.防撞气囊中的NaN3是一种含有共价键的离子化合物
C.钛镁合金的导电性和导热性是通过自由电子定向移动实现的
D.冠醚(18-冠-6)的空穴与K+尺寸适配,两者能通过弱相互作用形成超分子
2.下列化学用语错误的是
A.NH3的VSEPR模型:
B.Cr3+的结构示意图:
C.的名称:3-甲基-4-乙基己烷
D.用电子云轮廓图表示HCl中σ键的形成:
3.下列说法正确的是
A.元素周期表中,s区所含元素的种类最少
B.钠的焰色呈黄色的主要原因是电子跃迁时吸收了黄光以外的光
C.若基态原子的最外层有3个未成对电子,该原子一定属于主族元素
D.碳原子间能形成双键而硅原子间难以形成,是因为碳的得电子能力强于硅您看到的资料都源自我们平台,家威鑫 MXSJ663 低至0.3/份 4.利用反应CCl4+4Na4NaCl+C(金刚石)可实现人工合成金刚石。下列说法正确的是
A.反应过程中有离子键的断裂与形成
B.熔点:C (金刚石)> Na > NaCl > CCl4
C.NaCl晶体中,每个Cl–的周围距离其最近的Cl–有6个
D.金刚石晶胞中,若键长为a pm,则晶胞参数为a pm
5.噻唑()中所有原子在同一平面上,能与H2反应生成四氢噻唑()。下列说法错误的是
A.在水中的溶解度:噻唑>噻吩()
B.噻唑中S原子提供2个电子参与形成大π键
C.四氢噻唑的熔点主要取决于范德华力
D.C-S-C键角:噻唑>四氢噻唑
6.在HY沸石催化作用下,丙烯与萘反应可生成二异丙基萘M和N。下列说法正确的是
A.上述反应中,丙烯仅π键发生断裂
B.萘的二溴代物有13种
C.M中所有碳原子可能共平面
D.萘、M、N互为同系物
7.结构决定性质,下列性质差异与结构因素匹配错误的是
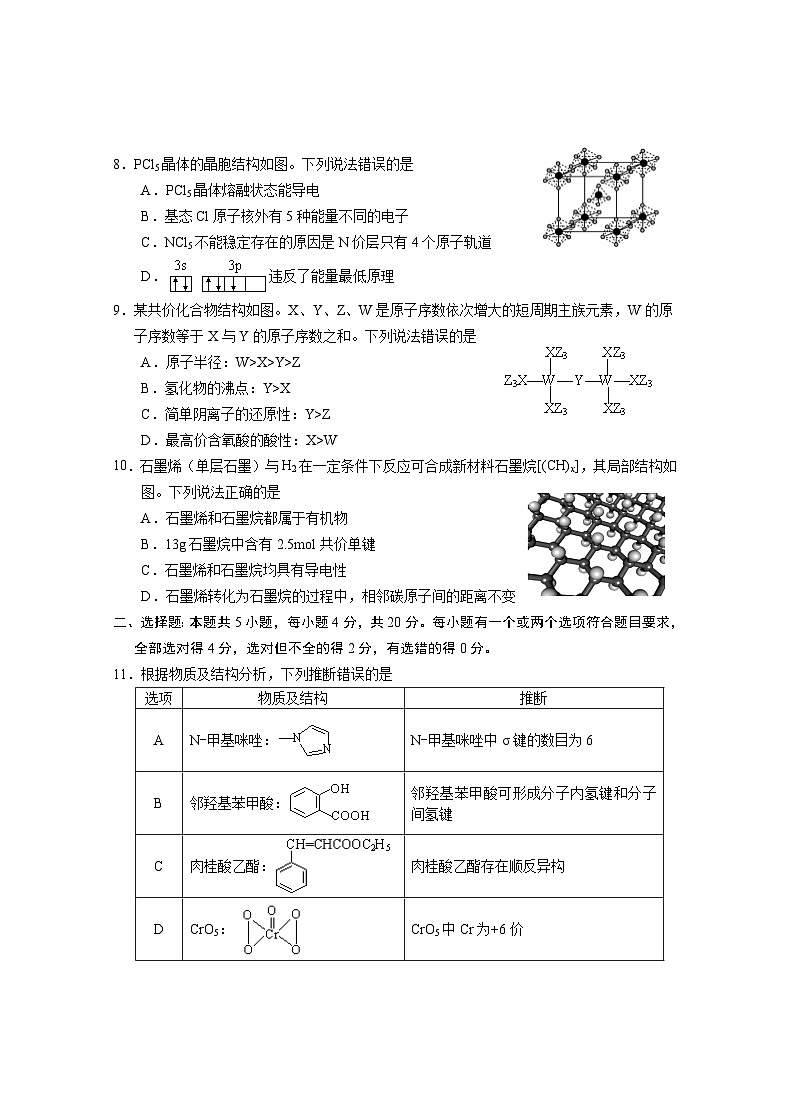
8.PCl5晶体的晶胞结构如图。下列说法错误的是
A.PCl5晶体熔融状态能导电
B.基态Cl原子核外有5种能量不同的电子
C.NCl5不能稳定存在的原因是N价层只有4个原子轨道
D.违反了能量最低原理
9.某共价化合物结构如图。X、Y、Z、W是原子序数依次增大的短周期主族元素,W的原子序数等于X与Y的原子序数之和。下列说法错误的是
A.原子半径:W>X>Y>Z
B.氢化物的沸点:Y>X
C.简单阴离子的还原性:Y>Z
D.最高价含氧酸的酸性:X>W
10.石墨烯(单层石墨)与H2在一定条件下反应可合成新材料石墨烷[(CH)x],其局部结构如图。下列说法正确的是
A.石墨烯和石墨烷都属于有机物
B.13g石墨烷中含有2.5ml共价单键
C.石墨烯和石墨烷均具有导电性
D.石墨烯转化为石墨烷的过程中,相邻碳原子间的距离不变
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得4分,选对但不全的得2分,有选错的得0分。
11.根据物质及结构分析,下列推断错误的是
12.三氟化氯(ClF3)是极强助燃剂,能自耦电离:2ClF3ClF2++ClF4–,其分子空间结构如图。下列推测合理的是
A.ClF3分子是含有极性键的非极性分子
B.BrF3比ClF3更易发生自耦电离
C.ClF3水解反应的产物为HCl和HFO
D.ClF2+与H2O、ClF4–与CCl4的空间结构分别相同
13. 某含Ru(Ⅱ)的催化剂(用[L-Ru-NH3]+表示)高效
电催化氧化NH3合成N2H4的反应机理如图。
下列说法错误的是
A.反应过程中没有非极性键的断裂
B.反应过程中所有氮的杂化方式相同
C.M与[L-Ru-NH2]+中Ru的化合价相同
D.Ru(Ⅱ)被氧化至Ru(Ⅲ)后,N-H键的极性减弱
14. 某锂电池的负极材料由锂原子嵌入石墨烯层间形成,其晶胞结构如图甲。下列说法错误的是
A. 该晶体的化学式为LiC6
B.1号、2号 Li之间的距离为
C.图乙可表示该化合物沿z轴的局部投影图
D.利用X射线衍射实验可测得晶胞参数α、β、γ
15. 某种新型储氢材料(摩尔质量为188 g∙ml–1)的立方晶胞如图,该晶胞可储存6个氢原子。已知M核内中子数比质子数多4,标准状况下氢气的密度为ρ g∙cm–3,NA表示阿伏加德罗常数的值。下列说法正确的是
A.晶胞中[M(NH3)6]n+和[BH4]–的配位数相同
B.M离子最外层电子排布式为3s23p63d6
C.在晶胞体对角线的一维空间上会出现的排布规律
D.该材料的储氢能力[]为
三、非选择题:本题共5小题,共60分。
16.(11分)有机物W的一种合成路线如下:
回答下列问题:
(1)X的分子式为______,分子中采用sp2与sp3杂化的原子个数之比为____。
(2)下列有关Y的说法错误的是____(填标号)。
a. 按碳骨架分类,Y属于脂环烃 b. 分子中含有2个手性碳原子
c. 五元环上的一氯代物有3种 d. 分子中的C-O键、O-H键在化学反应中易断裂
(3)Z中只含碳、氢、氧三种元素,其分子模型如图所示(图中小球表示原子,球与球之间的短线代表单键或双键)。Z中的极性键有_____种,所含官能团的名称为_____。
(4)有机物A属于醇类,其结构简式为___;写出符合下列条件的W的同分异构体___(填结构简式,不考虑立体异构)。
①含-COOH和-CHO; ②含五元碳环结构
17.(13分)W、X、Y、Z、R为原子序数依次增大的短周期主族元素。W的核外电子只有一种自旋方向;Y、Z、R在元素周期表中相邻,X的核外电子数与Y的价层电子数相等,R2是氧化性最强的单质。回答下列问题:
(1)由X原子核形成的三种微粒,电子排布式分别为:①1s22s2、②1s22s22p1、③1s22s12p2,有关这些微粒的叙述正确的是 (填标号)。
a.得电子能力:②>① b.表示基态原子(或离子)的是:①②
c.微粒半径:①>② d.电离一个电子所需最低能量:①>②>③
(2)YR3是一种重要的电子工业材料。分子的极性:YR3______XR3(填“>”或“<”或“=”);
YR3与YW3结构相似,YW3易与过渡金属阳离子形成配离子而YR3不能,原因是_____。
(3)同周期元素中,第一电离能比Z大的元素有 种;Z与Y形成的固态Y2Z5由YZ2+和YZ3–两种离子组成,固态Y2Z5中Y原子的杂化方式为 ,YZ2+的电子式为 。
(4)X与Z可形成多种结构形式的阴离子。已知阴离子X3Z6n–结构中只有一个正六元环,则n=____,该阴离子的结构式为_____。
18.(12分)由Sn、V、Gd等元素组成钒基笼目金属在超导电性方面有广阔的应用前景。回答下列问题:
(1)Sn与C同主族,基态Sn原子的价电子排布式为 ,Sn和Cl2反应会生成SnCl2和SnCl4。SnCl2(s)以线性聚合状态存在,其结构如图。
Cl-Sn-Cl键角:SnCl2(s) SnCl4(填“>”或“<”),原因是 。
(2)基态V原子的价电子中,未成对电子数与成对电子数之比为 ;钒有+2、+3、+4、+5等多种化合价,从原子结构角度分析最稳定的化合价是 ;将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,下列含V物质中,属于顺磁性物质的是 (填标号)。
A.VF4 B.V(NH3)3Cl3 C.Na3VO4 D.Na4[V(CN)6]
(3)已知钒基笼目金属的晶体结构如图。该钒基笼目金属的化学式为 ,1号、2号Sn原子间的距离为 pm。
19.(12分)Cu是生活中常见的金属元素,在材料、农业、医药等领域具有广泛应用。回答下列问题:
(1)Cu位于周期表的 区;从结构角度分析,比较Cu+与Cu2+的稳定性并说明原因 。
(2)某氨基吡啶衍生物铜配合物X的结构简式如下图所示。
X中Cu2+的配位数是 ,两种配体分别为 。
(3)CuFeS2晶体属四方晶系,晶胞棱边夹角均为90°。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。M点、N点原子的分数坐标分别为(0,0,0)、。下图中B所示结构单元不能作为CuFeS2晶胞的原因是 ,X点硫原子的分数坐标为 ,晶胞中四面体空隙的占有率为 ,晶胞中硫原子间的最短距离为 pm。
20.(12分)铁的化合物种类繁多,应用广泛。回答下列问题:
(1)某含Fe2+的结晶水合物的结构片段如图所示(球与球之间的短线代表单键或双键)。
该结晶水合物的化学式为 ,其中Fe2+和H2O之间的作用力类型为 。
(2)南开大学某课题组成功合成无机二茂铁的配离子[FeP8]2–,其中环状配体P42–以π电子参与配位,结构如图。该配离子中与Fe2+形成配位键的电子共有 个,P原子的价层孤电子对占据___(填标号)。
A.3s轨道 B.3p轨道 C.sp2杂化轨道 D.sp3杂化轨道
(3)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。由铁、钾、硒形成的一种超导材料的晶胞结构如下图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如下表所示。
晶胞中Fe的数目为 ,距离K(0.5,0.5,0.5)最近的Se的数目为 ,该晶体的密度ρ=___g·cm–3。(NA表示阿伏加德罗常数的值,用含a、c、NA的计算式表示),该晶胞在yz平面投影为 (填标号)。
选项
性质差异
结构因素
A
键能:F-F键
B
稳定性:H2O>H2S
半径:O<S
C
酸性:HClO3
D
沸点:正戊烷>新戊烷
分子间作用力
选项
物质及结构
推断
A
N-甲基咪唑:
N-甲基咪唑中σ键的数目为6
B
邻羟基苯甲酸:
邻羟基苯甲酸可形成分子内氢键和分子间氢键
C
肉桂酸乙酯:
肉桂酸乙酯存在顺反异构
D
CrO5:
CrO5中Cr为+6价
原子
坐标
x
y
z
K
0.5
0.5
0.5
Fe
0
0.5
m
Se
0
0
n
注:m、n均≠0
70, 山东省烟台市2023-2024学年高二上学期期末考试化学试题: 这是一份70, 山东省烟台市2023-2024学年高二上学期期末考试化学试题,共21页。试卷主要包含了 PCl5晶体的晶胞结构如图, 某共价化合物结构如图等内容,欢迎下载使用。
14, 山东省烟台市2023-2024学年高二上学期期末考试化学试题: 这是一份14, 山东省烟台市2023-2024学年高二上学期期末考试化学试题,共2页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
12,山东省烟台市2023-2024学年高三上学期期末考试化学试题(1): 这是一份12,山东省烟台市2023-2024学年高三上学期期末考试化学试题(1),共9页。试卷主要包含了50 mLNaOH溶液,6 ml·L–1,0~8等内容,欢迎下载使用。












