





还剩28页未读,
继续阅读
所属成套资源:鲁教版五四制化学八年级全一册 课件
成套系列资料,整套一键下载
鲁教版五四制化学八年级全一册 第二单元 第二单元探秘水世界复习 课件
展开
这是一份鲁教版五四制化学八年级全一册 第二单元 第二单元探秘水世界复习 课件,共36页。
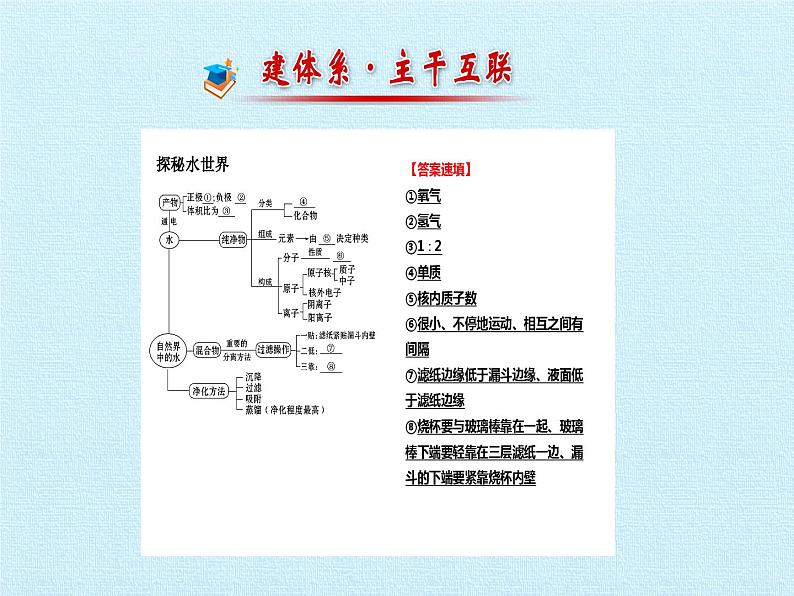
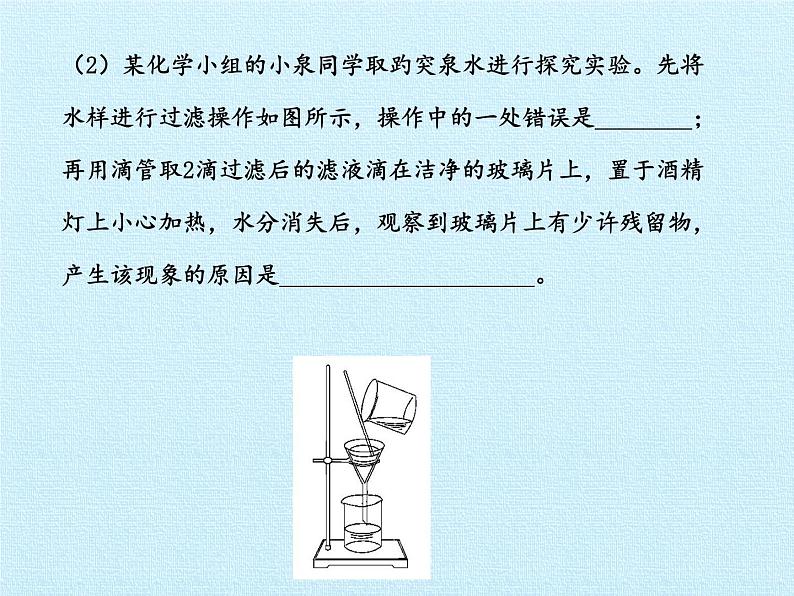
第二单元 探索水世界 复习课件主题一:水的净化与水的电解【主题训练1】(2013·乌鲁木齐中考)在电解水的实验中,可以直接观察到的现象是( )A.水由氢、氧两种元素组成。B.有氢气和氧气产生,且体积比为2∶1C.在电极上均有气泡产生,两个试管内气体的体积之比约为2∶1D.每个水分子是由两个氢原子和一个氧原子构成的。【解析】选C。水是由氢、氧两种元素组成的,有氢气和氧气产生是通过电解水的实验得出的实验结论;通电后,在电极上均有气泡产生,两个试管内气体的体积之比约为2∶1,此现象能直接观察到;每个水分子是由两个氢原子和一个氧原子构成的,是通过对电解水的实验综合分析得出的实验结论。故选C。【主题训练2】(2013·济南中考)泉水是“泉城”济南的文化之魂,首届济南泉水节于2013年8月28日开幕。节水环保、杜绝水污染、建设美丽泉城,是我们泉城人的职责。(1)自然界中,水的存在形式多姿多彩,水孕育了万物生灵,水通过三态变化实现天然循环,这个循环过程是由________提供的能量(填序号)。A.地球自转 B.太阳照射C.海洋潮汐 D.植物生长(2)某化学小组的小泉同学取趵突泉水进行探究实验。先将水样进行过滤操作如图所示,操作中的一处错误是________;再用滴管取2滴过滤后的滤液滴在洁净的玻璃片上,置于酒精灯上小心加热,水分消失后,观察到玻璃片上有少许残留物,产生该现象的原因是_____________________。【解析】水的三态变化是通过太阳能提供能量的;进行过滤操作时,漏斗的下端管口应紧靠烧杯内壁;由于滤液中含有一些可溶性杂质,故加热滤液,水分消失后,会观察到玻璃片上有少许固体残留物。答案:(1)B (2)漏斗的下端管口没有紧靠烧杯内壁,滤液中含有一些可溶性杂质。【关键点拨】1.水的电解实验:(1)现象:根据“正氧负氢、氢二氧一”判断。(2)产物检验。①负极:用燃着的木条,现象:能燃烧,产生淡蓝色火焰。②正极:用带火星的木条,现象:木条复燃。③结论:水由氢、氧元素组成。2.水的净化:(1)步骤:沉降→过滤→吸附→蒸馏。(2)过滤的注意事项。一贴:滤纸紧贴漏斗内壁。二低:滤纸边缘低于漏斗边缘、液面低于滤纸边缘。三靠:烧杯口紧靠玻璃棒;玻璃棒轻靠在三层滤纸处;漏斗下端紧靠烧杯内壁。【真题体验】1.(2013·上海中考)自来水厂对天然水进行人工净化的过程中,通常不会采用( )A.电解 B.吸附 C.过滤 D.消毒【解析】选A。本题考查学生对净化天然水步骤的认识。电解不属于天然水人工净化的过程。2.(2012·衡阳中考)下列有关水的描述中,不正确的是( )A.电解水时在正极产生氧气B.水是由氢原子和氧原子构成的C.可用肥皂水来区分硬水和软水D.在沉淀、过滤、蒸馏等净化水的操作中,净化程度最高的是蒸馏【解析】选B。水是由分子构成的纯净物,它的最小结构单位是水分子,氢原子和氧原子是构成水分子的结构单位。3.(2013·毕节中考)水是一切生命体生存所必需的物质,我们生活中使用的自来水是经过自来水厂净化处理的,主要净化过程是________。【解析】本题主要考查自来水厂的净水过程。自来水厂的主要净化过程包括沉淀、过滤、吸附等过程。答案:沉淀、过滤、吸附主题二:物质的构成【主题训练3】(2013·自贡中考)下列说法中,错误的是( )A.物理变化中分子种类不变。B.化学变化中,原子的种类和个数不变。C.带电的微粒都称为离子。D.分子、原子、离子都是构成物质的微粒。【解析】选C。在物理变化中,只是分子之间的间隔发生变化,而分子本身不发生变化,故A正确;化学变化的微观实质是分子分裂成原子,原子重新组合成新的分子的过程,该变化中原子的种类和个数不变,故B正确;带电的原子叫做离子,例如:电子带负电,但电子不是离子,故C错误;分子、原子、离子都是构成物质的微粒,故D正确。【训练备选】(2013·乌鲁木齐中考)下列叙述正确的是( )A.决定原子质量大小的主要是质子和电子。B.分子是保持物质性质的最小粒子。C.分子大,原子小。D.原子如果得到或失去电子就变成离子。【解析】选D。原子质量主要集中在原子核上,所以决定原子质量大小的主要是质子和中子,故A错;分子是保持物质化学性质的最小粒子,故B错;有的物质的分子比有的物质的原子大,有的物质的原子比有的物质的分子大,所以分子和原子不能比较大小,故C错;离子是带电荷的原子或原子团,原子如果得到或失去电子就变成离子,故D正确。【关键点拨】构成物质的粒子1.分子、原子、离子都可以直接构成物质。2.分子和原子的比较:(1)相同点:性质相似,都具有以下特征:质量和体积很小、不断运动、微粒间有间隔等。(2)不同点。①原子是化学变化中的最小微粒,分子是保持物质化学性质的最小微粒。②在化学变化中,分子可以再分,原子不可再分。(3)联系:分子是由原子构成的,原子间互相结合形成分子。3.同一元素的原子和离子之间可以通过得失电子相互转化。阳离子 原子 阴离子(带正电荷) (带负电荷)【真题体验】1.(2013·成都中考)以下事实不能用粒子运动的观点来解释的是( )A.走过花圃闻到花香。B.湿衣服经过晾晒变干。C.香水、汽油密闭保存。D.6000L氧气在加压下可装入容积为40L的钢瓶中。【解析】选D。本题是利用分子与原子的性质分析来解决问题。A、B、C中现象的发生均是粒子不断运动造成的;液体混合前后体积发生了改变是因为分子间存在间隔。2.(2013·怀化中考)下列有关分子、原子和离子的说法正确的是( )A.保持氧气化学性质的粒子是氧原子。B.原子的最外层电子数决定元素的种类。C.氯化钠是由离子构成的化合物。D.分子间有一定间隔,原子间没有间隔。【解析】选C。氧气由氧分子构成,所以氧分子是保持氧气化学性质的粒子;元素的种类决定于质子数;氯化钠由钠离子和氯离子构成;分子和原子间都有一定的间隔。3.(2012·锦州中考)如图是5种粒子的结构示意图,请回答下列问题:(1)在化学反应中,容易失去电子的是__(填字母)。(2)属于同种元素的粒子是________(填字母)。(3)若D带有2个单位的正电荷,则x=________。【解析】(1)由5种粒子的结构示意图可知,在C的结构示意图中,最外层的电子数是1,少于4个,在化学反应中,容易失去电子;(2)由元素的定义可知,5种粒子的结构示意图中,A、E的质子数相同都是8,属于同种元素;(3)由题意可知,若D带有2个单位的正电荷,则D的原子核外有12个电子,则核内的质子数是12。答案:(1)C (2)A、E (3)12主题三:组成物质的元素【主题训练4】(2013·滨州中考)如图中的①、②分别是钠元素、氯元素在元素周期表中的信息,A、B、C是三种粒子的结构示意图。试回答下列问题:(1)钠元素的原子序数为________,画出它的原子结构示意图________。(2)A、B、C中属于同种元素的粒子是________。(3)A和B两种粒子的________相同,所以它们具有相似的化学性质。(4)钠原子和氯原子反应所形成的化合物是由________(填“分子”“原子”“离子”)构成的。【解析】本题考查学生对元素周期表的信息及粒子结构示意图的应用能力。钠的原子序数为11;B、C核内质子数相同则为同种元素;A、B两种粒子的最外层电子数相同,因此,化学性质相似;氯化钠由钠离子和氯离子构成。答案:(1)11 (2)B、C (3)最外层电子数(4)离子【训练备选】(2013·南宁中考)根据图表提供的信息,下列判断错误的是( )A.镁的原子序数是12B.钠原子核外有三个电子层。C.表中所列元素均为金属元素。D.元素所在的周期序数等于其原子的电子层数。【解析】选C。元素周期表中左上角数字表示该元素的原子序数,所以镁的原子序数是12,故A说法正确;由图示可知钠原子核外有三个电子层,故B说法正确;金属元素是带“钅”字旁的(汞和金除外),表中氢和硼属于非金属元素,故C说法错误;由表中数据可知元素所在的周期数等于其原子的电子层数,故D说法正确。【关键点拨】元素、原子、分子、物质之间的关系【真题体验】1.(2013·南宁中考)正确读写化学符号是学好化学的基础。铝元素符号书写正确的是( )A.AL B.al C.aL D.Al【解析】选D。书写元素符号时应注意:①由一个字母表示的元素符号要大写;②由两个字母表示的元素符号,第一个字母大写,第二个字母小写。故选D。2.(2013·聊城中考)镉属于重金属,会危害人体健康。2013年5月16日,广州市食品药品监管公布的结果显示,抽检大米四成镉超标。这里的镉可理解为( )A.镉元素 B.镉单质 C.镉离子 D.镉原子【解析】选A。大米中的镉超标,这里的镉不是以单质、分子、原子、离子等形式存在,这里所指的“镉”是强调存在的元素,与具体形态无关。【知识拓展】重金属污染对人体的主要危害 对人体毒害最大的重金属有4种:铅、汞、砷、镉。这些重金属在水中不能被分解,人饮用后毒性大,与水中的其他毒素结合生成毒性更大的物质。 重金属一般以天然浓度广泛存在于自然界中,但由于人类对重金属的开采、冶炼、加工及商业制造活动日益增多,造成不少重金属如铅、汞、镉、钴等进入大气、水、土壤中,引起严重的环境污染。 以各种化学状态或化学形态存在的重金属,在进入环境或生态系统后就会存留、积累和迁移,从而对人体健康造成危害。3.(2013·柳州中考)在地壳中含量最多的非金属元素是( )A.氧(O) B.硅(Si) C.钠(Na) D.铝(Al)【解析】选A。地壳含量较多的元素(前四种)按含量从高到低的排序为氧、硅、铝、铁,其中含量最多的非金属元素是氧元素。4.(2013·绥化中考)如图是元素周期表中钼元素的相关信息。写出两条从图中获得的信息:(1)___________________________________。(2)___________________________________。【解析】本题考查对元素周期表单元格信息的掌握能力,从单元格中可以获得的信息有:元素的元素符号、元素的相对原子质量和元素的种类等。答案:钼元素符号是Mo或钼是金属元素或钼的相对原子质量是95.94或钼是42号元素等(写出两种任意合理答案即可)。谢 谢
第二单元 探索水世界 复习课件主题一:水的净化与水的电解【主题训练1】(2013·乌鲁木齐中考)在电解水的实验中,可以直接观察到的现象是( )A.水由氢、氧两种元素组成。B.有氢气和氧气产生,且体积比为2∶1C.在电极上均有气泡产生,两个试管内气体的体积之比约为2∶1D.每个水分子是由两个氢原子和一个氧原子构成的。【解析】选C。水是由氢、氧两种元素组成的,有氢气和氧气产生是通过电解水的实验得出的实验结论;通电后,在电极上均有气泡产生,两个试管内气体的体积之比约为2∶1,此现象能直接观察到;每个水分子是由两个氢原子和一个氧原子构成的,是通过对电解水的实验综合分析得出的实验结论。故选C。【主题训练2】(2013·济南中考)泉水是“泉城”济南的文化之魂,首届济南泉水节于2013年8月28日开幕。节水环保、杜绝水污染、建设美丽泉城,是我们泉城人的职责。(1)自然界中,水的存在形式多姿多彩,水孕育了万物生灵,水通过三态变化实现天然循环,这个循环过程是由________提供的能量(填序号)。A.地球自转 B.太阳照射C.海洋潮汐 D.植物生长(2)某化学小组的小泉同学取趵突泉水进行探究实验。先将水样进行过滤操作如图所示,操作中的一处错误是________;再用滴管取2滴过滤后的滤液滴在洁净的玻璃片上,置于酒精灯上小心加热,水分消失后,观察到玻璃片上有少许残留物,产生该现象的原因是_____________________。【解析】水的三态变化是通过太阳能提供能量的;进行过滤操作时,漏斗的下端管口应紧靠烧杯内壁;由于滤液中含有一些可溶性杂质,故加热滤液,水分消失后,会观察到玻璃片上有少许固体残留物。答案:(1)B (2)漏斗的下端管口没有紧靠烧杯内壁,滤液中含有一些可溶性杂质。【关键点拨】1.水的电解实验:(1)现象:根据“正氧负氢、氢二氧一”判断。(2)产物检验。①负极:用燃着的木条,现象:能燃烧,产生淡蓝色火焰。②正极:用带火星的木条,现象:木条复燃。③结论:水由氢、氧元素组成。2.水的净化:(1)步骤:沉降→过滤→吸附→蒸馏。(2)过滤的注意事项。一贴:滤纸紧贴漏斗内壁。二低:滤纸边缘低于漏斗边缘、液面低于滤纸边缘。三靠:烧杯口紧靠玻璃棒;玻璃棒轻靠在三层滤纸处;漏斗下端紧靠烧杯内壁。【真题体验】1.(2013·上海中考)自来水厂对天然水进行人工净化的过程中,通常不会采用( )A.电解 B.吸附 C.过滤 D.消毒【解析】选A。本题考查学生对净化天然水步骤的认识。电解不属于天然水人工净化的过程。2.(2012·衡阳中考)下列有关水的描述中,不正确的是( )A.电解水时在正极产生氧气B.水是由氢原子和氧原子构成的C.可用肥皂水来区分硬水和软水D.在沉淀、过滤、蒸馏等净化水的操作中,净化程度最高的是蒸馏【解析】选B。水是由分子构成的纯净物,它的最小结构单位是水分子,氢原子和氧原子是构成水分子的结构单位。3.(2013·毕节中考)水是一切生命体生存所必需的物质,我们生活中使用的自来水是经过自来水厂净化处理的,主要净化过程是________。【解析】本题主要考查自来水厂的净水过程。自来水厂的主要净化过程包括沉淀、过滤、吸附等过程。答案:沉淀、过滤、吸附主题二:物质的构成【主题训练3】(2013·自贡中考)下列说法中,错误的是( )A.物理变化中分子种类不变。B.化学变化中,原子的种类和个数不变。C.带电的微粒都称为离子。D.分子、原子、离子都是构成物质的微粒。【解析】选C。在物理变化中,只是分子之间的间隔发生变化,而分子本身不发生变化,故A正确;化学变化的微观实质是分子分裂成原子,原子重新组合成新的分子的过程,该变化中原子的种类和个数不变,故B正确;带电的原子叫做离子,例如:电子带负电,但电子不是离子,故C错误;分子、原子、离子都是构成物质的微粒,故D正确。【训练备选】(2013·乌鲁木齐中考)下列叙述正确的是( )A.决定原子质量大小的主要是质子和电子。B.分子是保持物质性质的最小粒子。C.分子大,原子小。D.原子如果得到或失去电子就变成离子。【解析】选D。原子质量主要集中在原子核上,所以决定原子质量大小的主要是质子和中子,故A错;分子是保持物质化学性质的最小粒子,故B错;有的物质的分子比有的物质的原子大,有的物质的原子比有的物质的分子大,所以分子和原子不能比较大小,故C错;离子是带电荷的原子或原子团,原子如果得到或失去电子就变成离子,故D正确。【关键点拨】构成物质的粒子1.分子、原子、离子都可以直接构成物质。2.分子和原子的比较:(1)相同点:性质相似,都具有以下特征:质量和体积很小、不断运动、微粒间有间隔等。(2)不同点。①原子是化学变化中的最小微粒,分子是保持物质化学性质的最小微粒。②在化学变化中,分子可以再分,原子不可再分。(3)联系:分子是由原子构成的,原子间互相结合形成分子。3.同一元素的原子和离子之间可以通过得失电子相互转化。阳离子 原子 阴离子(带正电荷) (带负电荷)【真题体验】1.(2013·成都中考)以下事实不能用粒子运动的观点来解释的是( )A.走过花圃闻到花香。B.湿衣服经过晾晒变干。C.香水、汽油密闭保存。D.6000L氧气在加压下可装入容积为40L的钢瓶中。【解析】选D。本题是利用分子与原子的性质分析来解决问题。A、B、C中现象的发生均是粒子不断运动造成的;液体混合前后体积发生了改变是因为分子间存在间隔。2.(2013·怀化中考)下列有关分子、原子和离子的说法正确的是( )A.保持氧气化学性质的粒子是氧原子。B.原子的最外层电子数决定元素的种类。C.氯化钠是由离子构成的化合物。D.分子间有一定间隔,原子间没有间隔。【解析】选C。氧气由氧分子构成,所以氧分子是保持氧气化学性质的粒子;元素的种类决定于质子数;氯化钠由钠离子和氯离子构成;分子和原子间都有一定的间隔。3.(2012·锦州中考)如图是5种粒子的结构示意图,请回答下列问题:(1)在化学反应中,容易失去电子的是__(填字母)。(2)属于同种元素的粒子是________(填字母)。(3)若D带有2个单位的正电荷,则x=________。【解析】(1)由5种粒子的结构示意图可知,在C的结构示意图中,最外层的电子数是1,少于4个,在化学反应中,容易失去电子;(2)由元素的定义可知,5种粒子的结构示意图中,A、E的质子数相同都是8,属于同种元素;(3)由题意可知,若D带有2个单位的正电荷,则D的原子核外有12个电子,则核内的质子数是12。答案:(1)C (2)A、E (3)12主题三:组成物质的元素【主题训练4】(2013·滨州中考)如图中的①、②分别是钠元素、氯元素在元素周期表中的信息,A、B、C是三种粒子的结构示意图。试回答下列问题:(1)钠元素的原子序数为________,画出它的原子结构示意图________。(2)A、B、C中属于同种元素的粒子是________。(3)A和B两种粒子的________相同,所以它们具有相似的化学性质。(4)钠原子和氯原子反应所形成的化合物是由________(填“分子”“原子”“离子”)构成的。【解析】本题考查学生对元素周期表的信息及粒子结构示意图的应用能力。钠的原子序数为11;B、C核内质子数相同则为同种元素;A、B两种粒子的最外层电子数相同,因此,化学性质相似;氯化钠由钠离子和氯离子构成。答案:(1)11 (2)B、C (3)最外层电子数(4)离子【训练备选】(2013·南宁中考)根据图表提供的信息,下列判断错误的是( )A.镁的原子序数是12B.钠原子核外有三个电子层。C.表中所列元素均为金属元素。D.元素所在的周期序数等于其原子的电子层数。【解析】选C。元素周期表中左上角数字表示该元素的原子序数,所以镁的原子序数是12,故A说法正确;由图示可知钠原子核外有三个电子层,故B说法正确;金属元素是带“钅”字旁的(汞和金除外),表中氢和硼属于非金属元素,故C说法错误;由表中数据可知元素所在的周期数等于其原子的电子层数,故D说法正确。【关键点拨】元素、原子、分子、物质之间的关系【真题体验】1.(2013·南宁中考)正确读写化学符号是学好化学的基础。铝元素符号书写正确的是( )A.AL B.al C.aL D.Al【解析】选D。书写元素符号时应注意:①由一个字母表示的元素符号要大写;②由两个字母表示的元素符号,第一个字母大写,第二个字母小写。故选D。2.(2013·聊城中考)镉属于重金属,会危害人体健康。2013年5月16日,广州市食品药品监管公布的结果显示,抽检大米四成镉超标。这里的镉可理解为( )A.镉元素 B.镉单质 C.镉离子 D.镉原子【解析】选A。大米中的镉超标,这里的镉不是以单质、分子、原子、离子等形式存在,这里所指的“镉”是强调存在的元素,与具体形态无关。【知识拓展】重金属污染对人体的主要危害 对人体毒害最大的重金属有4种:铅、汞、砷、镉。这些重金属在水中不能被分解,人饮用后毒性大,与水中的其他毒素结合生成毒性更大的物质。 重金属一般以天然浓度广泛存在于自然界中,但由于人类对重金属的开采、冶炼、加工及商业制造活动日益增多,造成不少重金属如铅、汞、镉、钴等进入大气、水、土壤中,引起严重的环境污染。 以各种化学状态或化学形态存在的重金属,在进入环境或生态系统后就会存留、积累和迁移,从而对人体健康造成危害。3.(2013·柳州中考)在地壳中含量最多的非金属元素是( )A.氧(O) B.硅(Si) C.钠(Na) D.铝(Al)【解析】选A。地壳含量较多的元素(前四种)按含量从高到低的排序为氧、硅、铝、铁,其中含量最多的非金属元素是氧元素。4.(2013·绥化中考)如图是元素周期表中钼元素的相关信息。写出两条从图中获得的信息:(1)___________________________________。(2)___________________________________。【解析】本题考查对元素周期表单元格信息的掌握能力,从单元格中可以获得的信息有:元素的元素符号、元素的相对原子质量和元素的种类等。答案:钼元素符号是Mo或钼是金属元素或钼的相对原子质量是95.94或钼是42号元素等(写出两种任意合理答案即可)。谢 谢
相关资料
更多









