
高中化学人教版 (2019)必修 第二册第七章 有机化合物第三节 乙醇与乙酸同步测试题
展开一、单选题
1.经研究发现白蚁信息素有: (2,4-二甲基-1-庚烯), (3,7-二甲基-1-辛烯),家蚕的性信息素为:CH3(CH2)8CH==CH—CH==CH(CH2)8CH3。下列说法不正确的是
A.2,4-二甲基1庚烯的分子式为C9H18
B.2,4-二甲基-1-庚烯与3,7-二甲基-1-辛烯互为同系物
C.以上三种信息素均能使溴的四氯化碳溶液褪色
D.1 ml家蚕的性信息素与1 ml Br2加成,产物只有一种
2.下列有关物质组成或结构的判断正确的是
A.分子式为C2H4O2的有机物一定是乙酸
B.甲烷、乙烷、丙烷的一氯代物都只有一种
C.的分子式为C11H20O
D.在光照条件下,与Br2反应可能得到的一溴代物有6种
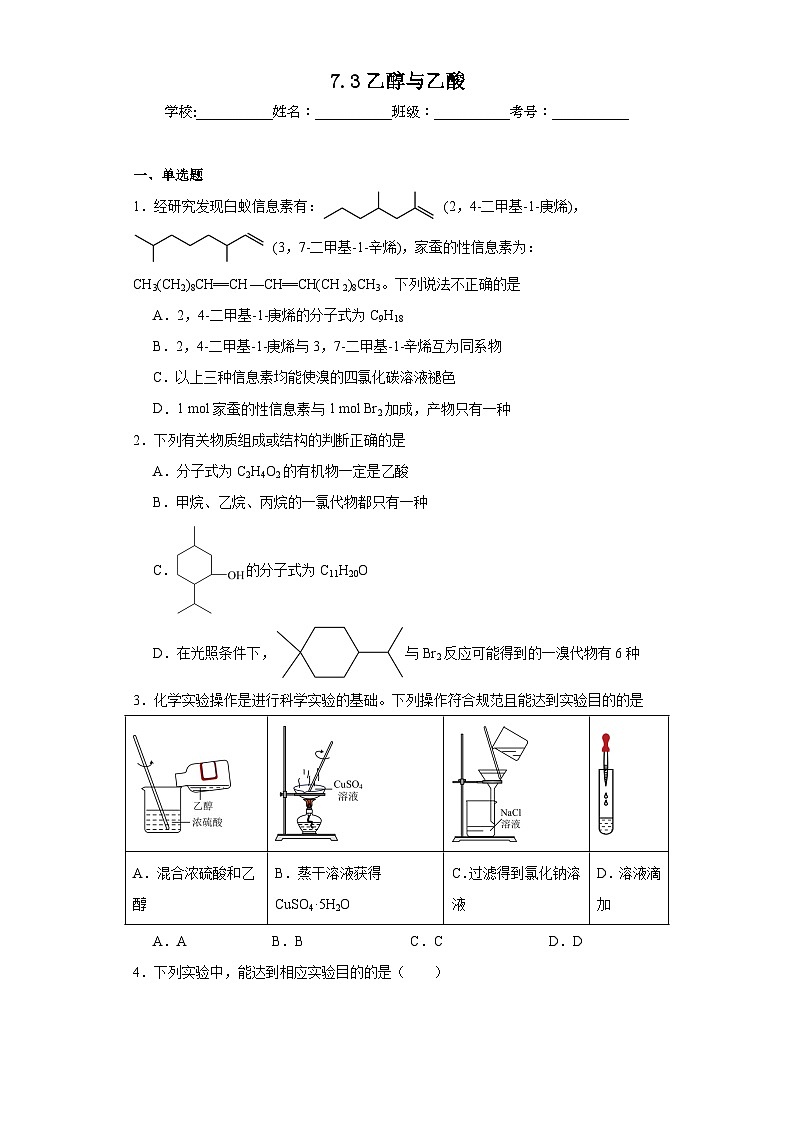
3.化学实验操作是进行科学实验的基础。下列操作符合规范且能达到实验目的的是
A.AB.BC.CD.D
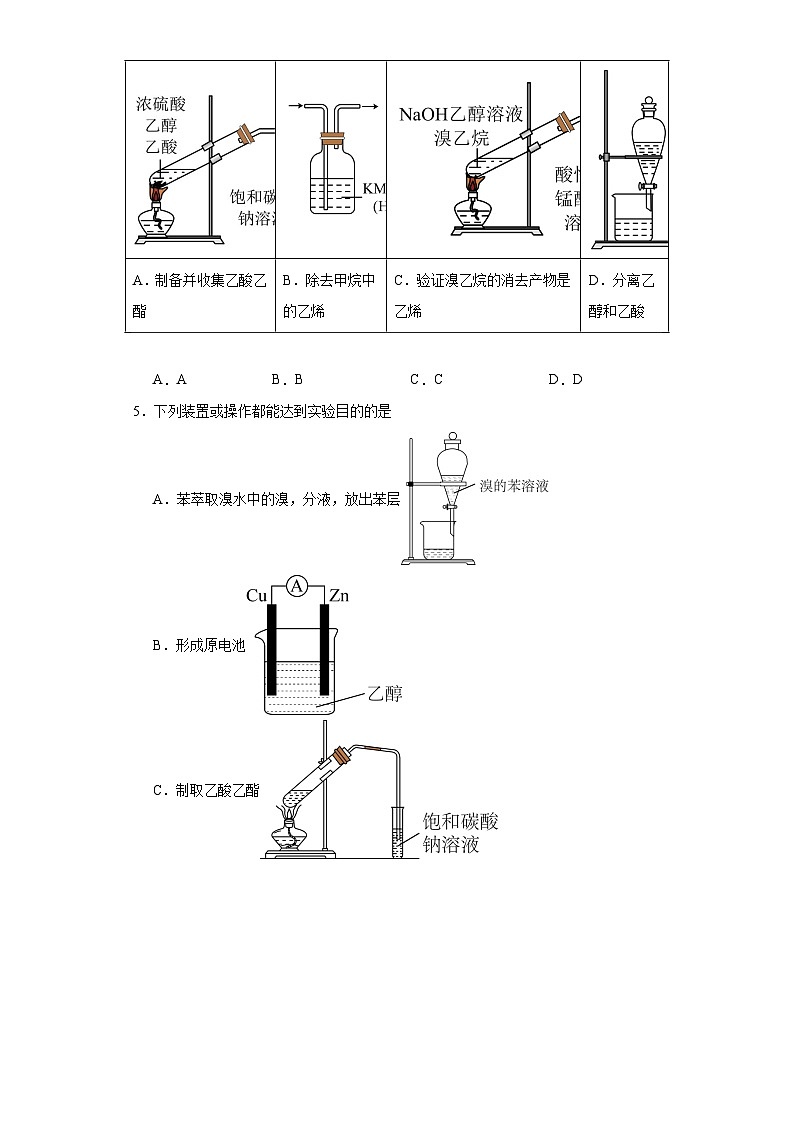
4.下列实验中,能达到相应实验目的的是( )
A.AB.BC.CD.D
5.下列装置或操作都能达到实验目的的是
A.苯萃取溴水中的溴,分液,放出苯层
B.形成原电池
C.制取乙酸乙酯
D.蒸馏米酒
6.下列关于酯化反应说法正确的是
A.用CH3CH218OH与CH3COOH发生酯化反应,生成H218O
B.反应液混合时,将浓硫酸倒入乙醇和乙酸的混合液中
C.可用分液漏斗分离饱和Na2CO3溶液和乙酸乙酯的混合溶液
D.在制备乙酸乙酯的实验中,为了防止乙酸和乙醇挥发,小火加热,避免液体沸腾
7.山梨酸是常用的食品防腐剂,其结构简式如图所示,下列有关山梨酸的叙述正确的是
A.不能发生取代反应,能发生加成反应
B.分子中所有碳原子可能在同一平面上
C.与互为同分异构体
D.1ml该物质与足量Na反应生成2gH2
8.在乙醇发生的各种反应中,断键方式不正确的是
A.与金属钠反应时,键①断裂B.与醋酸、浓硫酸共热时,键②断裂
C.与浓硫酸共热至170℃时,键②和④断裂D.与HCl反应生成氯乙烷时,键②断裂
9.下列化合物中,既不能与NaOH溶液发生反应,又不能与溴的CCl4溶液反应,也不能使酸性KMnO4溶液褪色的是
A.丙烷B.乙醇
C.乙酸D.丙烯
10.只用水就能鉴别的一组物质是( )
A.苯、乙醇、四氯化碳B.乙醇、乙醛、乙酸
C.乙醛、乙二醇、硝基苯D.乙醇、溴苯、甲酸
二、填空题
11.乙酸的物理性质
食醋是生活中常见的调味品,其中含有3%~5%的乙酸,纯乙酸在温度低于熔点(16.6℃)时凝结成类似冰一样的晶体,因此纯净的乙酸又称为 。
12.根据下图,回答问题。
(1)有机物的名称: B. F. ,E中所含官能团的名称 。
(2)有机物的结构简式:C. ,G. 。
(3)反应D®E的化学方程式是 .
(4)A®B的反应类型属于 。
(5)写出实验室制取A的化学方程式 。
13.乙酸的分子结构与物理性质
(1)分子结构
①乙酸的分子式为 ,结构式为 ,结构简式为 。
②乙酸的官能团是 。
(2)物理性质
①乙酸又称 或 ,食醋中含有 的乙酸。
②乙酸是一种无色、具有刺激性气味的液体,能与水和酒精以任意比互溶,易挥发。
14.化学工业为疫情防控提供了强有力的物质支撑。常用的消毒剂产品按成分可以分为含氯消毒剂、醇类消毒剂、含碘消毒剂等9种。回答下列问题:
(1)①碘酊又称碘酒,常见配制方法是将一定质量的单质碘溶于适量酒精,再加水稀释。碘酒属于 。(选填:溶液、胶体、悬浊液、乳浊液)
②I4O9是碘元素最稳定的氧化物之一,已知其中碘元素的化合价为+3、+5价,则I4O9中+3价和+5价的碘原子数目之比为 ,若I4O9溶于水会生成两种含氧酸,写出该过程的化学方程式 。
(2)乙醇是生活中最常见的醇类消毒剂。
①下列关于乙醇的说法正确的是 。
a.将日常饮用的白酒直接蒸馏即可得到无水乙醇
b.95%的酒精消毒杀菌效果比浓度为75%的酒精好
c.表面氧化的铜丝在酒精灯内焰加热时会恢复红色,说明酒精具有挥发性和还原性
d.平时生活中,可以采用大面积喷洒酒精的方式对室内等封闭空间消毒
②酒驾的检测原理是乙醇使酸化的K2Cr2O7橙色溶液迅速还原成绿色的Cr2O3,同时生成无色无味气体,写出该反应的离子方程式 。
(3)“84”消毒液的有效成分是NaClO,某同学用广泛PH试纸测量该种市售消毒液的PH,观察到的现象是 ,造成该现象的原因是 。
(4)广谱消毒剂ClO2可利用电解饱和食盐水的方法制得,写出该电极反应方程式 。
15.阿司匹林()能解热镇痛。
(1)阿司匹林中含氧官能团有酯基和 (填名称)。
(2)向阿司匹林的水溶液中滴入2~3滴紫色石蕊溶液,溶液颜色变红,说明阿司匹林溶液具有 性。
(3)阿司匹林在一定条件下水解生成水杨酸()和另一种酸A,试写出另一种酸A的结构简式 。
16.有下列微粒:①16O ②35Cl2 ③18O ④14N ⑤14C ⑥ H ⑦ D ⑧37Cl2
(1)互为同位素的是: ;(填序号,下同)中子数相等的是:
(2)同位素原子可以用作“示踪原子”,研究一些反应机理。
①已知可逆反应2SO2+O22SO3 ,向一密闭容器内充入SO2和18O2,反应一段时间后,18O可能存在于
A.仅O2中 B.仅SO3中 C. 仅O2和SO3中 D.O2、 SO2、SO3中
②根据乙酸和乙醇发生反应的原理,写出CH3CO18OH与CH3CH2OH反应的化学方程式: 。
(3)20g D2O中质子的物质的量为:
17.写出乙酸和乙醇反应的化学方程式 。二者在一定条件下发生反应的类型是 。
18.已知乳酸的结构简式为 。试回答:
(1)乳酸分子中含有两种官能团为 (写名称);
(2)乳酸与足量金属钠反应的化学方程式为
;
(3)乳酸与Na2CO3溶液反应的化学方程式为
;
19.近年来,乳酸成为研究热点之一。乳酸可以用化学方法合成,也可以由淀粉通过发酵法制备。以乳酸()为原料制成的高分子材料具有生物相容性,而且在哺乳动物体内或自然环境中最终降解为二氧化碳和水。
(1)乳酸分子中所含有的官能团名称为 。
(2)乳酸可与金属钠、溶液反应,等物质的量的乳酸分别与和溶液反应时,消耗 。
(3)乳酸能与铁粉反应制备一种补铁药物乳酸亚铁[],请写出反应的化学方程式: 。
(4)写出一种比乳酸少一个碳原子的同系物的结构简式: 。
(5)乳酸在一定条件下分子内脱去一分子水生成丙烯酸()。由丙烯酸一步制得聚丙烯酸的有机反应类型为 ;下列关于丙烯酸的性质的说法错误的是 (填标号)。
A.丙烯酸可使溴水或酸性溶液褪色,二者的原理相同
B.丙烯酸可与新制反应
C.一定条件下,丙烯酸与反应可能得到两种有机物
D.丙烯酸与为同种物质
聚丙烯酸可用于配制某些高档商品的涂饰剂、制取丙烯酸树脂漆等。写出聚丙烯酸的结构简式: 。
20.写出下列反应的化学方程式:
(1)甲酸与新制氢氧化铜悬浊液受热: ;
(2)乙二酸和乙二醇酯化成环: ;
(3)HOCH2CH2CH2COOH在浓硫酸加热条件下分子内成环的反应方程式: ;
(4)1分子咖啡与2分子CH3COCl在一定条件下发生反应生成酯的方程式: ;
(5)丙烯酸甲酯(CH2=CHCOOCH3)加聚反应方程式: ;
(6)发生银镜反应的化学方程式: ;
(7)与足量NaOH溶液共热的化学方程式: ;
三、判断题
21.将冰醋酸、乙醇和2ml/L的硫酸加热制取乙酸乙酯。( )
22.乙酸分子中含有和—OH两种官能团。( )
23.医用酒精的浓度通常为95%。( )
24.质量分数为75%的乙醇溶液常作消毒剂。(_______)
25.制备乙酸乙酯时可用热的NaOH溶液收集产物以除去其中的乙酸。( )
四、解答题
26.苯甲酸乙酯( )是重要的精细化工试剂,常用于配制水果型食用香精。实验室制备流程如下:
试剂相关性质如下表:
回答下列问题:
(1)为提高原料苯甲酸的纯度,可采用的纯化方法为 。
(2)步骤①的装置如图所示(加热和夹持装置已略去)将一小团棉花放仪器B中靠近活塞孔处,将吸水剂(无水硫酸铜的乙醇饱和溶液)放入仪器B中,在仪器C中加入纯化后的苯甲酸晶体、无水乙醇(约)和浓硫酸,加入沸石加热至微沸,回流反应。仪器A的作用是 ;仪器C中反应液最好应采用 方式加热。
(3)随着反应进行,反应体系中水分不断被有效分离,仪器B中吸水剂的现象为 。
(4)反应结束后,对C中混合液进行分离提纯,操作Ⅰ是 ;操作Ⅱ所用的玻璃仪器除了烧杯外还有 。
(5)反应结束后,步骤③中将反应液倒冷水的目的除了溶解乙醇外,还有 ;加入的试剂X为 (填写化学式)。
27.某课外小组设计的实验室制取乙酸乙酯的装置如图已知:A中放有浓硫酸;B中放有乙醇、乙酸;D中放有饱和碳酸钠溶液。
有机物的相关数据如表:
请回答:
(1)浓硫酸的作用: 、 。
(2)仪器C的名称是 ,其作用有 和 ,若反应前向D中加入几滴酚酞,溶液呈红色。实验完毕后,将烧杯D中的溶液充分振荡、静置,现象为 。
(3)若用同位素18O标记乙醇中的氧原子,写出反应的化学方程式: 。
(4)某学习小组用3.00mL乙醇、2.00mL乙酸、2.00mL浓硫酸进行实验,实验结束得到2.20mL乙酸乙酯,则该实验的产率为 %。(产率等于实际产量除以理论产量;结果保留3位有效数字。)
28.已知:A是石油裂解气的主要产物之一,其产量常用于衡量一个国家石油化工发展水平的标志。下列是有机物A~G之间的转化关系:
请回答下列问题:
(1)A官能团的名称是 ;D官能团名称: ;C结构简式: 。
(2)B是一种具有特殊香味的液体,写出B→E的化学反应方程式 ,该反应类型是 。
(3)比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射物质F(沸点12.27℃)进行应急处理。写出由A制F的化学反应方程式 。由氯乙烯可以制取某种高分子化合物,写出该物质的结构简式 。
(4)某同学用如图所示的实验装置制取少量乙酸乙酯。实验结束后,试管甲上层为透明且不溶于水的油状液体。
①实验结束后,振荡试管甲,有无色气泡生成,其主要原因是(用化学方程式表示) 。
②除去乙酸乙酯中混有的少量乙酸和乙醇,应加入 ,分离时用到的主要仪器是 。
A.混合浓硫酸和乙醇
B.蒸干溶液获得CuSO4·5H2O
C.过滤得到氯化钠溶液
D.溶液滴加
A.制备并收集乙酸乙酯
B.除去甲烷中的乙烯
C.验证溴乙烷的消去产物是乙烯
D.分离乙醇和乙酸
俗名
颜色
状态
气味
溶解性
挥发性
色
体
刺激性
溶于水和乙醇
挥发
苯甲酸
乙醇
苯甲酸乙酯
常温性状
白色针状晶体
无色液体
无色透明液体
沸点/℃
249.0
78.0
212.6
相对分子量
122
46
150
溶解性
微溶于水,易溶于乙醇、乙醚等有机溶剂
与水任意比互溶
难溶于冷水,微溶于热水,易溶于乙醇和乙醚
试剂
乙醇
乙酸
乙酸乙酯
沸点/℃
78.5
118
77.1
密度(g/cm3)
0.7893
1.05
0.900
相对分子质量
46
60
88
参考答案:
1.D
【详解】A、根据键线式和碳原子的4价理论可知,2,4-二甲基-1-庚烯的分子式为C9H18,A正确;
B、2,4-二甲基-1-庚烯与l-庚烯分子式不同,结构相似,二者互为同系物,B正确;
C、三种信息素都含有碳碳双键,均可与溴发生加成反应而使溴的四氯化碳褪色,C正确;
D、家蚕信息素与溴可发生1,2-加成或1,4-加成,因此与1mlBr2加成产物有两种,D错误,
答案选D。
2.D
【详解】A.分子式为C2H4O2的有机物可以是乙酸(CH3COOH),也可以是甲酸甲酯(HCOOCH3),故A错误;
B.甲烷(CH4)有一种H,乙烷(CH3CH3)有1种H,丙烷(CH3CH2CH3)有2种H,一氯代物数目分别为1种、1种、2种,故B错误;
C.由结构简式可知,其分子式为C10H20O,故C错误;
D.由可知,在光照条件下与Br2发生取代反应,得到的一溴代物有6种,位置如图所示,故D正确;
答案为D。
3.C
【详解】A.混合浓硫酸和乙醇时,应将密度大的浓硫酸缓慢加入到乙醇中,故A错误;
B.蒸干硫酸铜溶液时,会使五水硫酸铜受热脱去结晶水,无法制得五水硫酸铜,故B错误;
C.过滤氯化钠溶液时,烧杯应紧贴着玻璃棒,玻璃棒应紧靠着三层滤纸,漏斗下端应紧靠烧杯内壁,防止液体飞溅,故C正确;
D. 用胶头滴管向试管中滴入溶液时,胶头滴管不能插入试管内,故D错误;
故选C。
4.A
【详解】A. 反应物是乙酸、乙醇,浓硫酸作催化剂和吸水剂,用饱和碳酸钠溶液接受乙酸乙酯,故A符合题意;
B. 酸性高锰酸钾与乙烯反应生成二氧化碳,因此不能用酸性高锰酸钾除掉甲烷中的乙烯,只能用溴水或溴的四氯化碳除掉,故B不符合题意;
C. 乙醇易挥发,乙醇也能被酸性高锰酸钾氧化而溶液褪色,因此不能验证消去产物为乙烯,故C不符合题意;
D. 乙酸和乙醇是互溶的不能用分液来分离,故D不符合题意。
综上所述,答案为A。
【点睛】检验甲烷中的乙烯用溴水或酸性高锰酸钾溶液;除掉甲烷中的乙烯用溴水。
5.D
【详解】A. 苯的密度小于水的密度,分层后溴的苯溶液在上层,分液时,上层液体从上口倒出,下层液体从下口流出,而本题中溴的苯溶液从下口流出,故A错误;
B. 乙醇为非电解质,该装置不是闭合回路,因此不能构成原电池,故B错误;
C. 制取乙酸乙酯时,为防止倒吸,导管不能伸入液面以下,而本题中导管伸入液面以下,故C错误;
D. 蒸馏米酒需要用蒸馏装置,题中所给装置,符合蒸馏装置的要求,故D正确;
答案为D。
6.C
【详解】A.根据酯化反应规律特点“酸脱羟基醇脱氢”可知18O应存在酯中,故A错误;
B.酯化反应加入试剂先后顺序为:先加入醇,再加入浓硫酸和羧酸,故B错误;
C.乙酸乙酯在饱和碳酸钠溶液中溶解度降低分层,可用分液漏斗进行分液,故C正确;
D.小火加热主要目的是为了避免温度过高生成其它产物,例如乙醇和浓硫酸在140℃会发生反应分子间脱水成醚,故D错误;
答案选C。
7.C
【详解】A.该分子中的羧基和醇羟基均能发生取代反应,碳碳双键能发生加成反应,A错误;
B.箭头所指的C()为烷烃的C,以这个C为中心形成四面体形,因此所有的C不可能共平面,B错误;
C.和的分子式均为C7H10O5,分子式相同但结构不同,二者互为同分异构体,C正确;
D.羧基和羟基都能和Na反应生成氢气,且存在关系式2-COOH~H2、2-OH~H2,则1ml该有机物与足量Na反应生成1.5ml氢气,生成氢气的质量为1.5ml×2g/ml=3g,D错误;
故选C。
8.B
【详解】A.与金属钠反应时,生成乙醇钠和氢气,乙醇中的O-H键断裂,即键①断裂, A项正确;
B.与醋酸、浓硫酸共热时,发生酯化反应,醇脱H,故乙醇中的O-H键断裂,即键①断裂,B项错误;
C.与浓硫酸共热至170℃时,发生消去反应生成乙烯和水,C-O、甲基上的C-H键断裂,即键②和④断裂,C项正确;
D.与HCl反应生成氯乙烷时,-OH被-Cl取代,C-O键断裂,即键②断裂,D项正确;
答案应选B。
9.A
【详解】A.丙烷性质稳定,与氢氧化钠、溴的四氯化碳以及高锰酸钾都不反应,故A符合题意;
B.乙醇可与酸性高锰酸钾发生氧化还原反应,故B不符合题意;
C.乙酸可与氢氧化钠发生中和反应,故C不符合题意;
D.丙烯含有碳碳双键,可与溴的四氯化碳发生加成反应,与高锰酸钾发生氧化还原反应,故D不符合题意;
答案选A。
10.A
【详解】A.乙醇与水混溶,苯和四氯化碳不溶于水,但苯的密度比水小,四氯化碳的密度比水大,可鉴别,故A正确;
B.乙醇、乙醛、乙酸都溶于水,不能鉴别,故B错误;
C.乙醛、乙二醇都溶于水,不能鉴别,故C错误;
D.乙醇、甲酸都溶于水,不能鉴别,故D错误;
答案选A。
【点睛】只用水就能鉴别,可根据物质的水溶性、密度的大小或者是否与水反应的性质进行鉴别。
11. 醋酸 无 液 强烈 易 易 冰醋酸
【解析】略
12. 氯乙烯 乙酸 羟基 CH3COOC2H5 CH2=CH2 + H2O CH3CH2OH 加成反应 CaC2+2H2O→CH≡CH↑+Ca(OH) 2
【详解】试题分析:碳化硅与水反应生成氢氧化钙和乙炔,即A是乙炔。乙炔与氯化氢发生加成反应生成氯乙烯,即B是氯乙烯。氯乙烯发生加聚反应生成聚氯乙烯,即C是聚氯乙烯。乙炔与氢气发生加成反应生成乙烯,乙烯与水发生加成反应生成乙醇。乙醇氧化可以转化为乙酸,乙酸与乙醇酯化生成乙酸乙酯,所以D是乙烯,E是乙醇,F是乙酸,G是乙酸乙酯。
(1)根据以上分析可知B、F分别是氯乙烯、乙酸乙醇中所含官能团的名称是羟基。
(2)C、G的结构简式分别表示、CH3COOC2H5。
(3)反应D→E的化学方程式是)CH2=CH2 + H2OCH3CH2OH。
(4)A→B的反应类型属于加成反应。
(5)实验室制取A的化学方程式为CaC2+2H2O→CH≡CH↑+Ca(OH) 2。
考点:考查有机物推断的应用
13.(1) C2H4O2 CH3COOH 羧基
(2) 醋酸 冰醋酸 3%~5%
【详解】(1)①乙酸的分子式为C2H4O2;结构式为;结构简式为CH3COOH;
②由结构简式可知,乙酸的官能团是羧基;
(2)乙酸又称醋酸或者冰醋酸,食醋中主要成分是乙酸,含有3%~5%的乙酸。
14. 溶液 1:3 I4O9+2H2O=HIO2+3HIO3 C 2+CH3CH2OH+4H+= 2Cr2O3+2CO2↑+5H2O PH试纸先变成蓝色,然后迅速变为无色 NaClO溶液水解成碱性,生成的HClO具有漂白性 Cl--2e-+2H2O=ClO2↑+4H+
【详解】
(1)①从常见配制方法可知,碘酒是碘的酒精溶液,碘酒属于溶液。②I4O9中碘元素的化合价为+3、+5价,碘酸根中I的化合价为+5价,碘酸根为−1价,则I4O9可写成Im(IO3)n形式,所以前面的I的化合价为+3价,则I4O9化学式为I(IO3)3, I4O9+3价和+5价的碘原子数目之比为1:3,若I4O9溶于水会生成两种含氧酸,则元素化合价不变,故生成的酸为HIO2和HIO3,该过程的化学方程式为:I4O9+2H2O=HIO2+3HIO3。
(2)①a. 将日常饮用的白酒直接蒸馏,会有少量水随酒精一起蒸馏出来,无法得到无水乙醇,加入新制的生石灰吸水再蒸馏可得到无水乙醇,故a错误;b. 医用酒精是75%的酒精,95%的酒精消毒杀菌效果比浓度为75%的酒精差,b错误;c. 表面氧化的铜丝在酒精灯内焰加热时会恢复红色,是因为氧化铜和焰心、内焰处乙醇发生氧化还原反应重新生成了铜,说明酒精具有挥发性和还原性,c正确;d.酒精是易燃物,封闭空间大面积喷洒酒精有易燃易爆的可能,这种做法极其危险,d错误;则说法正确的是c。
②酒驾的检测原理是:乙醇具有还原性,使酸化的K2Cr2O7橙色溶液迅速还原成绿色的Cr2O3,同时生成无色无味气体二氧化碳,该反应的离子方程式为:2+CH3CH2OH+4H+= 2Cr2O3+2CO2↑+5H2O。
(3)“84”消毒液的有效成分是NaClO,是一种强碱弱酸盐,若用PH试纸测量该种市售消毒液的p H,观察到的现象是p H试纸先变成蓝色,然后迅速变为无色,原因是NaClO溶液水解成碱性,生成的HClO具有漂白性。
(4) ClO2可利用电解饱和食盐水的方法制得,则氯元素化合价升高被氧化,在阳极上发生氧化反应,该电极反应方程式为:Cl--2e-+2H2O=ClO2↑+4H+。
15. 羧基 酸 CH3COOH
【分析】(1)根据阿司匹林的结构简式判断;
(2)石蕊遇酸变红;
(3)阿司匹林()分子中含有酯基,根据酯水解产物判断。
【详解】(1)阿司匹林的结构简式为,分子中的含氧官能团有酯基和羧基,故答案为:羧基;
(2)石蕊遇酸变红,向阿司匹林的水溶液中滴入2~3滴紫色石蕊溶液,溶液颜色变红,说明阿司匹林溶液具有酸性,故答案为:酸;
(3)阿司匹林()分子中含有酯基,在一定条件下水解生成水杨酸()和另一种酸A,则另一种酸A的结构简式应为CH3COOH,故答案为:CH3COOH。
16. ①和③ 、 ⑥和⑦ ①和⑤ D CH3CO18OH + CH3CH2OH CH3COOCH2CH3 +H218O 10 ml
【详解】(1)有相同质子数,不同中子数的原子或同一元素的不同核素互为同位素;①16O和③18O二者质子数相同,中子数不同,属于同一元素的不同原子,互为同位素,同理⑥ H 和⑦ D属于氢元素的同位素,①16O中中子数为8,⑤14C中中子数为8,二者中子数相等,答案为互为同位素是①和③,⑥和⑦;中子数相等的是①和⑤。
(2)①因为2SO2+O2⇌2SO3是可逆反应不能进行彻底,所以反应后18O 存在于所有含氧物质中,即存在于SO2、O2、SO3中,答案为D。
②根据乙酸与乙醇反应机理是乙酸脱羟基乙醇脱氢生成乙酸乙酯和水,即乙酸分子断裂C-18O单键,醇分子断裂O-H键,故18O原子到了水中,则CH3CO18OH与CH3CH2OH反应的化学方程式为:CH3CO18OH + CH3CH2OH CH3COOCH2CH3 +H218O,答案为CH3CO18OH + CH3CH2OH CH3COOCH2CH3 +H218O。
(3)D2O中质子数=2+8=10,n(D2O)==1ml,则质子的物质的量为10ml;答案为10ml。
17. CH3COOH+C2H5OHCH3COOC2H5+H2O 取代反应
【详解】乙酸和乙醇在浓硫酸加热条件下反应生成乙酸乙酯和水,其化学方程式CH3COOH+C2H5OHCH3COOC2H5+H2O。乙酸中羧基上的—OH被乙醇的—OC2H5取代,因此反应的类型是取代反应;故答案为:CH3COOH+C2H5OHCH3COOC2H5+H2O;取代反应。
18.(1)羟基、羧基
(2)+2Na+H2↑
(3)2+Na2CO32+CO2↑+H2O
【详解】(1)乳酸分子中含有羟基(—OH)和羧基(—COOH)两种官能团,答案:羟基、羧基;
(2)羟基和羧基都可以与金属钠发生反应,所以乳酸与金属钠反应的化学方程式为+2Na+H2↑,答案:+2Na+H2↑;
(3)乳酸含有的羧基可以与Na2CO3溶液反应,产生羧酸钠、CO2和水,反应的化学方程式为2+Na2CO32+CO2↑+H2O,答案:2+Na2CO32+CO2↑+H2O。
19.(1)羟基、羧基
(2)2∶1
(3)
(4)
(5) 加聚反应 AD
【详解】(1)根据乳酸的结构简式可知,其中含有的官能团名称为羟基、羧基。
(2)乳酸中的羟基、羧基都能和Na反应,乳酸中的羧基能与NaOH反应,则等物质的量的乳酸分别与Na、NaOH溶液反应,消耗的Na和NaOH的物质的量之比为2:1。
(3)乳酸中的羧基能电离出氢离子从而与Fe反应生成乳酸亚铁,化学方程式为。
(4)比乳酸少一个碳原子的同系物,则该同系物的结构与乳酸相似,也含有羟基和羧基,该同系物的结构简式为HOCH2COOH。
(5)丙烯酸中含有碳碳双键,可发生加聚反应生成聚丙烯酸。
A.丙烯酸与溴水发生加成反应使其褪色,与酸性高锰酸钾反应氧化反应使其褪色,两者的原理不同,A错误;
B.丙烯酸中含有羧基,能与新制氢氧化铜反应,B正确;
C.丙烯酸与水发生加成反应,生成的物质可能为HOCH2CH2COOH或CH3CH(OH)COOH,C正确;
D.丙烯酸和HCOOCH=CH2的结构简式不同,两者互为同分异构体而不是同种物质,D错误;
故答案选AD。
丙烯酸中碳碳双键发生加聚反应生成聚丙烯酸,则聚丙烯酸的结构简式为。
20.(1)HCOOH+2NaOH+2Cu(OH)2Na2CO3+Cu2O↓+4H2O
(2)HOCH2CH2OH+HOOCCOOH+2H2O
(3)HOCH2CH2CH2COOH+H2O
(4)
(5)n CH2=CHCOOCH3
(6)
(7)+ 5NaOHCH3COONa+C2H5OH+ 3H2O+
【详解】(1)甲酸与新制氢氧化铜悬浊液受热,既要考虑甲酸的酸性还要考虑甲酸中的醛基,以及悬浊液中过量的NaOH对反应的影响,发生反应的化学方程式为HCOOH+2NaOH+2Cu(OH)2Na2CO3+Cu2O↓+4H2O;故答案为HCOOH+2NaOH+2Cu(OH)2Na2CO3+Cu2O↓+4H2O。
(2)乙二酸和乙二醇在浓硫酸的催化作用下,通过酯化生成六元环酯,此反应的化学方程式为HOCH2CH2OH+HOOCCOOH+2H2O;故答案为
(3)HOCH2CH2CH2COOH在浓硫酸加热条件下分子内酯化成环的反应方程式为HOCH2CH2CH2COOH+H2O;故答案为HOCH2CH2CH2COOH+H2O。
(4)1分子咖啡与2分子CH3COCl在一定条件下酚与酰氯之间发生取代反应,发生反应生成酯的方程式为;故答案为。
(5)丙烯酸甲酯中含有碳碳双键,可发生类似乙烯的加聚反应,此反应的化学方程式为n CH2=CHCOOCH3;故答案为n CH2=CHCOOCH3。
(6)分子内有醛基,可发生银镜反应,化学方程式为;故答案为。
(7)与足量NaOH溶液共热时可发生酯的水解、羧酸的中和及酚与NaOH的中和等,反应的化学方程式为+ 5NaOHCH3COONa+C2H5OH+ 3H2O+。故答案为+ 5NaOHCH3COONa+C2H5OH+ 3H2O+。
21.错误
【详解】乙酸乙酯的制备需要用浓硫酸作催化剂和吸水剂,2ml/L的硫酸是稀硫酸,故错误。
22.错误
【解析】略
23.错误
【详解】医用酒精的浓度通常是75%。95%的酒精吸收病毒蛋白质中的水分的速度快,会使病毒蛋白质在短时间之内迅速凝固,如此一来,就相当于给病毒建立了一层保护膜,隔绝了酒精的进入。故错误。
24.错误
【详解】体积分数为75%的乙醇溶液常作消毒剂,错误。
25.错误
【详解】乙酸能和氢氧化钠反应,错误。
26. 重结晶 冷凝回流乙醇和水 水浴加热 吸水剂由白色变为蓝色 蒸馏 分液漏斗 降低苯甲酸乙酯的溶解度利于分层 或
【分析】①苯甲酸、乙醇(过量)以及浓硫酸,混合均匀并加入沸石,按图示装好仪器,控制温度在65~70℃加热回流2h。②操作1是蒸馏出乙醇来,使油层尽量回到圆底烧瓶中,③加入冷水,分批加入Na2CO3至溶液呈中性,④用分液漏斗分出有机层,水层用25mL乙醚萃取分液,然后合并至有机层,加入氯化钙等干燥剂,对粗产物进行纯化。
【详解】(1)可通过重结晶的方式提高原料苯甲酸的纯度。故答案为:重结晶;
(2)仪器A为球形冷凝管,在制备过程中乙醇易挥发,因此通过球形冷凝管冷凝回流乙醇和水;该反应中乙醇作为反应物,因此可通过水浴加热控制温度,避免乙醇大量挥发。故答案为:冷凝回流乙醇和水;水浴加热;
(3)仪器B中吸水剂为无水硫酸铜的乙醇饱和溶液,吸收水分后生成五水硫酸铜,吸水剂由白色变为蓝色。故答案为:吸水剂由白色变为蓝色;
(4)乙醇沸点和苯甲酸、苯甲酸乙酯沸点差异较大,操作Ⅰ为蒸馏;操作Ⅱ为分液,除烧杯外,还需要的玻璃仪器为分液漏斗。故答案为:蒸馏;分液漏斗;
(5)因苯甲酸乙酯难溶于冷水,步骤③中将反应液倒入冷水还可降低苯甲酸乙酯的溶解度有利于分层;试剂X为(或)。故答案为:降低苯甲酸乙酯的溶解度利于分层;(或)。
【点睛】本题考查苯甲酸乙酯的合成,侧重物质制备实验及有机物性质的考查,把握合成反应及实验装置的作用为解答的关键,综合考查学生实验技能和分析解答问题的能力,难点突破,注意信息的处理及表格中信息的应用。
27.(1) 催化剂 吸水剂
(2) 球形干燥管(或干燥管) 防倒吸 冷凝乙酸乙酯 红色变浅或褪去且出现分层现象
(3)
(4)64.3%
【详解】(1)浓硫酸作用是:催化剂和吸水剂;
(2)仪器C为球形干燥管(或干燥管),乙酸、乙醇易溶于碳酸钠溶液,会导致装置内气体减少,球形干燥管的管口伸入液面以下会发生倒吸,但球形干燥管体积大,可冷凝乙酸乙酯,也可以防止倒吸,故球形干燥管的作用为防倒吸和冷凝乙酸乙酯;碳酸钠溶液显碱性,遇到酚酞变红,实验完毕后,将烧杯D中的溶液充分振荡、静置,乙酸和碳酸钠反应而使溶液红色变浅,乙酸乙酯不溶于饱和碳酸钠溶液,密度比水小,溶液分层,上层为无色油状液体,故现象为:红色变浅或褪去且出现分层现象;
(3)羧酸与醇发生的酯化反应中,羧酸中的羧基提供—OH,醇中的羟基提供—H,相互结合生成水,其他基团相互结合生成酯,同时该反应可逆,反应的化学方程式为;
(4)3.00mL乙醇的物质的量为:,乙酸的物质的量为:,乙醇过量,乙酸乙酯的理论产量为:0.035ml,实际产生的乙酸乙酯的物质的量为:,乙酸乙酯的理论产率为:。
28. 碳碳双键 羧基 CH3CHO CH3CH2OH+CH3COOHCH3COOC2H5+H2O 取代反应、/酯化反应 CH2=CH2+HClCH3CH2Cl 2CH3COOH+Na2CO3→2CH3COONa+H2O+CO2↑ 饱和碳酸钠溶液 分液漏斗
【分析】A是石油裂解气的主要产物之一,其产量常用于衡量一个国家石油化工发展水平的标志,A是乙烯,乙烯和氯化氢发生加成反应得到F,F是氯乙烷;A和水在催化剂的条件下反应得到乙醇,B是乙醇,乙醇在铜作催化剂加热的条件下反应制得C,C是乙醛,乙醇被高锰酸钾氧化成乙酸,D是乙酸,乙酸和乙醇在浓硫酸和加热的条件下反应制得乙酸乙酯,E为乙酸乙酯,A可以转化为G,G可能为聚乙烯,据此分析。
【详解】(1)根据分析可知,A是乙烯,结构简式为:CH2=CH2,官能团的名称是碳碳双键;D是乙酸,结构简式为:CH3COOH,官能团名称是羧基;C是乙醛,C结构简式:CH3CHO;
(2)B是一种具有特殊香味的液体,是乙醇,B→E是乙酸和乙醇发生酯化反应制得乙酸乙酯和水的反应,酸失去羟基醇失去羟基上的氢原子,化学反应方程式为:CH3CH2OH+CH3COOHCH3COOC2H5+H2O,该反应类型是取代反应,酯化反应;
(3)物质F是氯乙烷,由A制F是乙烯和氯化氢发生加成反应,化学反应方程式为:CH2=CH2+HClCH3CH2Cl,由氯乙烯可以制取某种高分子化合物,为聚氯乙烯,聚氯乙烯的结构简式为:;
(4)①实验结束后,试管甲中液体分层,上层液体含有乙酸乙酯、挥发出的乙醇和乙酸,振荡试管甲,有无色气泡生成,其主要原因是碳酸钠和乙酸反应制得乙酸钠和二氧化碳和水,化学方程式为:2CH3COOH+Na2CO3→2CH3COONa+H2O+CO2↑;
②除去乙酸乙酯中混有的少量乙酸和乙醇,应加入饱和碳酸钠溶液,可以溶解乙醇,中和乙酸,降低乙酸乙酯的溶解度,乙酸乙酯层和水层不互溶,要分离时需要分液,分液时用到的主要仪器是分液漏斗。
【点睛】乙酸和乙醇生成乙酸乙酯的反应是酸失去羟基,醇失去羟基上的氢原子,属于酯化反应,也属于取代反应,为易错点。
人教版 (2019)必修 第二册第三节 乙醇与乙酸课后作业题: 这是一份人教版 (2019)必修 第二册<a href="/hx/tb_c4000048_t7/?tag_id=28" target="_blank">第三节 乙醇与乙酸课后作业题</a>,共16页。试卷主要包含了3 乙醇与乙酸 同步训练,1ml乙醇与足量钠反应生成0等内容,欢迎下载使用。
人教版 (2019)必修 第二册第三节 乙醇与乙酸课后复习题: 这是一份人教版 (2019)必修 第二册第三节 乙醇与乙酸课后复习题,共13页。试卷主要包含了单选题,填空题,实验题等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第二册第三节 乙醇与乙酸课后作业题: 这是一份高中化学人教版 (2019)必修 第二册第三节 乙醇与乙酸课后作业题,共11页。试卷主要包含了单选题,填空题,实验题等内容,欢迎下载使用。













