






2024年中考化学精讲课件---专项突破6 酸、碱、盐反应的图象分析
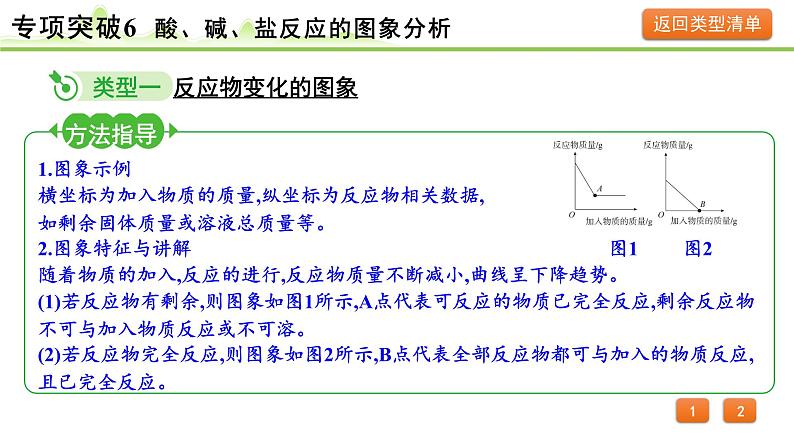
展开1.图象示例横坐标为加入物质的质量,纵坐标为反应物相关数据,如剩余固体质量或溶液总质量等。2.图象特征与讲解 图1 图2随着物质的加入,反应的进行,反应物质量不断减小,曲线呈下降趋势。(1)若反应物有剩余,则图象如图1所示,A点代表可反应的物质已完全反应,剩余反应物不可与加入物质反应或不可溶。(2)若反应物完全反应,则图象如图2所示,B点代表全部反应物都可与加入的物质反应,且已完全反应。
1.向盛有一定量铜和CaCO3混合物的烧杯中滴加稀盐酸,边滴边搅拌,反应过程中剩余固体的质量与加入稀盐酸的质量关系如图1所示。下列说法不正确的是( )A.M点时,剩余固体是铜和CaCO3 B.M、N点时,溶液中的溶质均只有CaCl2C.混合物中铜的质量为(a-b)gD.P点时,溶液中的溶质有两种 图1
2.实验室有一包白色固体,其中除了Na2CO3以外,还可能含有Ba(NO3) 2、Na2SO4、NaOH中的一种或几种。步骤① 取少量白色固体于烧杯中,向烧杯中加入足量水并不断搅拌,固体部分溶解。步骤② 接着向烧杯中加入足量稀硝酸并不断搅拌,此时固体质量变化如图2所示。下列说法正确的是( ) 图2A.A→B段对应的实验现象是固体全部溶解,有无色气泡冒出B.原白色固体中一定含有Na2CO3、Na2SO4、Ba(NO3) 2、NaOHC.C→D段对应溶液pH逐渐变大D.D点对应溶液中只含有两种溶质
1.图象示例横坐标为加入物质的质量,纵坐标为生成物相关数据,如沉淀或气体的质量、溶液总质量等。
图3 图4
2.图象特征与讲解(1)若只发生一步反应,则图象如左图所示,则随着反应的进行,生成物的质量不断增大,曲线呈上升趋势;当到达D点完全反应后,生成物的质量达到最大,不再发生变化。(2)若发生两个及以上反应,则图象如右图所示。E点之前为先发生的反应,E~F阶段为后发生的反应,F点之后反应完全进行,生成物质量达到最大,不再发生变化。3.多个反应的一般反应顺序(1)向盐和酸的溶液中加入碱,酸和碱的反应一般优先于该酸与盐的反应。(2)向可溶性钙盐或钡盐中加入可溶性碳酸盐,产生气体的反应优先,生成沉淀的反应在后。
3.向氯化镁和稀盐酸的混合溶液中滴加pH=12的氢氧化钠溶液,加入氢氧化钠溶液的质量与生成沉淀的质量关系如图5所示。下列说法错误的是 ( )A.O~a对应的溶液中溶剂质量不断增大B.a~b(b点除外)对应的溶液中溶质为NaCl和MgCl2C.b点对应溶液中含有的氯化钠的质量大于a点 图5D.c点对应溶液的pH=12
4.将某氢氧化钠溶液逐滴滴入硫酸和硫酸铜的混合溶液中,直至过量。根据实验事实绘制如图6所示曲线。其中说法错误的是( )A.b~c段有蓝色沉淀生成B.a~d段硫酸钠质量不断增大C.c~d段,溶液pH不断增大D.c点比a点所含的溶质种类少 图6
1.图象示例横坐标为加入物质的质量,纵坐标为溶液的pH。2.图象特征与讲解以向酸和盐的混合溶液中加入碱为例,发生两个及以上反应,图象如图7所示。 图7G点之前为先发生的反应,随着酸碱中和反应的进行,pH逐渐接近于7;G~H阶段为后发生的反应,盐与碱反应过程中pH=7;H点完全反应,之后碱过量,溶液pH逐渐大于7。
5.图象能直观反应有关信息。向一定质量CaCl2和HCl的混合溶液中逐滴加入Na2CO3溶液,并振荡,测得混合溶液的pH随着碳酸钠溶液体积的变化情况如图8所示,下列分析正确的是 ( )A.d~m段反应过程中有沉淀产生B.m点时溶液中的溶质只有CaCl2C.m~n段反应过程中有气泡产生D.n点时溶液中的溶质只有NaCl 图8
6.现有HCl与CaCl2的混合溶液,向其中逐滴滴入过量的某物质X,溶液的pH随滴入X的量的变化关系如图所示,则X可能是( ) 图9A.氯化钡溶液 B.澄清石灰水 C.纯碱溶液D.稀盐酸
1.图象示例 横坐标为时间,纵 横坐标为时间,纵坐标为生成物质量 坐标为反应物质量 图10 图11
2.归纳总结在进行酸、碱、盐反应的图象分析时,首先要注意横、纵坐标表示何种变量,然后分析相关变化过程,最后判断各量之间的变化关系是否与图象符合。关键在于三个方面:三点(起点、转折点、终点),曲线的变化趋势及横、纵坐标的比例关系(涉及计算)。
7.将一定量的Zn粉加入一定量的AgNO3和Fe(NO3)2的混合溶液中,得到的固体质量随时间的变化关系如图12所示。下列说法不正确的是 ( )A.当反应进行到t时,所得金属固体中的物质至少有两种 图12B.当反应进行到t时,取反应后的滤液滴加稀盐酸,有白色沉淀产生C.当反应进行到t时,此时取滤渣滴加稀盐酸,一定有气泡产生D.当反应进行到t时,取反应后的滤液观察,滤液呈浅绿色
中考化学复习---酸、碱、盐课件PPT: 这是一份中考化学复习---酸、碱、盐课件PPT,共11页。PPT课件主要包含了酸的化学性质5,碱的化学性质4,盐的化学性质4,复分解反应,溶解沉淀表等内容,欢迎下载使用。
人教版中考化学复习重难突破14酸、碱、盐之间的分段反应练习课件: 这是一份人教版中考化学复习重难突破14酸、碱、盐之间的分段反应练习课件,共16页。
【备战2023】中考化学一轮复习:第9讲《常见酸、碱、盐》课件: 这是一份【备战2023】中考化学一轮复习:第9讲《常见酸、碱、盐》课件,共60页。PPT课件主要包含了导图巧记忆,热点考点,重要考点,一般考点,不变色,中和反应,浓硫酸,苛性钠,熟石灰,消石灰等内容,欢迎下载使用。












