

宜宾市叙州区第二中学校2022-2023学年高一下学期3月月考化学试卷(含答案)
展开
这是一份宜宾市叙州区第二中学校2022-2023学年高一下学期3月月考化学试卷(含答案),共11页。试卷主要包含了单选题,实验题,填空题等内容,欢迎下载使用。
一、单选题
1.下列有关物质的性质和该性质的应用均正确的是( )
A.浓硫酸具有吸水性,可用于干燥氨气、二氧化碳等气体
B.二氧化硫具有漂白性,可用于加工食品使食品增白
C.铝具有良好的导电性,钢抗拉强度大,钢芯铝绞线可用作远距离高压输电线材料
D.铜的金属活动性比铁弱,可用铜罐代替铁罐贮运浓硝酸
2.下列物质中,既含有离子键又含有非极性共价键的是( )
A.HClOB.C.D.
3.2016年IUPAC将117号元素命名为Ts(中文名“石田”,tián),Ts的原子核外最外层电子数是7。下列说法错误的是( )
A.Ts与F同主族B.Ts的最外层p轨道中有5个电子
C.在同族元素中Ts金属性最强D.中子数为176的Ts符号是
4.下列化学用语书写正确的是( )
A.氯原子的结构示意图:B.含有6个中子的碳核素:
C.氯化钠的电子式:NaD.臭氧的化学式:
5.铯是制造光电管的主要材料,铯元素的部分信息如图所示。下列关于铯的说法中,不正确的是( )
A.原子序数为55B.属于ⅠA族元素
C.金属性比钠弱D.相对原子质量是132.9
6.下列有关化学用语表示正确的是( )
A.的电子式:
B.的结构示意图:
C.质子数为92、中子数为146的U原子:
D.的电子式:
7.下表是元素周期表的一部分,①~⑥代表6种短周期主族元素,已知③与氢元素能组成日常生活中常见的化合物。
下列说法正确的是( )
A.①~⑥中原子半径最大的是④B.②的最高化合价为+4
C.④的金属性比⑤的金属性弱D.⑥的最高价氧化物对应水化物是弱酸
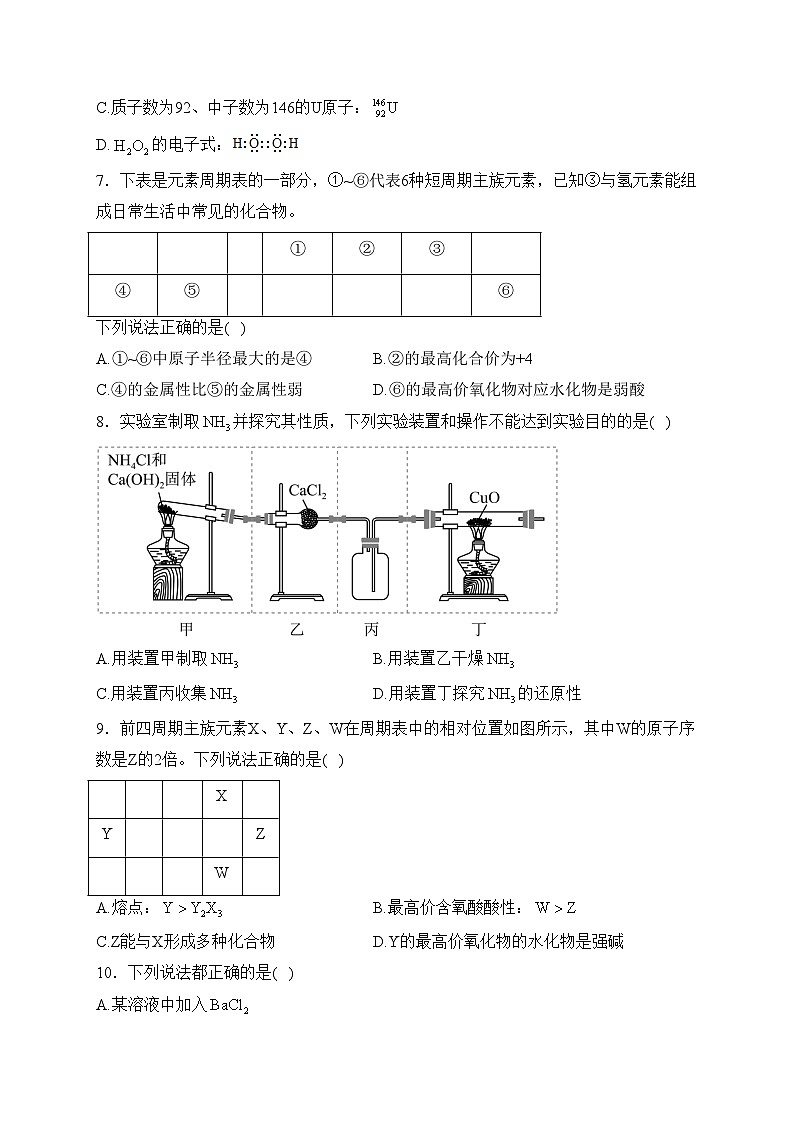
8.实验室制取并探究其性质,下列实验装置和操作不能达到实验目的的是( )
A.用装置甲制取B.用装置乙干燥
C.用装置丙收集D.用装置丁探究的还原性
9.前四周期主族元素X、Y、Z、W在周期表中的相对位置如图所示,其中W的原子序数是Z的2倍。下列说法正确的是( )
A.熔点:B.最高价含氧酸酸性:
C.Z能与X形成多种化合物D.Y的最高价氧化物的水化物是强碱
10.下列说法都正确的是( )
A.某溶液中加入溶液,有白色沉淀生成,再加入稀盐酸沉淀不溶解,说明原溶液中一定含
B.将含有杂质的气体,缓慢通过足量的高锰酸钾溶液,再通过浓硫酸干燥,可获得较纯净的气体
C.某钠盐(含、中的一种或两种)试样0.168g,将其灼烧,冷却,并用托盘天平称量残留固体的质量,根据质量是否变化,可确定样品的组成
D.铝热反应可生成铁,工业上可大量利用该反应来生产铁
11.将一定量的通入溶液中,无明显现象,当加入(或通入)某试剂(或气体)X后有沉淀生成。此试剂(或气体)X可能是:①溶液;②氨水;③NaOH溶液;④;⑤;⑥新制氯水( )
A.①②③⑥B.①③⑤C.②③⑤⑥D.①③④
12.中药材铁华粉的主要成分是,其检测流程如图所示。下列说法正确的是( )
A.刺激性气体X为
B.铁华粉中可能含有铁单质
C.向滤液中滴加酸性溶液,一定能证明具有还原性
D.滤液中加入试液,产生蓝色沉淀说明溶液中含有
13.短周期主族元素原子半径与原子序数的关系如图,下列有关说法错误的是( )
A.E的一种氧化物和A的单质在高温下能反应
B.氢化物的沸点:
C.D的简单离子半径是同周期元素形成简单离子半径中最小的
D.G的单质存在于火山喷口附近或地壳的岩层里
14.实验室用(沸点33.0℃)与过量在1100℃下反应制得纯硅,制备纯硅的装置如图所示(夹持及加热装置略去),已知:能与剧烈反应,在空气中易自燃,下列说法错误的是( )
A.装置B中的试剂是浓硫酸,目的是除去氢气中的水蒸气
B.装置C中的烧瓶需要加热,其目的是使滴入烧瓶中的气化
C.实验时石英管用酒精灯外焰加热
D.为保证制备纯硅实验的成功,操作的关键是排尽装置中的空气以及控制好反应温度
15.把铝粉和某铁的氧化物()粉末配成铝热剂,分成两等份。一份在高温下恰好完全反应后,再与足量盐酸反应;另一份直接放入足量的烧碱溶液中充分反应。前后两种情况下生成的气体质量比是5:7,则x:y为( )
A.1:1B.1:2C.5:7D.7:5
二、实验题
16.工业上在一定条件下可用将还原,减少二氧化氮的污染。某同学在实验室对该反应进行了模拟,实验设计如下图所示(部分夹持装置省略):
(1)用装置A制备,其中发生反应的化学方程式是_______。
(2)装置B内的干燥剂是_______。
(3)装置D中发生反应的离子方程式是_______;铜丝设计为可抽动的目的_______。
(4)M装置可将与转化为环境友好的气体,其反应化学方程式是_______。
17.根据要求完成下列实验过程(a、b为弹簧夹,加热及固定装置已略去)
(1)验证碳、硅非金属性的相对强弱(已知酸性:亚硫酸>碳酸)。
①实验步骤为:连接仪器、___________、加药品后,打开a、关闭b,然后滴入酸,加热。
②装置A中试剂是___________。
③能说明碳的非金属性比硅强的实验现象是___________。
(2)验证的氧化性、还原性和酸性氧化物的通性:在(1)①操作后打开b,关闭a。
①假设只有少量通入NaOH溶液中,发生反应的化学方程式为___________。
②溶液变浑浊,证明具有___________(填“氧化性”或“还原性”)。
③溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
(3)实验中,取一定质量的铜片和一定体积的浓硫酸放在圆底烧瓶中共热,直到反应完全,发现圆底烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的剩余。
①有一定量的余酸但未能使铜片完全溶解,你认为原因是___________。
②下列药品中能用来证明反应结束后的圆底烧瓶中存在余酸的是___________(填字母)。
A.银粉B.溶液C.铁粉D.溶液
三、填空题
18.有V、W、X、Y、Z五种元素,它们的核电荷数依次增大,且都小于20。其中只有X、Z是金属元素;V元素的一种核素原子核内无中子,Z元素原子的最外层只有一个电子;W和Y元素原子的最外层电子数相同,且W元素原子L层电子数是K层电子数的3倍;X元素原子的最外层电子数是Y元素原子最外层电子数的一半。回答下列问题:
(1)V的一种核素中质子数为中子数的1/2,则该核素的名称为_______,是制造_______的原料。
(2)W元素的原子结构示意图为________。
(3)X元素的离子结构示意图为________。
(4)Y的单质在加热条件下与铁反应的化学方程式为______。
(5)Z的元素符号为________。
19.下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
回答下列问题:
(1)由c、d、e三元素形成的化合物中含有的化学键类型为_______。
(2)元素e、f的最高价氧化物对应水化物之间能发生反应,其离子方程式为_______。
(3)下列能证明非金属性的是_______。
a.简单气态氢化物的沸点
b.简单气态氢化物水溶液的酸性
c.单质分别与铜反应,h得到铜的高价态化合物,g得到铜的低价态化合物
d.简单气态氢化物还原性
(4)元素i(Se)是人体必需的微量元素,h和i的最高价氧化物对应水化物的酸性由强到弱的顺序_______(用化学式表示)。与足量e的最高价氧化物的水化物反应的化学方程式为_______。
(5)可与c的简单气态氢化物反应得到单质Se,反应的化学方程式是_______。
20.铝氢化钠()是重要的还原剂。以铝土矿(主要成分,含少量、等杂质)为原料制备的一种流程如图:
已知:碱浸中转化成难溶的
(1)用氧化物的形式表示为______________(x用具体的数值表示)。
(2)过滤1得滤液的主要成分为NaOH和,写出反应1中与反应的离子方程式:______________。
(3)电解2生成和NaOH用于循环使用,写出电解2阴极的电极反应式:___________。
(4)反应3的化学方程式为___________。
(5)铝氢化钠遇水发生剧烈反应产生大量气泡,其反应的化学方程式为___________。
(6)滤渣主要成分有和,可以采用如图流程进行分离:
①滤渣溶于盐酸所得的固体物质可能为___________(填化学式)。
②滤渣溶于盐酸的“酸浸率”与温度关系如图所示,试解释温度过高,“酸浸率”降低的原因___________。
参考答案
1.答案:C
解析:
2.答案:C
解析:
3.答案:D
解析:
4.答案:D
解析:
5.答案:C
解析:
6.答案:A
解析:
7.答案:A
解析:根据上述分析可知:①是C元素,②是N元素,③是O元素,④是Na元素,⑤是Mg元素,⑥是Cl元素;
A.不同周期元素,原子核外电子层数越多,原子半径越大;同一周期元素,原子序数越大,原子半径就越小,所以①~⑥中原子半径最大的是④号元素Na元素,故A正确;
B.②是N元素,N原子最外层有5个电子,其最高化合价为+5价,故B错误;
C.同一周期元素,原子序数越大,原子半径就越小,该原子失去电子的能力就越弱,元素的金属性逐渐减弱,则④的金属性比⑤的金属性强,故C错误;
D.⑥是Cl元素,Cl元素的最高价氧化物对应水化物是强酸,故D错误;
故选:A。
8.答案:B
解析:
9.答案:C
解析:
10.答案:B
解析:
11.答案:C
解析:
12.答案:B
解析:
13.答案:B
解析:
14.答案:C
解析:
15.答案:B
解析:
16.答案:(1)
(2)碱石灰
(3);可以通过抽动铜丝控制反应的发生和停止
(4)
解析:
17.答案:(1)检验装置气密性;高锰酸钾溶液;A中高锰酸钾不褪色,硅酸钠溶液中有白色沉淀生成
(2);氧化性;;
(3)反应过程中浓硫酸被消耗同时生成水,浓硫酸逐渐变稀,而铜不与稀硫酸反应;CD
解析:
18.答案:(1)氚;氢弹
(2)
(3)
(4)
(5)K
解析:
19.答案:(1)共价键、离子键
(2)
(3)cd
(4);
(5)
解析:
20.答案:(1)
(2)
(3)(或)
(4)
(5)
(6);温度过高,盐酸挥发损失,从而使“酸浸率”降低
解析:
55Cs
铯
132.9
①
②
③
④
⑤
⑥
X
Y
Z
W
滴加的溶液
氯水
氨水
沉淀的化学式
_____
_____
相关试卷
这是一份四川省宜宾市叙州区第二中学校2022-2023学年高一下学期开学考试化学试卷(含答案),共20页。试卷主要包含了单选题,填空题,实验题,推断题等内容,欢迎下载使用。
这是一份四川省宜宾市叙州区第二中学校2022-2023学年高二下学期开学考试化学试卷(含答案),共16页。试卷主要包含了单选题,填空题,实验题等内容,欢迎下载使用。
这是一份四川省宜宾市叙州区第二中学校2023-2024学年高一上学期12月第三学月考试化学试题含答案,共7页。试卷主要包含了5 Si,200ml/LKCl溶液,4L,2LH2O含有的分子数为0等内容,欢迎下载使用。








