

2024年九省新高考第二次模拟考试卷:化学(新九省高考“15+4模式”)(考试版A4)
展开
这是一份2024年九省新高考第二次模拟考试卷:化学(新九省高考“15+4模式”)(考试版A4),共11页。
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回
可能用到的相对原子质量:H 1 N 14 O 16 Na 23 S 32 Cl 35.5 Fe 56 Mn 55 Zn 65 Ni 59
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.《后汉书·蔡伦传》中记载:“自古书契多编以竹简,其用缣帛者,谓之纸。缣贵而简重,不便于人,伦乃造意用树肤,麻头及弊布、渔网以为纸。”下列叙述错误的是
A.“缣帛”是丝质品,其主要成分为蛋白质
B.“树肤”与“麻头”的主要成分属于糖类
C.造纸过程中可以采用过氧化氢漂白纸浆
D.现代渔网的主要成分是尼龙,属于纤维素
2.某分子的片段如图所示。下列关于该片段的说法不正确的是
A.该片段结构最多与发生加成
B.胸腺嘧啶与酸或碱溶液加热条件下均可以反应
C.分子可通过氢键①②形成双螺旋结构
D.该片段能使溴水和酸性高锰酸钾溶液褪色
3.催化剂能催化脱除烟气中的,反应为。下列说法正确的是
A.的电子式:
B.的模型名称:直线型
C.的价电子排布图为:
D.是极性键构成的非极性分子
4.下列关于物质的性质、用途等描述中不正确的是
A.SO2具有还原性,并且可以杀菌、抗氧化,在葡萄酒中添加适量的SO2能杀灭微生物并防止葡萄酒的氧化变质
B.高铁酸钾在水处理过程中涉及的变化过程有:氧化还原反应、蛋白质变性、盐类水解、胶体聚沉等
C.储氢合金是一类能大量吸收H2,并与H2结合成金属氢化物的材料
D.液氨作为清洁能源的反应原理是
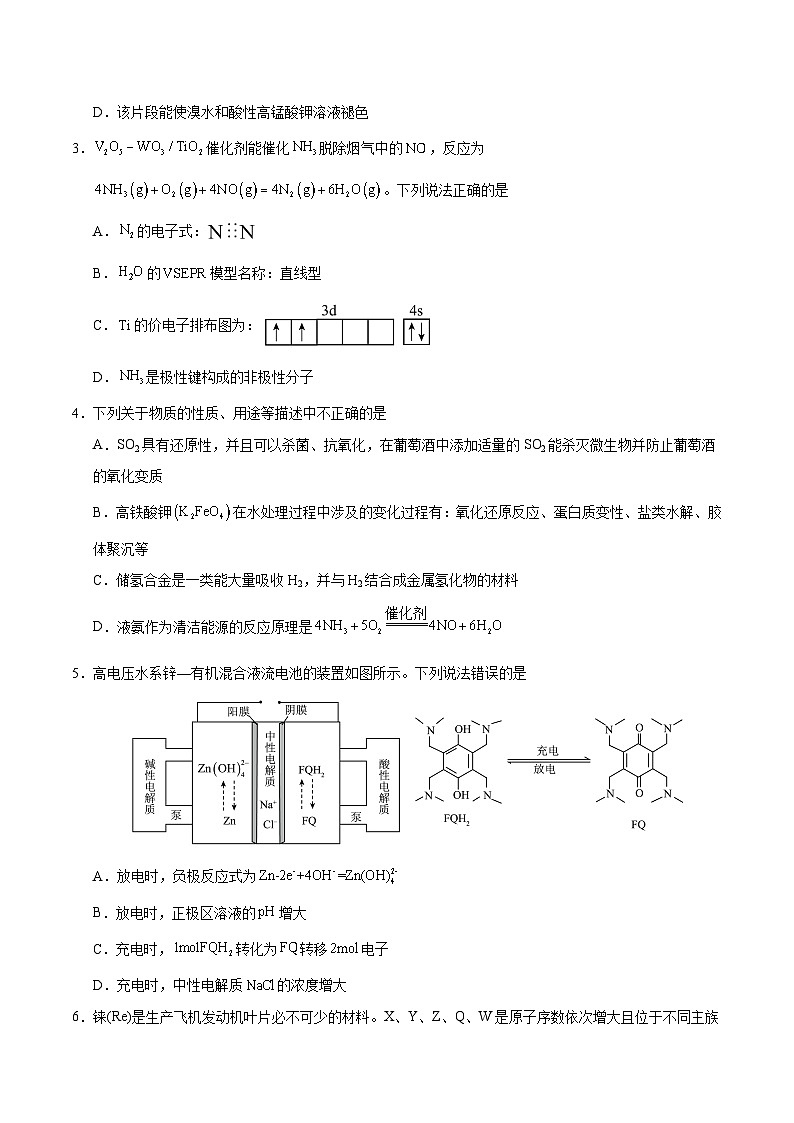
5.高电压水系锌—有机混合液流电池的装置如图所示。下列说法错误的是
A.放电时,负极反应式为
B.放电时,正极区溶液的增大
C.充电时,转化为转移电子
D.充电时,中性电解质的浓度增大
6.铼(Re)是生产飞机发动机叶片必不可少的材料。X、Y、Z、Q、W是原子序数依次增大且位于不同主族的短周期元素,其中X、Y、Z三种元素可与铼元素组成一种化合物(结构如图),该化合物与X的单质反应可得到铼。Q是地壳中含量最丰富的金属元素,Z与W形成的化合物为共价晶体。下列说法不正确的是
A.元素第一电离能:
B.图中的阳离子与互为等电子体,具有相同的空间结构
C.Q的最高价氧化物对应水化物可以和强碱反应
D.熔点:W晶体小于W、Y形成的晶体
7.碳元素及其化合物在自然界广泛存在且具有重要应用。、、是碳元素的3种核素,碳元素不仅可以形成金刚石等单质,还能形成、、、、HCOONa、等重要化合物。具有较大的燃烧热(890.3 ),是常见燃料。用NaOH溶液吸收生成溶液是“固定”再利用的方法之一、电解溶液可获得;向溶液中加入铁粉,反应初期产生并生成,迅速转化为活性,活性催化加氢生成。“侯氏制碱法”是以、、NaCl为原料制备。下列化学反应表示正确的是
A.甲烷的燃烧:
B.铁粉和溶液反应制:
C.通入氨的饱和食盐水中:
D.催化电解生成的阳极反应式:
8.碳元素及其化合物在自然界广泛存在且具有重要应用。、、是碳元素的3种核素,碳元素不仅可以形成金刚石等单质,还能形成、、、、HCOONa、等重要化合物。具有较大的燃烧热(890.3 ),是常见燃料。用NaOH溶液吸收生成溶液是“固定”再利用的方法之一、电解溶液可获得;向溶液中加入铁粉,反应初期产生并生成,迅速转化为活性,活性催化加氢生成。“侯氏制碱法”是以、、NaCl为原料制备。活性催化加氢生成的总反应为:,可能的反应历程如下图所示。下列说法正确的是
A.的空间构型是三角锥形
B.该总反应为置换反应
C.步骤Ⅰ中吸附在Fe上的H与C结合
D.反应中消耗11.2 mL 转移电子0.001ml
9.一种以CH3OH、CO、HI作原料合成乙酸的催化机理如图所示。下列说法错误的是
A.是反应的催化剂
B.该过程中有非极性键的形成
C.含Rh物质参与反应历程中的每个步骤
D.总反应的化学方程式为CH3OH+COCH3COOH
10.利用如下流程可从废光盘的金属层中回收其中的银(金属层中其他金属含量过低,对实验影响可忽略):
已知:溶液在加热时易分解产生和;“溶解”工序发生的反应为可逆反应。下列说法错误的是
A.“氧化”时,适宜选择水浴加热方式
B.若省略第一次过滤,会使氨水的用量增加
C.滤渣Ⅱ洗涤后的滤液可送入“还原”工序利用
D.“还原”时,每生成,理论上消耗
11.下列说法不正确的是
A.装置甲可以用于探究铁与水蒸气反应,并点燃肥皂泡检验氢气
B.图乙用(杯酚)识别和,操作①②为过滤,操作③为蒸馏
C.装置丙可用于实验室配制银氨溶液
D.装置丁中若将溶液替换成溶液,仍然形成原电池
12.二氧化氯(ClO2)为新型绿色消毒剂,沸点为9.9℃,可溶于水,有毒,浓度较高时易发生爆炸。用CH3OH和NaClO3在硫酸催化作用下反应可制得ClO2。利用ClO2与H2O2在碱性条件下制备少量NaClO2的实验装置如图所示。
下列说法正确的是
A.为配制分液漏斗中的混合液,应将甲醇溶液倒入浓硫酸中搅拌
B.若装置甲烧瓶内氧化产物为HCOOH,则氧化剂与还原剂的物质的量之比为4:1
C.实验中通入气体的速率应尽可能慢
D.装置乙中应使用热水浴,以加快反应速率
13.某反应的速率方程为。其中,k为速率常数。已知其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为0.8/k。改变反应物浓度时,反应的瞬时速率如表所示,下列说法不正确的是
A.上述表格中的、
B.该反应的速率常数
C.升温、加入催化剂均可使k增大,反应瞬时速率加快
D.在过量的B存在时,当剩余6.25%的A时,所需的时间是375min
14.下列实验过程可以达到实验目的的是
15.溶液滴定溶液时,、各含磷元素微粒的和的关系如图。下列说法中正确的是
A.①为的与的关系
B.b点时,溶液中
C.的
D.d点时,溶液中存在着
二、非选择题:本题共4小题,共55分。
16.(12分)纳米铁酸锰(,具有磁性)在光、电子、催化等领域应用广泛。实验室可采用共沉淀法制备纳米铁酸锰,步骤如下:
步骤1:按,称取和于烧杯中,加入200mL的蒸馏水,搅拌,形成混合溶液;
步骤2:配制浓度为的NaOH溶液,并加热至沸腾;
步骤3:将步骤1的混合液加热至80℃,剧烈搅拌下于10s内加入沸腾的130mL的NaOH溶液中,然后将该溶液倒入仪器X中回流,于90℃恒温晶化1h;
步骤4:反应结束后,将铁酸锰晶体粒子分离出来,依次用蒸馏水、乙醇洗涤干燥后,即得到黑色具有磁性的铁锰酸。
回答下列问题:
(1)步骤2所配NaOH溶液的物质的量浓度为 。配制过程中,下列仪器不需要用到的是 (填字母)。
(2)步骤3回流装置如图所示,其中夹持仪器和加热装置均省略。
①仪器X的名称为 。
②回流时的加热方式为 。
③写出形成铁酸锰反应的离子方程式: 。
(3)步骤4分离出铁酸锰的简单方法是 ,检验蒸馏水将铁酸锰洗涤干净的操作是 ,乙醇洗涤的目的是 。
17.(16分)草酸镍是一种不溶于水的浅绿色粉末,常用于制镍催化剂和镍粉等。以铜镍合金废料(主要成分为镍和铜,含有一定量的铁和硅)为原料生产草酸镍的工艺流程如图:
已知:①“浸出”液含有的离子主要有;
②增大,被氧化的速率加快,同时生成的水解形成更多的胶体能吸附。
③草酸的
回答下列问题:
(1)生产时为提高合金废料浸出率,常采取的措施有 (填字母)。
a.适当延长浸出时间 b.高温浸出 c.分批加入混酸浸取并搅拌
(2)“萃取”步骤中萃取除去的主要金属阳离子是 。
(3)“氧化”过程中,控制、pH小于3的条件下进行。
①的电子式为 。
②“氧化”过程的离子方程式为 。
③为3~4时,镍的回收率降低的原因是 。
(4)已知常温下,当溶液时,沉淀完全[时认为完全沉淀],则此时溶液中草酸的浓度 。
(5)在空气中加热二水合草酸镍得到如下热分解曲线如图所示,已知:指的是在程序控制温度下测量待测样品的质量与温度变化关系,指通过单独的加热器补偿样品在加热过程中发生的热量变化,以保持样品和参比物的温差为零。这种补偿能量即样品吸收(峰向下)或放出(峰向上)的热量。则时,反应的化学方程式为 。二水合草酸镍分解的整个反应是 (填“吸热”或“放热”)反应。
18.(14分)氢能将在实现“双碳”目标中起到重要作用。乙醇—水催化重整可获得氢气。主要发生以下反应:
反应①:
反应②:2
回答下列问题:
(1)反应①自发进行的条件是 。
A.高温B.低温C.高压D.低压
(2)已知有关键能数据如下表:
反应②中△H2= kJ∙ml-1反应的△H3= kJ∙ml-1。
(3)为提高氢气的平衡产率,可采取的措施为 (写出2条)。
(4)向体积为VL的恒容密闭容器中充入1mlC2H5OH(g)和发生上述反应①②。初始时体系压强为100kPa,平衡时CO2和CO的选择性、H2的产率随温度的变化曲线如图所示。(CO的选择性
①表示CO2的选择性的是曲线 。
②400℃以后,H2的产率随温度变化的原因是 。
③反应①的标准平衡常数其中p0为标准压强100kPa),p(X)为气体X的平衡分压,分压=总压×该气体的物质的量分数。500℃时,测得的转化率为80%,则反应①的= (保留1位小数)。
19.(14分)已知间苯二酚可以合成中草药的活性成分Psralidin(化合物P),合成路线如图:
P
已知:①2 equiv即加入2倍物质的量的试剂
② ③
(1)A中官能团的名称为 。
(2)C的结构简式为 。
(3)D→E的方程式为 。
(4)写出一个满足下列条件的B的同分异构体 。
①与溶液反应显紫色
②核磁共振氢谱显示5组峰,且峰面积之比为2:2:2:1:1
(5)H+→Psralidin+J的反应原理如图。J的名称为 。
(6)G→H的过程中分为三步反应。K的结构简式为 ,K→M的反应类型是 。
0.25
0.50
1.00
0.50
1.00
0.050
0.050
0.100
0.100
0.200
1.6
3.2
3.2
4.8
选项
实验目的
实验操作
A
测定中和热
将的NaOH溶液一次性迅速倒入盛盐酸的烧杯中
B
证明炭可与浓HNO3反应生成NO2
向浓HNO3中插入红热的炭,产生红棕色气体
C
证明AgCl的溶解度大于
向的溶液中滴加几滴NaCl溶液,产生白色沉淀,再滴加几滴溶液产生黑色沉淀
D
制取氨气并干燥
加热氯化铵和氢氧化钙的混合物,将产生的气体通过装有无水氯化钙的干燥管
化学键
H−H
H−O
C=O
C≡O
键能/kJ·ml⁻¹
436
464
803
1071
相关试卷
这是一份2024年高考第二次模拟考试化学(新九省高考“144模式”)试卷(Word版附解析),文件包含化学新九省高考“14+4模式”2024年高考第二次模拟考试全解全析docx、化学新九省高考“14+4模式”2024年高考第二次模拟考试考试版A4docx、化学新九省高考“14+4模式”2024年高考第二次模拟考试考试版A3docx、化学新九省高考“14+4模式”2024年高考第二次模拟考试参考答案docx等4份试卷配套教学资源,其中试卷共30页, 欢迎下载使用。
这是一份2024年高考第二次模拟考试化学(新九省高考“154模式”)试卷(Word版附解析),文件包含化学新九省高考“15+4模式”2024年高考第二次模拟考试全解全析docx、化学新九省高考“15+4模式”2024年高考第二次模拟考试考试版A4docx、化学新九省高考“15+4模式”2024年高考第二次模拟考试考试版A3docx、化学新九省高考“15+4模式”2024年高考第二次模拟考试参考答案docx等4份试卷配套教学资源,其中试卷共42页, 欢迎下载使用。
这是一份化学(新九省高考“14+4模式”)--2024年高考化学第二次模拟考试,文件包含化学新九省高考“14+4模式”考试版A4pdf、化学新九省高考“14+4模式”参考答案pdf等2份试卷配套教学资源,其中试卷共10页, 欢迎下载使用。









