
2024年江苏省徐州市新沂市五科联考中考化学模拟试卷
展开
这是一份2024年江苏省徐州市新沂市五科联考中考化学模拟试卷,共7页。试卷主要包含了选择题,非选择题共44分等内容,欢迎下载使用。
1.中国传统文化博大精深,源远流长。下列对古文献记录内容理解正确的个数是( )
①《抱朴子•金丹篇》中记载:“丹砂(HgS)烧之成水银,积变又还成丹砂”。该过程发生了分解反应和化合反应,在分解反应中硫元素被氧化
②《本草纲目拾遗》写道:“强水性最烈,能蚀五金……,五金八石皆能穿滴,惟玻璃可盛。”文中的“强水”即现代化学中的盐酸
③“春蚕到死丝方尽,蜡炬成灰泪始干”中“丝”的主要成分是纤维素,“泪”的主要成分是石蜡,它们均属于有机物
④《本草纲目》记载“烧酒非古法也,自元时创始,其法用浓酒和糟入甑(指蒸锅),蒸令气上,用器承滴露。”该段文字记载了白酒(烧酒)的制造过程中采用了蒸馏的方法来分离和提纯
⑤《泉州府志》物产条载:“初,人不知盖泥法,元时南安有长者为宅煮糖,宅垣(黄泥造的墙)忽坏,去土而糖白,后人遂效之”,该段文字记载了蔗糖的分离提纯采用了黄泥来吸附红糖中的色素
A.2个B.3个C.4个D.5个
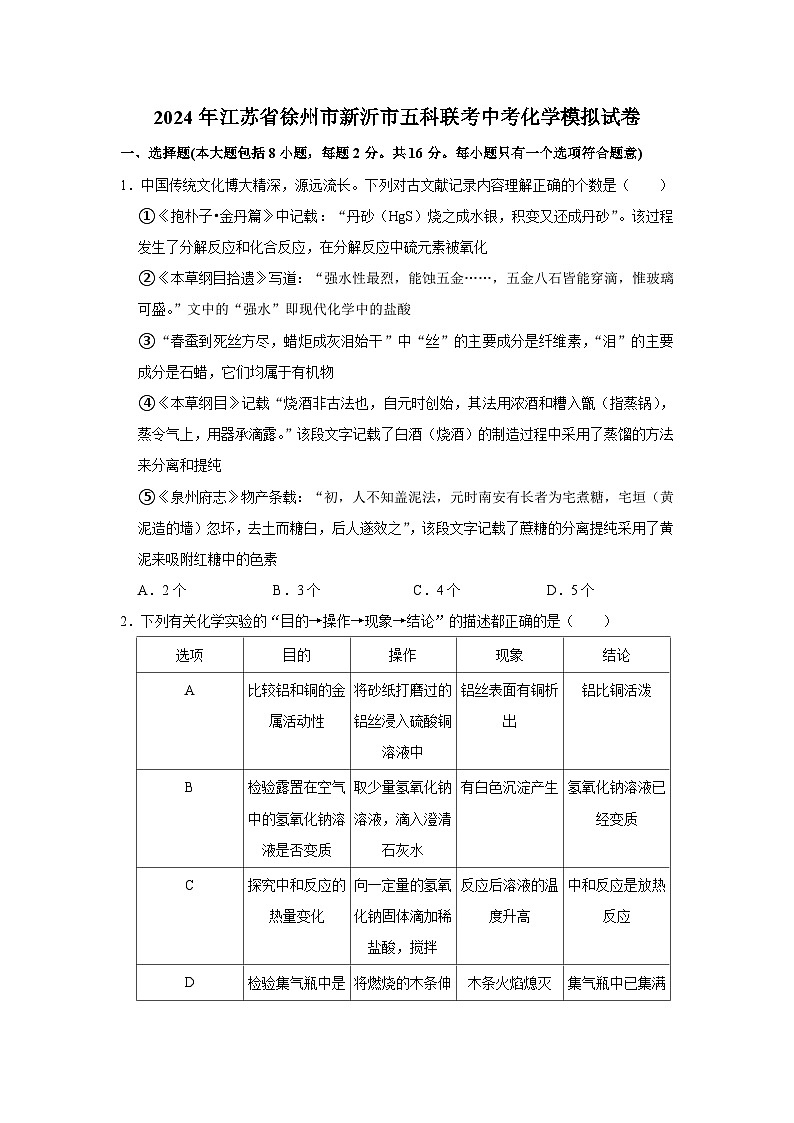
2.下列有关化学实验的“目的→操作→现象→结论”的描述都正确的是( )
A.AB.BC.CD.D
3.下列装置(省略了夹持仪器)中能作为制备CO2的发生装置,且能随时控制反应的发生与停止的是( )
A.B.
C.D.
4.如图为某化工企业生产流程示意图:
下列说法不正确的是( )
A.钛酸亚铁(FeTiO3)中钛元素为+4价
B.①中反应为:2FeTiO3+6C+7Cl2═2X+2TiCl4+6CO,则X为FeCl3
C.③中氩气(Ar)作保护气,反应类型为置换反应
D.②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为1:2
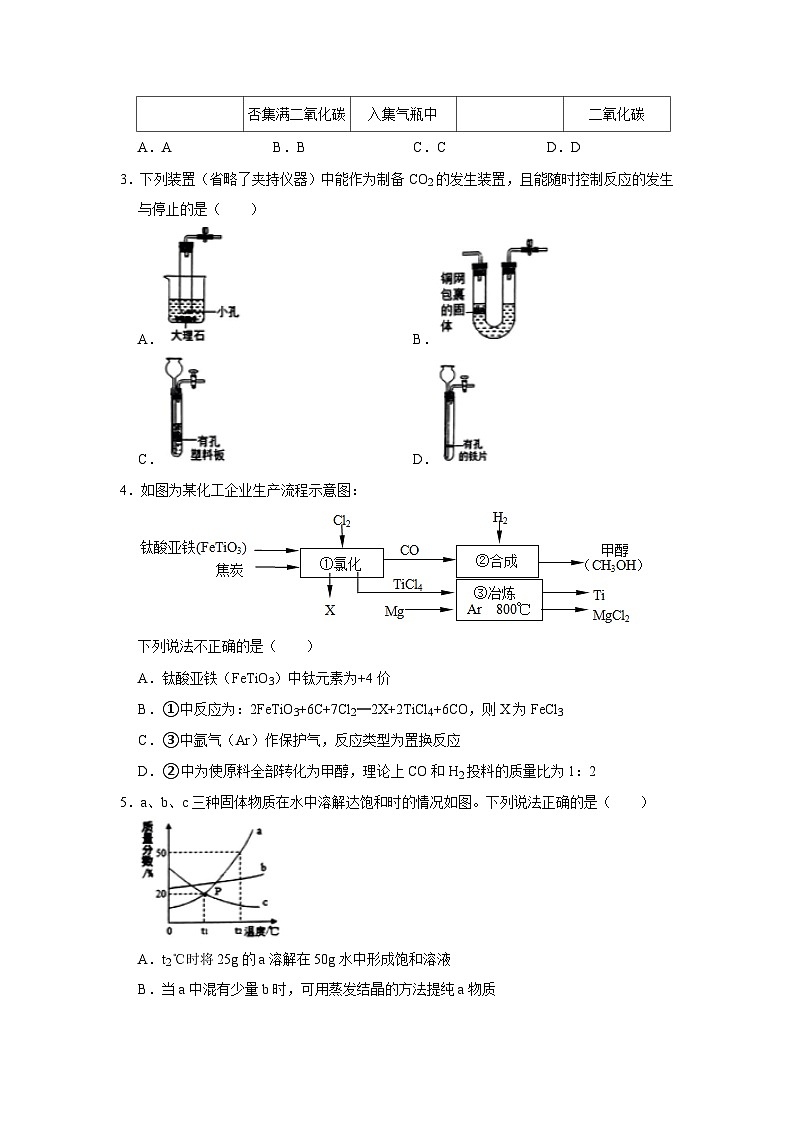
5.a、b、c三种固体物质在水中溶解达饱和时的情况如图。下列说法正确的是( )
A.t2℃时将25g的a溶解在50g水中形成饱和溶液
B.当a中混有少量b时,可用蒸发结晶的方法提纯a物质
C.t1℃时a、b、c的溶解度大小顺序为a>b=c
D.t2℃时a、c的饱和溶液降温至t1℃时它们的质量分数a>c
6.将一定质量的铁粉加至H2SO4、MgSO4和CuSO4的混合溶液中,充分反应后过滤,得到滤液M和滤渣N。下列有关说法中,不合理的是( )
A.若滤液呈蓝色,则滤液的pH小于7
B.滤渣N的质量一定大于加入铁粉的质量
C.滤渣N中一定没有单质镁
D.滤液M中至少含有两种金属阳离子
7.天然气是一种重要的化工原料和燃料,常含有少量H2S,一种在酸性介质中进行天然气脱硫的原理示意图如图所示。下列说法正确的是( )
A.脱硫过程中溶液中的浓度逐渐增大
B.过程②中发生的反应属于化合反应
C.整个脱硫过程中参加反应的n(H2S):n(O2)=2:1
D.脱硫过程需不断补充FeSO4
8.向100gNaOH溶液中通入CO2得到溶液X,向溶液X中逐滴滴加3.65%的盐酸,产生CO2的质量与加入盐酸质量的关系如图(已知:Na2CO3+HCl═NaHCO3+NaCl,NaHCO3+HCl═NaCl+CO2↑+H2O),下列说法正确的是( )
A.NaOH溶液的溶质质量分数为6.4%
B.通入CO2的质量为3.92g
C.溶液X中含有NaOH和NaHCO3
D.加盐酸至120g时溶液中的溶质只有NaHCO3
二、非选择题共44分
9.科学技术的进步,证明宏观物质世界由分子、原子、离子等微观粒子构成。
(1)根据图示,按要求回答问题:
①图甲是氯元素在元素周期表中的部分信息,氯元素的相对原子质量是 ;
②图乙是某原子的结构示意图,该元素处在元素周期表第 周期;
③图丙是某化学反应的微观示意图,写出该反应的化学方程式 。
(2)如图为金属Zn和NaHSO4溶液反应的微观示意图,实际与Zn发生反应且得到电子的粒子是 (填符号)。
(3)以化合价为纵坐标、物质类别为横坐标绘制成如图。图中A、B、C、D、E是初中常见物质且都含有氧元素,各物质中均有某种组成元素的化合价与纵坐标的数值相对应。“→”表示物质间的转化关系,其中B通常为无色无味气体,D的水溶液呈蓝色。
①D→E的化学方程式是 。
②B→A的实现路径可以是 。
10.关于酸的研究是一项重要的课题,某小组以“研究硝酸(HNO3)的性质”为主题开展了以下项目式学习。
【任务一】硝酸的物理性质
(1)同学们通过查阅资料可知,纯硝酸为无色透明液体,有窒息性刺激气味。浓硝酸含量为68%左右,无色透明,易挥发,在空气中产生白雾(与浓盐酸相同),浓硝酸敞口放置浓度会 (填“变大”、“不变”或“变小”)。
【任务二】硝酸的化学性质
(2)①不稳定性:浓、稀硝酸性质相差很大,如稀硝酸相对稳定,但浓硝酸不稳定,遇光或热会分解而放出二氧化氮、水和某助燃单质。请写出浓硝酸受热发生的反应化学方程式为 。
②强酸性:稀硝酸具有酸的通性,将氧化铁加入装有稀硝酸的试管中,观察到的现象是红棕色粉末消失,溶液由无色变为黄色。
③强氧化性:小组同学将紫色石蕊溶液滴到装有浓硝酸的试管中,发现石蕊溶液先变红后褪色。
【提出问题】石蕊溶液褪色的原因是什么?
【猜想假设】甲同学:石蕊变质。乙同学: 。
【实验与结论】同学们认为甲同学猜测不合理,理由是 。
为了验证自己的猜想是否正确,乙同学设计了如下实验方案。
(3)工业上以氨气为原料制备硝酸的过程(如图1)如图:
某课外小组认真分析了工业制取硝酸的流程及反应原理,设计了如图2的实验装置制备硝酸,试回答下列相关问题:
①完成图1工业上用氨气制取NO的化学方程式 ,然后产生的NO被氧气氧化成NO2,NO2和水反应生成硝酸和NO。
②图2中通入的a气体(氧气)的目的是 。
③盛有Na2CO3溶液的烧杯作为尾气处理装置有点缺陷,某兴趣小组把图2右边装置改进成如图3的装置,这样改进的优点是 。
11.在丰富多彩的物质世界里,铁及其化合物占有重要地位。某化学兴趣小组进行了以下实验探讨铁及其化合物性质。
实验一:制备Fe3O4纳米材料:先向FeCl2溶液中加入NaOH生成Fe(OH)2,再用O2将其部分氧化为Fe(OH)3;最后将氢氧化物加热分解制得Fe3O4纳米材料。
(1)当Fe(OH)2和Fe(OH)3的质量比为 时,生成的Fe3O4的质量最优。
实验二:某工业铁红(Fe2O3)样品中可能混有一种黑色的氧化物杂质,该杂质可能是FeO或Fe3O4,为探究样品中是否含有杂质及杂质的成分,兴趣小组同学准确称取8.0g样品,进行如下实验,完全反应后E装置增重2.4g。
注:碱石灰是氧化钙与氢氧化钠固体混合物,可用作干燥剂,能与二氧化碳气体反应。
(2)实验时装置的连接顺序为A→F→C……,装置F中试剂X是 。
(3)下列实验操作步骤的合理顺序是 (填编号)。
A.加热装置D中反应管
B.检验H2的纯度
C.打开装置A中分液漏斗活塞,向圆底烧瓶中加入稀盐酸
(4)待D反应结束后停止加热,继续通A产生气体的作用是 。
(5)该工业铁红样品中混有 杂质。
实验三:探究铁锈蚀的因素
小组设计了如图一装置,检查气密性,将5g铁粉和2g炭粉加入三颈烧瓶,t1时刻加入2mL饱和NaCl溶液后,再将一只装有5mL稀盐酸的注射器插到烧瓶上,采集数据。
(6)据图二,t2时刻后反应并未停止温度却开始降低,原因是 。
(7)据图三,分析t1时刻压强突然变大的原因是 (用化学方程式表示)。
12.现有FeCl3和CuCl2的混合溶液195.2g,向其中加入铁粉反应的先后顺序为:2FeCl3+Fe═3FeCl2,CuCl2+Fe═FeCl2+Cu。加入铁粉质量与反应后溶液中剩余固体质量的关系如图所示。
(1)m(剩余固体)>6.4g时,剩余固体的成分是 (填化学式)。
(2)求当加入11.2g铁粉时,反应后所得溶液中FeCl2的质量分数(写出计算过程)。
选项
目的
操作
现象
结论
A
比较铝和铜的金属活动性
将砂纸打磨过的铝丝浸入硫酸铜溶液中
铝丝表面有铜析出
铝比铜活泼
B
检验露置在空气中的氢氧化钠溶液是否变质
取少量氢氧化钠溶液,滴入澄清石灰水
有白色沉淀产生
氢氧化钠溶液已经变质
C
探究中和反应的热量变化
向一定量的氢氧化钠固体滴加稀盐酸,搅拌
反应后溶液的温度升高
中和反应是放热反应
D
检验集气瓶中是否集满二氧化碳
将燃烧的木条伸入集气瓶中
木条火焰熄灭
集气瓶中已集满二氧化碳
实验步骤
实验现象
实验结论
分别取2mL稀硝酸和浓硝酸于2支试管中,依次滴加2滴紫色石蕊溶液
稀硝酸:溶液变为红色
浓硝酸:溶液先变红后褪色
乙同学猜想正确
相关试卷
这是一份2024年江苏省徐州市新沂市五科联考中考化学模拟试卷,共7页。试卷主要包含了选择题,非选择题共44分等内容,欢迎下载使用。
这是一份2023年江苏省徐州市柳新镇中心中学中考模拟化学试卷,共1页。
这是一份2022年江苏省徐州市中考化学试卷,共19页。试卷主要包含了选择题,化学填空题,化学实验与探究题,化学计算题等内容,欢迎下载使用。









