

初中化学课题3 溶液的浓度教学设计
展开1、通过生活经验和自主学习,知道溶质的质量分数可以表示浓度,认识溶质的质量分数的含义,能用公式表示溶质的质量分数。通过合作探究,加深对溶质的质量分数含义的理解。
2.通过对问题的判断、讨论和归纳,知道固体溶解度与其同温度下饱和溶液中溶质的质量分数的关系。
3.通过合作学习,能够灵活的运用所学的知识进行有关溶质质量分数的计算,掌握基本的解题方法,建立溶液的稀释问题中“溶质的质量不变”的思想,培养运用知识和分析解决问题的能力,初步感受定量研究的意义,体会溶液在生产生活中的应用价值。
【教学重难点】
重点:溶质的溶质质量分数的概念,以及有关溶质质量分数的简单的计算。
难点:溶液的溶质质量分数的简单计算,以及有关溶液稀释的计算。
【评价任务】
评价任务 1:通过生活经验和自主学习,知道溶质的质量分数可以表示浓度,认识溶质的质量分数的含义,能用公式表示溶质的质量分数。通过合作探究,加深对溶质的质量分数含义的理解。(针对目标 1)
评价任务 2:通过对问题的判断、讨论和归纳,知道固体溶解度与其同温度下饱和溶液中溶质的质量分数的关系。(针对目标 2)
评价任务 3:通过合作学习,能够灵活的运用所学的知识进行有关溶质质量分数的计算,掌握基本的解题方法,建立溶液的稀释问题中“溶质的质量不变”的思想,培养运用知识和分析解决问题的能力,初步感受定量研究的意义,体会溶液在生产生活中的应用价值。(针对目标 3)
【教学方法】讲授法、讨论法、启发引导法
【教学活动设计】
教学流程
课后反思
《溶液的浓度》本节课是课题三的内容,重点是溶质的质量分数概念及简单计算。这节课我主要是以学生的自学与交流为主,老师的解惑、纠正为辅,把课堂交给学生来完成的。学生小组的讨论比老师直接灌输要更深刻,更容易接受。教材中引入的溶质质量分数概念非常简单,计算公式也简洁明了,通过自学与合作探究,学生可以完成对基本概念的理解,其中重要的问题让学生先来讲解,并做适当补充。加强了物理与数学化学等学科的联系,引导学生在更宽广的学科背景下综合的运用化学和其他学科的知识分析。在教学实践过程中,通过“刘能贪图便宜买到了不好的玉米种子,怎样才能把好的玉米种子选出来?王天来配制的食盐水太浓了无法进行选种,该如何稀释?”这个情景,让学生感受到化学是来源于生活,学习化学知识可以解决生活中的问题,在“用中学”,同时,让学生处在浓厚的学习兴趣中,带着渴求知识的状态合作探究。兴趣是学习知识的最好导师,让学生在体会学习所带来的喜悦。通过溶液在无土栽培技术中的应用,紧密联系生产生活实际使学生认识到化学能够创造更丰富的物质,满足人们日益增长的美好的生活的需求,让学生感知化学对人类文明和社会可持续发展有重要价值。用习近平总书记的期盼做结尾,增强学生为实现中华民族伟大复兴和推动社会进步而勤奋学习的责任感。
通过本次化学教学活动,以下是我的反思:
1、在教学目标的制定上,体现核心素养发展的全面性和进阶性,教师无论在课堂还是课后都要善于思考,理论与实践相结合,多点对自己的教学进行反思和总结,不断修正自己的教学方法,树立正确的教学观念,与时俱进。培养学生的科学思维,在事实和逻辑的基础上进行独立思考和判断,对不同信息观点和结论进行质疑和批判,提出创造性见解的能力。发展科学思维,强化创新意识,养成科学态度,使学生对化学促进人类文明和社会可持续发展的重要价值有积极的认识。
2、在教学中采用小组为单位合作探究,讲究实效。把握探究的程度和水平,避免浅尝辄止或随意提高知识的难度的做法,在教学过程当中注重探究,实践与科学思维的培养,重视教学评一体化,注重启发式探究式学习,促进学生自主学习和深度学习,发展科学思维能力。加强过程性评价,注重活动性评价,注重学生的自评和互评。加强学生自我反思能力,以评促学,以评促教,发挥评价的育人功能。
3、增加对学生的了解,多和学生沟通和交流,接收学生在学习化学上存在的疑问等有效信息,有针对性地进行教学。同时也能增加师生的感情,令课堂气氛愉快,促进师生互动,增大教学效果。
4、提高化学用语的表述能力,提高化学教师的专业素养。多留意教学上的细节方面,给学生打下扎实的化学基础。
5、多媒体的使用要恰当,不要过渡依赖多媒体,也不要太过注重传统教学模式,忽视多媒体的作用。环节
教学活动
评价要点
导入
(一)创设情境、唤醒常识大家在生活中是怎样感知溶液的浓和稀的?
【学生回答】根据颜色的深浅,味道或气味的不同,大家可以判断溶液是浓还是稀,可是这种方法比较粗略,不能准确的表明一定量的溶液里究竟含有多少溶质,在实际的生产生活中常常要准确的知道一定量的溶液里所含溶质的质量及溶液的浓度
我们青州走着悠久的种植蜜桃的历史,为了防治病虫害,获得丰收,吃到美味的桃子,所以要定期喷洒农药,如果药太稀了,不能有效防治病虫害,如果农药浓度太浓的话,不仅会伤害农作物,还会造成不必要的环境污染和浪费!所以我们需要精准的知道溶液的浓度。在生活中我们可以见到很多表示溶液浓度的方法,白酒百分数是体积分数,代表酒精体积与总的溶液的体积比,0.9%的生理盐水是 100mL水中有 0.9g氯化钠。表示溶质浓度的方法有很多,
【学生回答】今天我们来学习一种比较常用的方法---溶质的质量分数。
(二)出示学习目标
1、通过生活经验和自主学习,知道溶质的质量分数可以表示浓度,认识溶质的质量分数的含义,能用公式表示溶质的质量分数。通过合作探究,加深对溶质的质量分数含义的理解。
2.通过对问题的判断、讨论和归纳,知道固体溶解度与其同温度下饱和溶液中溶质的质量分数的关系。
3.通过合作学习,能够灵活的运用所学的知识进行有关溶质质量分数的计算,掌握基本的解题方法,建立溶液的稀释问题中“溶质的质量不变”的思想,培养运用知识和分析解决问题的能力,初步感受定量研究的意义,体会溶液在生产生活中的应用价值。
从生活经验出发,让学生感受溶液的浓和稀溶液浓度的方法,生活中处处有化学,感受我们家乡的魅力,化学与我们的生活息息相关的理念,同时培养语言表达能力
板块一:溶质质量分数的含义(对应目标 1)
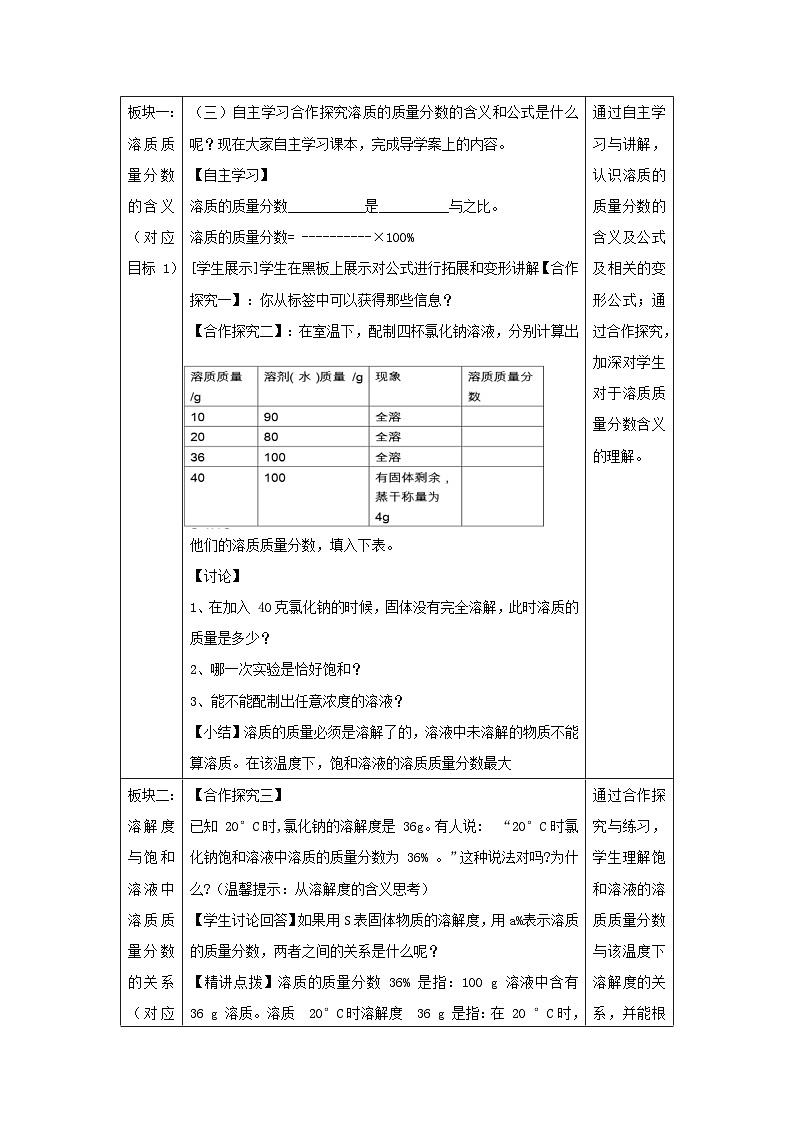
(三)自主学习合作探究溶质的质量分数的含义和公式是什么呢?现在大家自主学习课本,完成导学案上的内容。
【自主学习】
溶质的质量分数___________是__________与之比。
溶质的质量分数= ----------×100%
[学生展示]学生在黑板上展示对公式进行拓展和变形讲解【合作探究一】:你从标签中可以获得那些信息?
【合作探究二】:在室温下,配制四杯氯化钠溶液,分别计算出他们的溶质质量分数,填入下表。
【讨论】
1、在加入 40克氯化钠的时候,固体没有完全溶解,此时溶质的质量是多少?
2、哪一次实验是恰好饱和?
3、能不能配制出任意浓度的溶液?
【小结】溶质的质量必须是溶解了的,溶液中未溶解的物质不能算溶质。在该温度下,饱和溶液的溶质质量分数最大
通过自主学习与讲解,认识溶质的质量分数的含义及公式及相关的变形公式;通过合作探究,加深对学生对于溶质质量分数含义的理解。
板块二:溶解度与饱和溶液中溶质质量分数的关系(对应目标 2)
【合作探究三】
已知 20°C时,氯化钠的溶解度是 36g。有人说: “20°C时氯化钠饱和溶液中溶质的质量分数为 36% 。”这种说法对吗?为什么?(温馨提示:从溶解度的含义思考)
【学生讨论回答】如果用S表固体物质的溶解度,用a%表示溶质的质量分数,两者之间的关系是什么呢?
【精讲点拨】溶质的质量分数 36% 是指:100 g 溶液中含有 36 g 溶质。溶质 20°C时溶解度 36 g 是指:在 20 °C时,100 g 水中最多溶解该溶质 36 g 。
【学生回答】关系:
【学以致用】在 20°C时,将 40g硝酸钾固体加入 100g水中,充分搅拌后,仍有 8.4g硝酸钾固体未溶解。
请填写下列空白:
①所得溶液是 20°C时硝酸钾的_______ 溶液(填“饱和”或“不饱”)
② 20°C时硝酸钾的溶解度为 ________;
③所得溶液中硝酸钾的质量分数为。(只列算式)。
【学生回答】对答案并说明
【自评表】
通过合作探究与练习,学生理解饱和溶液的溶质质量分数与该温度下溶解度的关系,并能根据溶解度进行饱和溶液的溶质质量分数的计算。
板块三:关于溶质的质量分数的计算(对应目标 3)
(四)运用新知,解决问题关于溶质的质量分数的计算
【情景导入】刘能贪图便宜买到了不好的玉米种子,怎样才能把好的玉米种子选出来?如何解决这个问题呢?
例 1、在农业上,常需要用质量分数为 16%的氯化钠溶液来选种。配制 150kg这种溶液,需要氯化钠和水的质量各是多少?
【学生描述思路步骤】过渡语:我们做实验时,常需要用到稀盐酸或稀硫酸等,但我们实验室购买的却是浓盐酸、浓硫酸,那大家想想怎么把浓溶液变为稀溶液呢?
提问:浓溶液变稀溶液的方法:加溶剂
【情景导入】王天来配制的食盐水太浓了无法进行选种,该如何稀释?探究:溶液的稀释问题
【精讲点拨】
1、溶液稀释前后溶质的质量不变
2、溶液稀释计算公式:m浓×W浓=m稀×W稀
例 2、化学实验室现有质量分数为 98%的浓硫酸,但在实验中常需要用较稀的硫酸。要把 50g上述浓硫酸稀释为溶质质量分数为 20%的硫酸,需要水的质量是多少?
【学生讨论】黑板展示
【学以致用】要把 50mL 20%的 NaCl溶液稀释为 16%,需要加入水多少 g?
(氯化钠的密度为 1.15g/mL)(温馨提示:对于涉及体积计算的题,在计算过程中,一定要将体积转化为质量。)
【自评表】
通过刘能贪图便宜买到了不好的玉米种子,怎样才能把好的玉米种子选出来?王天来配制的食盐水太浓了无法进行选种,该如何稀释?让学生感受到化学是来源于生活,学习化学知识可以解决生活中的问题,同时,让学生处在浓厚的学习兴趣中,带着渴求知识的状态自主学习。通过例题的谈论和分析,学会溶质质量分数的简单计算及溶液稀释问题的解题方法,能运用所学的理论解决实际的问题,并了解化学计算题表达的规范格式,养成良好的解题习惯。
总结和知识构建
说说这节课学到了什么?
【学生发表收获感言】
【教师总结】溶液在无土栽培技术中的应用简介习近平总书记的寄语期盼
通过溶液在无土栽培技术中的应用,感受化学学习的意义,通过寄语,督促同学们好好学习发扬创新
板书设计
初中化学人教版九年级下册课题3 溶液的浓度教学设计: 这是一份初中化学人教版九年级下册<a href="/hx/tb_c76882_t8/?tag_id=27" target="_blank">课题3 溶液的浓度教学设计</a>,共4页。教案主要包含了教学目标,教学重难点,教学分析,教学过程等内容,欢迎下载使用。
初中化学人教版九年级下册课题3 溶液的浓度教案设计: 这是一份初中化学人教版九年级下册<a href="/hx/tb_c76882_t8/?tag_id=27" target="_blank">课题3 溶液的浓度教案设计</a>,共2页。教案主要包含了复习引入,学习新课,课堂小结,板书设计等内容,欢迎下载使用。
初中化学人教版九年级下册课题3 溶液的浓度教学设计: 这是一份初中化学人教版九年级下册课题3 溶液的浓度教学设计,共2页。教案主要包含了教学目标,教学重点难点,教法学法,教学仪器用品和药品,教学流程等内容,欢迎下载使用。













