

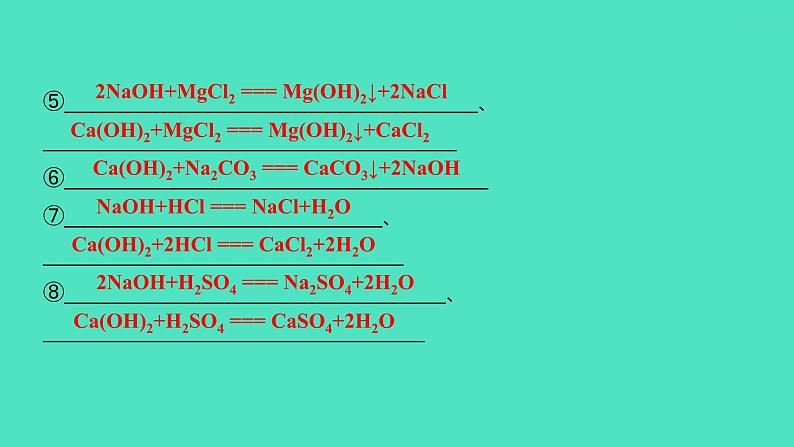

2024中考一轮复习 鲁教版化学 教材基础复习 第七单元 第一节、第二节 酸及其性质、碱及其性质 课件
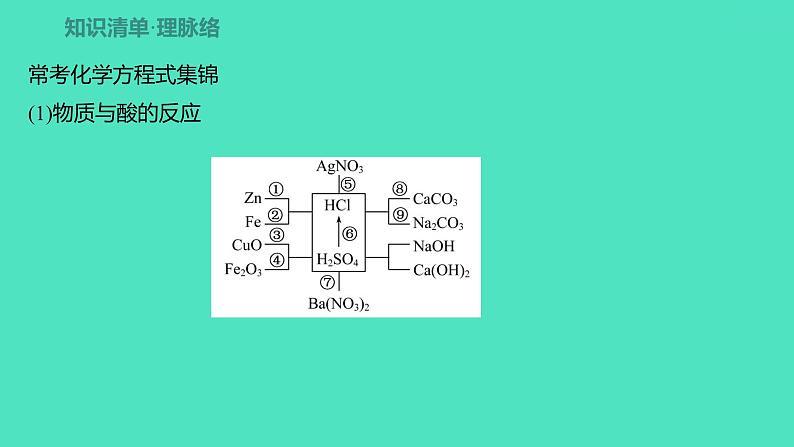
展开常考化学方程式集锦(1)物质与酸的反应
①___________________________、______________________________ ②___________________________、 _____________________________ ③______________________________、 ________________________________ ④________________________________、 _________________________________ ⑤________________________________ ⑥__________________________________
Zn+2HCl===ZnCl2+H2↑
Zn+H2SO4 === ZnSO4+H2↑
Fe+2HCl === FeCl2+H2↑
Fe+H2SO4 === FeSO4+H2↑
CuO+2HCl === CuCl2+H2O
CuO+H2SO4 === CuSO4+H2O
Fe2O3+6HCl === 2FeCl3+3H2O
Fe2O3+3H2SO4 === Fe2(SO4)3+3H2O
AgNO3+HCl === AgCl↓+HNO3
H2SO4+BaCl2 === BaSO4↓+2HCl
⑦_______________________________________ ⑧______________________________________ ⑨________________________________________________
Ba(NO3)2+H2SO4 === BaSO4↓+2HNO3
2HCl+CaCO3 === CaCl2+H2O+CO2↑
Na2CO3+2HCl === 2NaCl+H2O+CO2↑(合理即可)
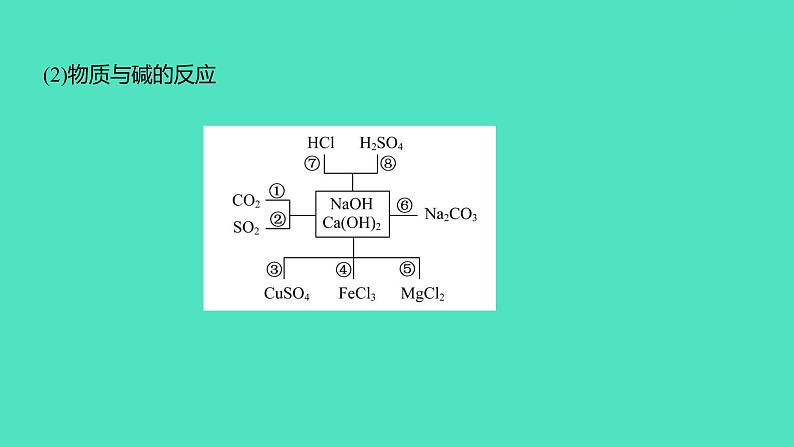
①_________________________________、 __________________________________ ②________________________________、 _________________________________③________________________________________、________________________________________④_____________________________________
CO2+2NaOH === Na2CO3+H2O
CO2+Ca(OH)2 === CaCO3↓+H2O
SO2+2NaOH === Na2SO3+H2O
SO2+Ca(OH)2 === CaSO3+H2O
2NaOH+CuSO4 === Cu(OH)2↓+Na2SO4
Ca(OH)2+CuSO4 === CaSO4+Cu(OH)2↓
FeCl3+3NaOH === Fe(OH)3↓+3NaCl
⑤_______________________________________、_______________________________________ ⑥________________________________________⑦______________________________、__________________________________⑧____________________________________、 ____________________________________
2NaOH+MgCl2 === Mg(OH)2↓+2NaCl
Ca(OH)2+MgCl2 === Mg(OH)2↓+CaCl2
Ca(OH)2+Na2CO3 === CaCO3↓+2NaOH
NaOH+HCl === NaCl+H2O
Ca(OH)2+2HCl === CaCl2+2H2O
2NaOH+H2SO4 === Na2SO4+2H2O
Ca(OH)2+H2SO4 === CaSO4+2H2O
易错辨析判断下列说法是否正确。(1)酸中一定含有氢元素,但含有氢元素的物质不一定是酸。( )(2)能与酸反应生成盐和水的不一定是碱。( )(3)Ca(OH)2溶液与NaOH溶液都能与CO2反应,都可用来检验CO2。( )(4)浓盐酸敞口放置,瓶口有白烟产生。( )(5)氢氧化钙显碱性,可用来治疗胃酸过多,同时可用作补钙剂。( )(6)硫酸与氯化钡反应,盐酸与硝酸银反应都不是酸的通性。( )
追根溯源(教材习题变式)1.存放药品时,某化学实验员不小心将药品标签撕去了一部分(如图),根据所学知识,你判断该药品一定不是( )A.氧化物 B.酸 C.碱 D.盐2.实验室中有两瓶失去标签的无色溶液,分别为稀盐酸与氢氧化钠溶液,下列选用的物质不能将它们鉴别出来的是( )A.紫色石蕊试液 B.镁条C.氧化铜D.硫酸钠溶液
3.固体氢氧化钠在空气中不但易吸收水蒸气而潮解,还能吸收二氧化碳而变质。下列有关说法正确的是 ( )①潮解过程是物理变化②变质过程是化学变化③变质过程是物理变化④潮解过程是化学变化A.①② B.③④ C.①③ D.②④
4.下列关于硫酸的说法错误的是 ( )A.浓硫酸有强烈的腐蚀性B.稀释浓硫酸时,应将水注入浓硫酸中,并用玻璃棒搅拌C.稀硫酸可用来除铁锈D.浓硫酸有吸水性,可作干燥剂
5.某同学用实验方法区别稀硫酸和氢氧化钠溶液(记作A、B)。①他取适量A、B两种溶液于两支试管中,分别加入适量Na2CO3溶液,观察到A溶液中产生无色气泡,则A是____________,发生反应的化学方程式为 ______________________________________; ②他另取适量A、B两种溶液于两支试管中,分别加入适量CuCl2溶液,B溶液中的现象是__________________,发生反应的化学方程式为 ___________________________________; ③他还用了下列试剂中的一种区别A、B两种溶液,该试剂可以是___________。 A.铁锈B.石蕊溶液C.酚酞试液D.铁粉
Na2CO3+H2SO4===Na2SO4+H2O+CO2↑
2NaOH+CuCl2===Cu(OH)2↓+2NaCl
考点一 酸及其通性【示范题1】“泱泱齐风·陶韵淄博”。2023年火遍全国的淄博人专门制作了烧烤地图,开通了烧烤专列。受此启发在学了酸的化学性质后,小明同学以稀硫酸为主题展开了探究。
(1)初步探究:小明绘制了“多彩酸世界”思维导图。若用 Cu(OH)2实现②,会得到________色溶液。若想实现③,得到浅绿色溶液,可选用的单质是_____________。若选用 BaCl2溶液实现⑤,此反应的化学方程式为_________________________________。
BaCl2+H2SO4===BaSO4↓+2HCl
(2)拓展探究:“化学列车”的五节车厢分别乘坐了如图所示的五种物质,其中 A 是一种常见气体单质。“→”表示相邻车厢中物质从左至右的转化关系。请回答下列问题:①A 是_______________。
②写出上述转化关系中3号门两侧车厢中物质转化的化学方程式: ____________________________________________________________________________。 ③“旅客”能上车的条件是与门两边车厢中的物质都能反应。那么“旅客”稀硫酸可以从_______号门上车。
Ca(OH)2+Na2CO3===CaCO3↓+2NaOH[或
Ba(OH)2+Na2CO3===BaCO3↓+2NaOH]
【方法点拨】1.熟记酸的通性:
2.明确几个常考易错点:(1)酸的化学性质中有两条“生气”的反应:酸+活泼金属→H2↑+盐,酸+碳酸盐→CO2↑+盐+H2O。(2)稀盐酸(稀硫酸)与铁反应生成氯化亚铁(硫酸亚铁),溶液为浅绿色;和氧化铁反应生成氯化铁(硫酸铁),溶液为棕黄色。(3)由于不同的酸溶于水时电离出的酸根离子不同,其性质也存在差异(不属于酸的通性)。例如,硫酸能与氯化钡溶液反应,生成白色的硫酸钡沉淀,而盐酸不能。
考点二 碱及其通性【示范题2】(2023·山西中考)以典型物质为核心,进行问题的设置与整合,是我们全面认识物质性质及应用的有效途径。小明同学在小组合作学习过程中,对氢氧化钠的相关问题,以结构图的形式进行了如下梳理。联系实际,解决问题:
(1)氢氧化钠在生活中可用来___________________________。 (2)氢氧化钠在空气中吸水后的热量变化为__________。 (3)氢氧化钠使用时必须十分小心,原因是__________________________。 (4)检验氢氧化钠溶液的酸碱度,最简单的方法是____________________。 (5)向氢氧化钠溶液中滴加硫酸铜溶液,发生反应的化学方程式为_______________________________________。
作炉具清洁剂(合理即可)
氢氧化钠具有强腐蚀性
2NaOH+CuSO4===Cu(OH)2↓+Na2SO4
【方法点拨】1.熟记碱的通性(如图):
2.明确几个常考易错点:(1)可溶或微溶性碱的溶液能使酸碱指示剂变色,而难溶于水的碱,如Cu(OH)2、Fe(OH)3等在水中难电离则不能使指示剂变色。(2)碱与盐的反应,两种反应物必须均易溶于水。
实验 关于氢氧化钠、氢氧化钙变质的探究一、氢氧化钠变质的探究1.原因: NaOH与空气中的CO2反应生成碳酸钠,反应原理:2NaOH+CO2===Na2CO3+H2O。2.成分分析(1)没有变质:___________; (2)部分变质:____________________; (3)全部变质:____________。
NaOH和Na2CO3
Na2CO3+2HCl===2NaCl+H2O+CO2↑
Na2CO3+Ca(OH)2===CaCO3↓+ 2NaOH
Na2CO3+CaCl2===CaCO3↓+2NaCl
Na2CO3+BaCl2===BaCO3↓+2NaCl
4.除杂:若NaOH中混有Na2CO3 ,在溶液中滴入________________至不再产生沉淀为止,过滤,反应原理:________________________________________。
Na2CO3+Ca(OH)2 ===CaCO3↓+2NaOH
5.探究已变质氢氧化钠是部分变质还是完全变质的方法
Na2CO3+CaCl2 ===
CaCO3↓+2NaCl
Na2CO3+BaCl2 ===
BaCO3↓+2NaCl
二、氢氧化钙变质的探究1.原因:Ca(OH)2与空气中的CO2反应生成碳酸钙,反应原理:Ca(OH)2+CO2===CaCO3↓+H2O。2.成分分析(1)没有变质:_____________; (2)部分变质:_____________________; (3)全部变质:____________。
Ca(OH)2和CaCO3
3.检验氢氧化钙是否变质的方法(1)方法:加入盐酸,若____________产生则说明氢氧化钙已变质。 (2)原理:______________________________________。
CaCO3+2HCl===CaCl2 +H2O+CO2 ↑
4.探究氢氧化钙是部分变质还是全部变质的方案设计
5.在氢氧化钠变质的探究中(1)要确认是否有NaOH,为什么不能直接滴加无色酚酞溶液,原因是___________________________________________。 (2)在除Na2CO3时,不能用盐酸,因为_____________________________。 (3)在除Na2CO3时,也不能用Ca(OH)2或Ba(OH)2原因是________________________________________________________________________。 (4)在除Na2CO3时,为什么要加足量的氯化钙或氯化钡溶液,原因是________________________。
Na2CO3溶液也呈碱性,也能使酚酞溶液变红
盐酸与NaOH也会发生反应
Ca(OH)2、Ba(OH)2
会与Na2CO3反应生成NaOH干扰原溶液中NaOH的检验
除尽溶液中的Na2CO3
6.注意事项(1)检验某物质是否变质,即检验是否有“新物质”;(2)检验某物质的变质程度,即检验是否还有“原物质”。
【示范题】(2023·烟台中考)欲证明“CO2与NaOH能发生化学反应”,某化学兴趣小组进行了以下探究实验(实验装置中夹持仪器、电脑均已略去)。实验一:小亮同学按图1所示装置进行实验实验前U形管两端液面相平,将NaOH溶液滴入试管中,待反应后恢复到室温,U形管中的液面左高右低。
(1)小亮同学根据U形管中液面高度变化得出结论:CO2与NaOH发生了化学反应,该反应的化学方程式是________________________________。 (2)小明认为仅凭U形管中液面高度变化,不足以得出“CO2与NaOH发生了化学反应”的结论,理由是__________________________________。
CO2+2NaOH===Na2CO3+H2O
二氧化碳能溶于水,且可与水反应
实验二:为获得充足的证据,兴趣小组设计了图2所示装置进行实验探究,并利用压强传感器测定实验过程中三颈瓶内压强的变化。
按图2所示,打开压强传感器,观察到三颈瓶内初始压强为101 kPa,将滴有酚酞试液的适量氢氧化钠溶液快速推入瓶内,振荡充分反应。待压强不再减小后,再将适量的稀盐酸快速推入瓶内,振荡充分反应。待压强不再增大后,将两个注射器活塞先后拉回原位(不进行活塞操作时,活塞不能自主移动)。瓶内压强变化如图3所示。
(3)滴有酚酞试液的NaOH溶液呈________色。 (4)向瓶内推入适量稀盐酸后,能证明CO2与NaOH已发生了反应的现象是________________,产生此现象的反应的化学方程式是 ____________________________________。 (5)图3中,________(填序号)段的压强比初始压强低,说明瓶内的水能吸收CO2。 ①CD ②DE ③MN(6)图3中,DE段压强远低于MN段压强,能够说明______________________________________。
二氧化碳与氢氧化钠发生
命题点 常见的酸和碱1.(2019·淄博中考)以下化学实验现象的描述正确的是( )A.镁条在空气中燃烧,火星四射,生成黑色固体B.生锈铁钉放入少量的稀盐酸中,溶液呈现黄色C.打开浓硫酸的试剂瓶塞,瓶口出现大量的白雾D.向氢氧化钠溶液中滴加少量紫色石蕊试液,溶液变红色
2.(2021·淄博中考)向以下4支试管中分别加入足量盐酸,充分反应后,试管中有残渣的是( )
3.(2022·烟台中考)某化学兴趣小组为探究盐酸的化学性质,进行了如下实验(所加稀盐酸均过量)。
(1)试管A中观察到紫色石蕊试液变________色。 (2)试管B中观察到溶液由无色逐渐变成黄色,是因为反应生成了________ (填化学式),一段时间后有气泡产生,写出产生气泡的化学方程式: ________________________。 (3)试管C中发生反应的化学方程式是____________________________________。 (4)试管D中加稀盐酸至过量,始终没有明显现象。请你设计实验方案证明试管D中的NaOH与HCl发生了反应,__________________________________________________________________________(写出操作及其现象)。
Fe+2HCl===FeCl2+H2↑
向氢氧化钠溶液中滴入几滴酚酞试液,再逐
滴加入稀盐酸,溶液由红色变为无色
基础达标1.(2022·聊城中考)下列图示是几种常见物质溶于水后发生解离的微观示意图,其中能使紫色石蕊试液变红的是 ( )
2.(2023·深圳中考)有关NaOH说法错误的是( )A.NaOH固体溶解时放出热量B.NaOH包装箱上张贴的标识是 C.NaOH是所有气体的干燥剂D.NaOH应密封保存
3.(2023·重庆中考A卷)硫酸和盐酸是工农业生产中重要的两种酸。下列有关选项正确的是( )①它们都能使紫色石蕊溶液变红②打开盛有浓盐酸的试剂瓶可观察到白雾,说明分子在不断运动③将两瓶浓溶液敞口放在空气中,溶液质量都减小④稀硫酸和氯化钡溶液发生复分解反应生成盐酸A.①②③④B.①②④C.①②③D.①③
4.稀释浓硫酸并进行硫酸性质实验的下列操作,正确的是 ( )
5.(2023·南充中考)“物质性质决定用途”是化学观念之一,下列说法错误的是( )A.NaOH显碱性——常用于改良酸性土壤B.洗涤剂具有乳化作用——可用于清洗餐具上的油污C.浓硫酸有吸水性——在实验室中常用作某些气体的干燥剂D.稀有气体在通电时能发出不同颜色的光——可制成多种用途的电光源,如霓虹灯
6.(2023·滨州中考)下列有关实验现象的描述,正确的是( )A.打开盛浓硫酸的试剂瓶,瓶口会形成白雾B.铁与稀硫酸反应时有气泡产生,形成黄色溶液C.将铜片放入稀硫酸中,铜片逐渐消失,形成蓝色溶液D.用稀硫酸除铁锈时,铁锈逐渐溶解,形成黄色溶液
7.(2023·江西中考)《天工开物》中记载:“凡石灰经火焚炼为用。”“石灰”主要成分为氧化钙,下列说法错误的是 ( )A.“石灰”与石灰石成分相同B.“石灰”含有钙、氧元素C.“石灰”与水反应会放热D.“石灰”可用作干燥剂
8.(2023·淄博临淄区模拟)食醋中含有醋酸,在生活中有许多妙用。下列使用食醋肯定不能达到目的的是( )A.使紫色石蕊纸花变红B.检验黄金中是否含有铜C.除去菜刀上的铁锈D.检验鸡蛋壳中是否含有碳酸钙
9.(2022·温州中考)物质的结构决定性质,性质决定用途。下列物质的结构、性质和用途之间匹配正确的是( )
10.在复习课上,同学们让初中常见的化学物质入驻空间站,相互连接的舱中的物质可以发生反应。已知图中X的物质类别是酸,则以下说法正确的是( )A.指示剂为无色酚酞溶液B.Y可能是氯化钡C.Fe2O3与X反应的化学方程式可能为Fe2O3+6HCl===2FeCl3+3H2OD.Ba(NO3)2与X反应后所得溶液的pH一定小于7
11.诗句“梅子留酸软齿牙”中的“梅子”含有较多的柠檬酸,柠檬酸具有酸的通性。小华同学设计如图所示实验,验证柠檬酸的某些性质,下列实验设计不能达成实验目的的是 ( )A.实验①验证柠檬酸溶液呈酸性B.实验②验证柠檬酸能与金属反应C.实验③验证柠檬酸能与碱反应D.实验④验证柠檬酸能与碳酸盐反应
12.(2023·遂宁中考)遂宁某中学举办“理科节”主题活动,杨阳同学表演了一个魔术——“多变的气球”。雅菲用所学知识选择下表4组物质设计如图所示的模拟实验,推测气球变化的现象并分析原理(假设过程中,装置气密性良好;忽略固体和液体的体积变化),现象推测和原理分析都正确的个数有( )
A.1 B.2 C.3 D.4
13.(2023·眉山中考)将一块已生锈的铁片放入质量分数为7.3%的稀盐酸中充分反应,测得生成H2的质量与稀盐酸的质量关系如图所示(假设铁片除有Fe2O3外不含其他杂质)。下列说法错误的是( )A.配制200 g质量分数为7.3%的稀盐酸需要质量分数为36.5%的浓盐酸40 gB.刚开始加稀盐酸时发生反应的化学方程式为Fe2O3+6HCl===2FeCl3+3H2OC.加入12 g稀盐酸时,溶液中的溶质为FeCl2和FeCl3D.m=0.2
14.(2023·河北中考)小明按如图所示进行趣味实验,将U形管开口端放入烧杯内,观察到溶液进入U形管并流入另一端。
(1)烧杯内的溶液呈________色。 (2)二氧化碳与氢氧化钠溶液反应的化学方程式为 ______________________________。 (3)U形管开口端放入烧杯后,管内气体压强__________(选填“增大”“不变”或“减小”),溶液在管内上升并流入另一端。
2NaOH+CO2===Na2CO3+H2O
15.(2022·陕西中考)如图所示,稀硫酸能与相连的物质发生化学反应。(1)稀硫酸与BaCl2溶液反应的现象是__________________。 (2)写出稀硫酸与CuO反应的化学方程式:_______________________________。 (3)若X可用作钾肥,其化学式为___________。
CuO+H2SO4===CuSO4+H2O
16.(2022·新疆中考)归纳总结是学习化学的重要方法,小明同学用思维导图的形式总结了NaOH的四条化学性质如图甲(即NaOH与四类物质能够发生化学反应)。请回答:
(1)反应①中若把酚酞溶液滴加到氢氧化钠溶液中,观察到的现象是________________________。 (2)写出一个符合反应②的化学方程式:_____________________________________________;小红同学将某稀酸溶液逐滴滴入一定量的稀氢氧化钠溶液中,用温度传感器对反应过程中溶液的温度进行实时测定,得到的曲线如图乙,根据图像可以得出该反应是__________(填“吸热”或“放热”)反应。
溶液由无色变为红色
2NaOH+H2SO4===Na2SO4+2H2O
(3)反应③可以选用的盐是________,你选择的依据是________________________________________。 A.NaNO3 B.CuSO4 C.NH4NO3 D.KNO3(4)二氧化碳和一氧化碳都是非金属氧化物,二氧化碳能和氢氧化钠反应,一氧化碳却不能,造成此性质差异的微观原因是______________________。
能力提升1.下列化学反应与事实相符且化学方程式书写正确的是 ( )A.铁和稀盐酸反应:2Fe+6HCl===2FeCl3+3H2↑B.碳酸钠投入稀盐酸中:Na2CO3+HCl===NaCl+CO2↑+H2OC.利用生石灰与水反应放出的大量热来做速热饭盒:CaO+H2O===Ca(OH)2D.酸雨形成的原因:CO2+H2O===H2CO3
2.(2023·连云港中考)在三颈烧瓶中用排空气法收集CO2气体,然后将三颈烧瓶与盛有盐酸、NaOH溶液的注射器和压强传感器密封连接(如图1)。检验气密性后,在t0时快速注入一种溶液,t2时快速注入第二种溶液,测得瓶内压强随时间变化曲线如图2。下列说法中正确的是 ( )
A.t0时注入的溶液是盐酸B.t1前压强减小对应的反应示意图如图3所示C.t1~t2期间压强不变且大于0可证明收集的CO2气体不纯D.t2后压强增大的原因是NaOH溶液与盐酸发生中和反应
3.(2022·福建中考)兴趣小组用稀盐酸清洗铁夹表面的铁锈(主要成分为氧化铁),并进行保护实验。(1)除铁锈的反应属于________________(填基本反应类型)。 (2)铁夹在稀盐酸中浸泡较长时间,有气体产生。产生气体的化学方程式为__________________________。 (3)将清洗过的铁夹进行“发蓝”处理,形成致密的氧化物保护膜,其主要成分与铁在氧气中燃烧的产物相同,该氧化物的化学式为___________。
Fe+2HCl===FeCl2+H2↑
(4)验证废液显酸性,可选用的一种试剂或用品是______________________________。 (5)用氢氧化钠中和废液中的盐酸,反应的化学方程式为 ___________________________。
pH试纸(或紫色石蕊溶液等)
HCl+NaOH===NaCl+H2O
4.(2022·济南中考节选)实验室中有两瓶失去标签的无色溶液,已知是NaOH溶液和Ca(OH)2溶液中的各一种,小明和小红同学想用化学方法确定各是哪种溶液,并进行了实验探究。(1)小明各取两种无色溶液少许,分别加入A、B两支试管中,用干净的长塑料管分别向两试管中的溶液里慢慢吹气,观察到A试管中有白色浑浊现象,B试管中无明显现象。则可判断A试管中加入的是_____________(填化学式)溶液。 (2)小红从下列四种试剂中选取了一种试剂,进行鉴别实验,根据明显现象也成功鉴别了上述两种无色溶液。则小红所选的这种试剂是_______(填选项序号之一)。 A.酚酞试液 B.稀盐酸C.Na2CO3溶液D.NaCl溶液
5.(2023·广州中考)通过观察和实验等方法获取证据是科学探究的重要环节。(1)向少量Fe(OH)3沉淀中加入稀盐酸,观察到______________________________,可判断发生了反应。 (2)向Ca(OH)2溶液中通入CO2,观察到________________,可判断发生了反应。
固体溶解或溶液由无色变为黄色
(3)向氢氧化钙溶液中滴加稀盐酸,无明显现象。两位同学欲获取反应发生的证据。①甲同学向滴有酚酞溶液的氢氧化钙溶液中逐滴滴加稀盐酸至足量,溶液由红色变成无色,证明溶液中____________________,可判断Ca(OH)2与HCl发生了反应。 ②乙同学将氢氧化钙溶液与稀盐酸混合,然后检验出混合液中含有Ca2+和Cl-,他据此认为Ca(OH)2与HCl发生了反应,且生成了CaCl2。你认为乙同学是否找到了反应发生的证据,请说出你的观点并阐述理由:________________________________________________________________________________________________________________。
没有找到反应发生的证据,
因为氢氧化钙溶液中有钙离子、盐酸中有氯离子,混合后即使不反应也会存在
2024中考一轮复习 鲁教版化学 教材基础复习 第三单元 第一节 溶液的形成 课件: 这是一份2024中考一轮复习 鲁教版化学 教材基础复习 第三单元 第一节 溶液的形成 课件,共50页。PPT课件主要包含了知识清单·理脉络,溶解与乳化,溶质质量分数,75g,25g,考点突破·释疑难,实验探究·培素养,配制方法与步骤,托盘天平,玻璃棒等内容,欢迎下载使用。
2024中考一轮复习 鲁教版化学 教材基础复习 第三单元 第二节 溶液组成的定量表示 课件: 这是一份2024中考一轮复习 鲁教版化学 教材基础复习 第三单元 第二节 溶液组成的定量表示 课件,共53页。PPT课件主要包含了知识清单·理脉络,溶解度及溶解度曲线,氯化钾,BCD,考点突破·释疑难,不饱和,降温结晶,五四制地区5年真题,375%,分解反应等内容,欢迎下载使用。
2024中考一轮复习 鲁教版化学 教材基础复习 第六单元 第一节 燃烧与灭火 课件: 这是一份2024中考一轮复习 鲁教版化学 教材基础复习 第六单元 第一节 燃烧与灭火 课件,共50页。PPT课件主要包含了知识清单·理脉络,燃烧与灭火,①②④,考点突破·释疑难,实验探究·培素养,实验设计,着火点,燃烧需要与,充足氧气接触,物质具有可燃性等内容,欢迎下载使用。












