
2024年山东省枣庄市滕州市中考模拟化学试卷7
展开
这是一份2024年山东省枣庄市滕州市中考模拟化学试卷7,共5页。试卷主要包含了选择题,填空题,实验题,计算题等内容,欢迎下载使用。
一、选择题
1.材料的应用与发展丰富了人们的生活。下列物品主要用有机合成材料制成的是( )
A.塑料水盆B.纯棉毛巾C.陶瓷餐具D.黄金饰品
2.水是生命之源,人类的生产生活都离不开水。下列有关水的认识错误的是( )
A.地球上可利用的淡水资源有限 B.过滤可以除去水中的所有杂质
C.水是由氢元素和氧元素组成的 D.用淘米的水浇花可以节约用水
3.荧光灯内的白色粉末涂层是一种叫钨酸钙(CaWO4)的化合物,如图所示为钨元素在元素周期表中的部分信息。下列分析正确的是( )
A.钨原子中的质子数为74 B.一个钨原子的质量为183.8g
C.CaWO4中非金属元素有两种D.CaWO4中钨元素的化合价为0
4.《天工开物》中记载了用黏土烧制砖的过程,如图所示为该过程中某反应的示意图(其中“”“”和“”分别代表不同元素的原子)。则微粒X中( )
A.只含有 B.一定含有和
C.一定含有和 D.一定含有、和
5.20℃和60℃时KCl的溶解度分别为34.0g和45.5g,如图所示为对KCl进行的溶解实验。下列分析错误的是( )
A.①中溶液为KCl的饱和溶液
B.②中溶液的质量为25.0g
C.溶液中溶质的质量:①<②=③ D.溶液中溶质的质量分数:①<②=③
6.向盛有ag铜锌混合物的烧杯中加入稀硫酸,该过程中剩余固体与加入稀硫酸的质量关系如图所示。下列说法错误的是( )
A.M点时,溶液中的溶质只有ZnSO4
B.N点时,生成气体的总质量达到最大
C.N→P过程中,溶液的pH逐渐增大
D.该铜锌混合物中锌的质量为(a﹣b)g
7.党的二十大报告中提出“持续深入打好蓝天、碧水、净土保卫战”。下列做法不符合这一要求的是( )
A.坚持绿色出行,践行低碳生活 B.秸秆粉碎还田,增加农田肥料
C.垃圾分类回收,减少资源浪费 D.废弃电池深埋,防止土壤污染
8.河北历史悠久,文化源远流长。下列工艺中一定包含化学变化的是( )
A.剪窗花B.酿白洒C.刻石雕D.晒海盐
9.在塑料袋中滴入几滴酒精,挤瘪后把口扎紧,放入热水中,塑料袋鼓起来,如图所示。鼓起的过程中,塑料袋中酒精分子的( )
A.间隔增大B.质量增大C.种类增多D.数目增多
10.分类是认识和研究问题的重要方法之一,下列分类正确的是( )
A.萘和石蜡都是非晶体 B.银和铜都是导体
C.Al2O3和NaHCO3都是盐 D.(NH4)2SO4和CO(NH2)2都是铵态氮肥
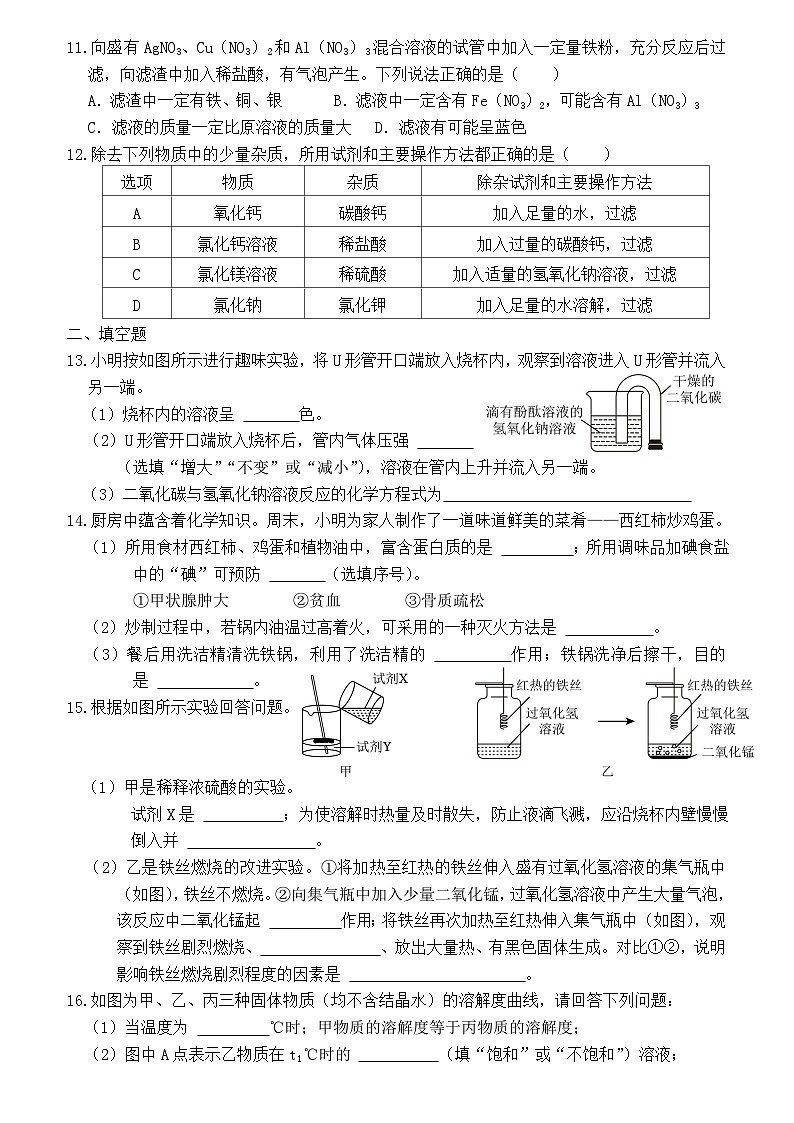
11.向盛有AgNO3、Cu(NO3)2和Al(NO3)3混合溶液的试管中加入一定量铁粉,充分反应后过滤,向滤渣中加入稀盐酸,有气泡产生。下列说法正确的是( )
A.滤渣中一定有铁、铜、银 B.滤液中一定含有Fe(NO3)2,可能含有Al(NO3)3
C.滤液的质量一定比原溶液的质量大D.滤液有可能呈蓝色
12.除去下列物质中的少量杂质,所用试剂和主要操作方法都正确的是( )
二、填空题
13.小明按如图所示进行趣味实验,将U形管开口端放入烧杯内,观察到溶液进入U形管并流入另一端。
(1)烧杯内的溶液呈 色。
(2)U形管开口端放入烧杯后,管内气体压强
(选填“增大”“不变”或“减小”),溶液在管内上升并流入另一端。
(3)二氧化碳与氢氧化钠溶液反应的化学方程式为
14.厨房中蕴含着化学知识。周末,小明为家人制作了一道味道鲜美的菜肴——西红柿炒鸡蛋。
(1)所用食材西红柿、鸡蛋和植物油中,富含蛋白质的是 ;所用调味品加碘食盐中的“碘”可预防 (选填序号)。
①甲状腺肿大 ②贫血 ③骨质疏松
(2)炒制过程中,若锅内油温过高着火,可采用的一种灭火方法是 。
(3)餐后用洗洁精清洗铁锅,利用了洗洁精的 作用;铁锅洗净后擦干,目的是 。
15.根据如图所示实验回答问题。
(1)甲是稀释浓硫酸的实验。试剂X是 ;为使溶解时热量及时散失,防止液滴飞溅,应沿烧杯内壁慢慢倒入并 。
(2)乙是铁丝燃烧的改进实验。①将加热至红热的铁丝伸入盛有过氧化氢溶液的集气瓶中(如图),铁丝不燃烧。②向集气瓶中加入少量二氧化锰,过氧化氢溶液中产生大量气泡,该反应中二氧化锰起 作用;将铁丝再次加热至红热伸入集气瓶中(如图),观察到铁丝剧烈燃烧、 、放出大量热、有黑色固体生成。对比①②,说明影响铁丝燃烧剧烈程度的因素是 。
16.如图为甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,请回答下列问题:
(1)当温度为 ℃时;甲物质的溶解度等于丙物质的溶解度;
(2)图中A点表示乙物质在t1℃时的 (填“饱和”或“不饱和”)溶液;
(3)若甲中含有少量乙时,可以采用 (填“降温结晶”或“蒸发结晶”)的方法提纯甲;
(4)将t2℃时接近饱和的丙溶液变成饱和溶液,下列方法不能达到目的的是 ;
A.蒸发溶剂 B.降低温度 C.增加溶质 D.升高温度
(5)将t2℃时甲的饱和溶液100g稀释成溶质质量分数为25%的溶液,
需加水的质量为 g。
17.金属与金属材料在人类文明进步和社会发展中起着至关重要的作用。回答下列问题:
(1)利用物理方法可以把黄金压成厚度只有1/10000mm的薄片,说明金具有良好的______(填字母)。 A. 金属光泽 B. 导电性 C. 延展性D. 导热性
(2)在钢铁制品表面刷油漆可防止锈蚀,其原因是 。
(3)某同学设计右上图所示实验方案,验证铁、铜、银三种金属的活动性强弱。能证明铁的金属活动性比铜强的实验现象是 ;要验证铜的金属活动性比银强,试管C中应加入 (填化学式)溶液。
三、实验题
18.自然界中的铝元素以化合物的形式存在于各种矿石中、某铝土矿的主要成分是,含少量等杂质。从该铝土矿中提取铝可采用如下工艺流程(不考虑杂质参与反应):
已知:不溶于水且不与盐酸反应;能与溶液反应,生成可溶性盐。
请回答下列问题。
(1)步骤①加盐酸前先将铝土矿粉碎的目的是 ;所得滤液A中的溶质有___种。
(2)步骤②中所加溶液须过量的目的是 。
(3)步骤③加热分解生成两种氧化物,请写出该反应的化学方程式 。
(4)步骤④是通过电解熔融状态的制备铝。的熔点是,很难达到熔融状态,工业上通过加入冰晶石使其在左右熔化,请写出这一做法的意义______。
19.气体的实验室制备是学生必备的实验技能,以下是实验室用于制取气体的部分装置,回答下列问题。
(1)仪器①名称为 。
(2)实验室用过氧化氢溶液和二氧化锰制取氧气,应选用的发生装置是 (填字母),反应的化学方程式为 。
(3)实验室用大理石和稀盐酸制取二氧化碳,反应的化学方程式为 。若使用装置C收集二氧化碳,将燃着的木条放在导管口______(填“a”或“b”)处,观察到 则证明气体已经收集满。
(4)实验室制取少量氢气时,可选用装置D或E收集。由此推断,氢气具有的物理性质是
。
20.纯碱在工业生产中用途极广,广泛应用于冶金、造纸、纺织、印染和洗涤剂生产等领域。某化学兴趣小组的同学在预习了纯碱的相关知识后,对纯碱的制备和部分化学性质展开项目式学习,并对部分实验废液进行了拓展探究。任务一:了解纯碱的制备——“侯氏制碱法”
“侯氏制碱法”的主要过程是利用饱和食盐水先后吸收两种气体,生成碳酸氢钠和氯化铵,再加热碳酸氢钠即可制得纯碱。
(1)“侯氏制碱法”中的“侯氏”指的是我国著名化学家 ;
(2)“侯氏制碱法”的主要过程中需要吸收的两种气体是 (填字母序号);
A.Cl2 B.NH3 C.SO2 D.CO2
任务二:探究纯碱与酸、碱、盐的反应
向盛有一定量纯碱溶液的三支试管中分别加入稀盐酸、澄清石灰水、氯化钡溶液,实验现象记录如下:
任务三:对部分废液的拓展探究
化学兴趣小组的同学将实验后试管2和试管3中的物质分别进行过滤,得到滤液甲和饱液乙。
[提出问题] 滤液乙中的溶质是什么?
[猜想与假设]猜想一:氯化钠; 猜想二:氯化钠和碳酸钠; 猜想三: 。
[进行实验]
[拓展延伸]基于以上探究结论,同学们取一定量的滤液甲和滤液乙于小烧杯中混合;发现有白色沉淀产生,试写出该反应的化学方程式 。
四、计算题
21.某化学兴趣小组欲测定一瓶失去标签的硫酸铜溶液的溶质质量分数,取该溶液20g,逐滴加入氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液质量的关系如图所示。计算硫酸铜溶液的溶质质量分数。
选项
物质
杂质
除杂试剂和主要操作方法
A
氧化钙
碳酸钙
加入足量的水,过滤
B
氯化钙溶液
稀盐酸
加入过量的碳酸钙,过滤
C
氯化镁溶液
稀硫酸
加入适量的氢氧化钠溶液,过滤
D
氯化钠
氯化钾
加入足量的水溶解,过滤
试管编号
1
2
3
加入试剂
稀盐酸
澄清石灰水
氯化钡溶液
实验现象
产生白色沉淀
产生白色沉淀
实验操作
实验现象
实验结论
取少量滤液乙于试管中,加入适量稀硫酸
猜想三成立
相关试卷
这是一份2024年山东省枣庄市滕州市中考模拟化学试卷1,共4页。试卷主要包含了下列物质中属于纯净物的是,“端午时节粽飘香,归纳与总结是学习化学的基本方法等内容,欢迎下载使用。
这是一份2024年山东省枣庄市滕州市中考模拟化学试卷2,共4页。试卷主要包含了常用来区分硬水和软水的试剂是,空气是人类生产活动的重要资源,下列实验设计能达到实验目的的是,推理是化学学习中常用的思维方法等内容,欢迎下载使用。
这是一份2024年山东省枣庄市滕州市中考模拟化学试卷3,共4页。试卷主要包含了硫酸是实验室常用的化学试剂,下列试剂实验室保存方法错误的是等内容,欢迎下载使用。









