






2024年广东省中考化学一轮知识点梳理复习课时10:溶液(二)——溶液的计算课件PPT
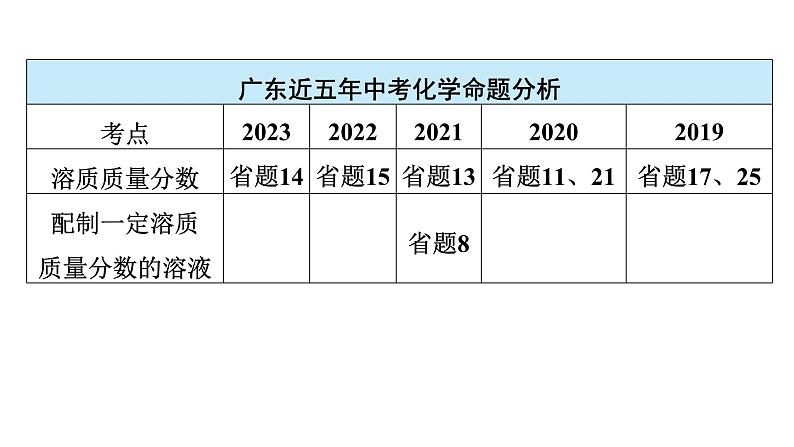
展开知识点1 溶液的浓度的计算与比较(1)溶质的质量分数:用溶质的质量占全部溶液质量的百分比来表示溶液的浓度。 (2)溶质的质量分数(c%)=_____________×100%=_________________________×100%即c%=m(溶质)/m(溶液)×100%。则m(溶质)=______________=_________________________
V(溶液)·ρ(溶液)·c%
(3)饱和溶液的溶质质量分数对于一定温度下的饱和溶液,其溶质质量分数还可利用该温度下的溶解度(S)进行计算:饱和溶液溶质质量分数=________________。
知识点2 溶液的稀释与配制(1)溶液的稀释:计算原理:稀释前后溶液中____________不变。①加水稀释:m(稀液)×c%(稀液)=____________________,m(稀液)=m(浓液)+m(加水),即m(加水)=m(稀液)-m(浓液)。②浓溶液混合稀溶液:m(浓液)×c%(浓液)+m(稀液)×c%(稀液)=[m(浓液)+m(稀液)]×c%(混合后)
m(浓液)×c%(浓液)
(2)配制一定溶质质量分数的氯化钠溶液配制溶液一般分以下几步进行:
①计算:正确的计算出所需溶质的______和水的______。②称量:一般用__________准确地称取氯化钠的质量,再用合适的______量取水的体积。③溶解:把称得的固体和量得的水倒入烧杯,并用________搅拌直至完全溶解为止。④装瓶:最后将配好的溶液倒入清洁的试剂瓶,并贴上标签,并写明“×%的××溶液”。
知识点3 与化学方程式结合进行的计算对于这类问题,抓住两条线索,第一条线索是物质,弄清楚物质之间是什么关系,是生成物还是反应物;第二条线索是数字,弄清楚数字的含义,有些数字是迷惑我们的。计算溶液的质量时,生成的气体和沉淀不可以计算在内。
【特别提醒】①在一定温度下,同一种溶质其饱和溶液的溶质质量分数比不饱和溶液的大。②配制一定溶质质量分数的溶液,装瓶过程中有少量溶液洒出来,对所配溶液的溶质质量分数无影响。
1.(省题)判断下列说法是否正确,正确的打“√”,错误的打“×”。(1)将10%的KNO3溶液倒出一半,剩余溶液中溶质的质量分数为20%。( )(2)将25 g KCl溶液蒸干得到5 g KCl固体,则原溶液中溶质的质量分数为20%。( )(3)将10 g硝酸钾完全溶于100 g水中可配制成10%的硝酸钾溶液。( )
(4)将某溶液的浓度增大一倍,可采用将溶剂蒸发掉一半的方法(无晶体析出)。( )(5)用50 g 10%的NaCl溶液配制5%的NaCl溶液需要加水50 g。( )(6)向饱和KNO3溶液中加入KMnO4固体的图像如下图。( )
2.(2023·苏州)在配制50 g溶质质量分数为2%的碳酸钠溶液的实验中,一定不需要用到的仪器是( )A.漏斗B.玻璃棒C.50 mL量筒D.烧杯
3.(2023·宜昌)实验室配制一定溶质质量分数的氯化钠溶液,下列操作错误的是( )
4.如图所示是实验室配制一定溶质质量分数的NaCl溶液的流程图。回答下列问题。(1)应称量_____ g NaCl,需加水______ mL。(2)若称量NaCl固体时指针向右偏转,则应______________________直到天平平衡。(3)取上述溶液10 g加水稀释到____ g,可得到5%的NaCl溶液。
重难点突破1:溶液的稀释 饱和溶液用水稀释变成不饱和溶液的过程中,保持不变的是( )A.溶质的质量B.溶剂的质量C.溶液的质量D.溶质的质量分数
饱和溶液用水稀释变成不饱和溶液的过程中,溶质质量不变,溶剂质量增加,溶液的质量增加,溶质的质量分数变小。
工业上常用10%的稀硫酸去除铁器表面的铁锈。为了配制50千克10%的稀硫酸,问:(1)需要98%的浓硫酸多少千克?解:根据m(溶质)=m(溶液)·c%稀溶液中溶质的质量=50 kg×10%设需要98%浓溶液质量为x,则溶质质量为x·98%。即x·98%=50 kg×10%x=5.1 kg
(2)需要加水多少千克?解:m(加水)=m(稀溶液)-m(浓溶液)=50 kg-5.1 kg=44.9 kg。
把98%的浓硫酸加水稀释成10%的稀硫酸,根据稀释原则,稀释前后,溶质的质量是不变的,稀溶液质量增加了多少,即为加入的水的质量。
(2023·广州模拟)把50 g质量分数为98%的浓硫酸稀释为质量分数为20%的稀硫酸,需加水( )A.245 gB.195 gC.49 gD.196 g 需要500 g 6%的过氧化氢溶液制取氧气,需用多少30%的过氧化氢溶液来稀释配制( )A.50 gB.100 gC.200 gD.300 g
一定溶质质量分数的氯化钠溶液的配制1.实验目的:学习配制一定溶质质量分数的溶液。2.实验仪器:托盘天平、药匙、烧杯、量筒、玻璃棒、胶头滴管、细口瓶。3.实验药品:氯化钠、蒸馏水。
4.实验步骤:(1)用固体药品配制溶液(以配制50 g 6%的氯化钠溶液为例)①计算:所需氯化钠质量为___ g,所需蒸馏水的体积为___ mL(水的密度约为1 g/mL)。②称量:分别在天平左右两盘放上纸片,调节平衡后,称量。
③量取:用规格为____ mL的量筒准确量取所需蒸馏水,倒入盛有固体的烧杯中。④溶解:用玻璃棒搅拌,使固体完全溶解。该操作中玻璃棒的作用是__________。⑤装瓶、贴标签:将配制好的溶液转移到试剂瓶中,盖上瓶塞并贴好标签。(标签写上__________和______________)
(2)浓溶液配制稀溶液(用6%的氯化钠溶液,其密度为1.04 g/mL,配制50 g 3%的氯化钠溶液)①计算:所需6%的氯化钠溶液的质量为____ g(体积为____ mL),所需蒸馏水的质量为____ g(体积为____ mL)。②量取:用量筒分别量取浓溶液和水,倒入烧杯中。③混匀:用玻璃棒搅拌,使溶液混合均匀。④装瓶、贴标签
5.反思:误差分析(1)导致溶液的溶质质量分数偏小的原因①天平使用不正确,如药品、砝码放反并且使用了游码;②量取水的过程中仰视读数,取水量偏多;③烧杯中原来就有水;④固体中含有杂质。(2)导致溶液的溶质质量分数偏大的原因①称量前天平偏右,导致药品偏多;②砝码已生锈;③量取水时俯视读数,量取水偏少;④将量筒中的水倒入烧杯中时有少量洒出。
配制一定溶质质量分数的氯化钠溶液的过程如下图所示:(1)写出图中标号a仪器的名称:______。(2)配制80 g质量分数为15%的氯化钠溶液,所需氯化钠和水的质量分别为:氯化钠____ g,水____ mL。(3)图示实验中有一处明显的错误是____(填序号)。(4)称量氯化钠时,氯化钠应放在托盘天平的____(填“左”或“右”)盘。
(5)溶解过程中玻璃棒的作用是______________________。(6)对配制的溶液进行检测发现溶质质量分数偏大,其原因可能有____。(填序号)A.称量时,药品与砝码放反了B.量取水的体积时,俯视读数C.装瓶时,有少量溶液洒出(7)把50 g质量分数为15%的氯化钠溶液稀释成5%的氯化钠溶液,需要水的质量是_____ g。
溶液的稀释与配制1.如图是配制100 g溶质质量分数为10%的NaCl溶液的实验操作示意图。(1)配制溶液的正确操作顺序是____________(填序号)。(2)图②中,有一种塑料仪器,其名称是______。
(3)量取所需要的水应选择________(填“50 mL”“100 mL”或“200 mL”)的量筒。(4)称量时发现指针向左偏,应进行的操作是__________________________________。
减少NaCl的质量直至托
(5)能导致溶液中NaCl质量分数小于10%的可能的原因是______(多选)。A.称量时NaCl与砝码放反了(1 g以下用游码)B.砝码生锈C.用量筒量取水时仰视读数D.NaCl中含有可溶性杂质
2.(2022·东莞模拟)实验室配制50 g溶质质量分数为6%的氯化钠溶液的步骤是( )A.计算、溶解、称量、贮存B.称量、贮存、计算、溶解C.计算、称量、溶解、贮存D.计算、贮存、称量、溶解
3.下列是小刚“配制50 g溶质质量分数为6%的氢氧化钠溶液”的实验过程,其中正确的是( )A.计算需要氢氧化钠3 g、水47 gB.将氢氧化钠放在托盘天平左盘的纸上称量C.将称取的氢氧化钠放入量筒中溶解D.将配制好的溶液转移一半后,小刚认为剩余溶液溶质质量分数为3%
与化学方程式结合的溶液计算4.(2023·威海)某化学兴趣小组欲测定一瓶失去标签的硫酸铜溶液的溶质质量分数,取该溶液20 g,逐滴加入氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液质量的关系如图所示。计算硫酸铜溶液的溶质质量分数。
解:由图像可知产生Cu(OH)2的质量为1.96 g,设硫酸铜溶液中硫酸铜的质量为x。CuSO4+2NaOH===Na2SO4+Cu(OH)2↓160 98x 1.96 g 答:硫酸铜溶液的溶质质量分数为16%。
5.请回答并完成下列计算。(1)实验室要配制50 g溶质质量分数为8%的氢氧化钠溶液,需称取___ g氢氧化钠固体。
(2)向上述配制好的溶液中加入50 g稀硫酸,恰好完全反应,求反应后所得溶液中溶质的质量分数。解:设反应后所得溶液中溶质的质量分数为x。2NaOH+H2SO4===Na2SO4+2H2O80 1424 g (50 g+50 g)x 答:反应后所得溶液中溶质的质量分数为7.1%
6.★★(2022·泰安)黄铜(铜、锌合金)具有合金的特性,可以用来制造机器零件。某学习小组的同学为了测定黄铜中铜的含量,取黄铜样品25 g放入烧杯中,再将160 g稀硫酸分4次加入烧杯中,充分反应后,分别测得剩余固体的质量记录如下。
请根据实验数据完成下列问题:(1)m的值为____。(2)黄铜样品中铜的质量分数为______。
2024年广东省中考化学一轮知识点梳理复习课时15:金属和金属材料(二)——金属的化学性质课件PPT: 这是一份2024年广东省中考化学一轮知识点梳理复习课时15:金属和金属材料(二)——金属的化学性质课件PPT,共46页。PPT课件主要包含了考情分析,知识梳理,金属活动性逐渐减弱,基础演练,难点突破,真题演练,素养提升等内容,欢迎下载使用。
2024年广东省中考化学一轮知识点梳理复习课时11:空气 氧气课件PPT: 这是一份2024年广东省中考化学一轮知识点梳理复习课时11:空气 氧气课件PPT,共60页。PPT课件主要包含了考情分析,知识梳理,空气和氧气,空气的成分,03%,94%,稀有气体,不活泼,很不活泼,保护气等内容,欢迎下载使用。
2024年广东省中考化学一轮知识点梳理复习课时9:溶液(一)——溶解度课件PPT: 这是一份2024年广东省中考化学一轮知识点梳理复习课时9:溶液(一)——溶解度课件PPT,共45页。PPT课件主要包含了考情分析,知识梳理,基础演练,难点突破,真题演练,素养提升等内容,欢迎下载使用。












