



广东省部分学校2024届高三百日冲刺联合学业质量监测(一模)化学试题(一模+一模)
展开
这是一份广东省部分学校2024届高三百日冲刺联合学业质量监测(一模)化学试题(一模+一模),文件包含广东省部分学校2024届高三百日冲刺联合学业质量监测一模化学试题原卷版docx、广东省部分学校2024届高三百日冲刺联合学业质量监测一模化学试题解析版docx等2份试卷配套教学资源,其中试卷共31页, 欢迎下载使用。
考生注意:
1.满分100分,考试时间75分钟。
2.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
3.本卷命题范围:高考范围。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Fe 56 Zn 65
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分,第11~16小题,每小题4分。在每小题给出的四个选项中,只有一个选项是符合题目要求的。
1. 起源于西汉的丝绸之路是最早的东西文明交流通道。下列商品的主要成分是金属材料的是
A. AB. BC. CD. D
2. 科学技术是第一生产力,下列说法错误的是
A. 被称为“黑金”的新型纳米材料石墨烯属于无机非金属材料
B. 日本福岛核电站排放核污水的2种放射性同位素和中子数相同
C. 1965年,我国科学家在世界上第一次用化学方法合成了结晶牛胰岛素
D. “深地一号”为进军万米深度提供核心装备,制造钻头用的金刚石为共价晶体
3. 化学与人类生产、生活、科研密切相关,下列有关说法正确的是
A. PM2.5是指空气中直径接近的颗粒物,其分散在空气中形成胶体
B. 维生素C用作食品中的防腐剂,是因为维生素C有较强的氧化性
C. 蒸馏“地沟油”可以获得汽油
D. 推广使用可降解塑料,能减少白色污染
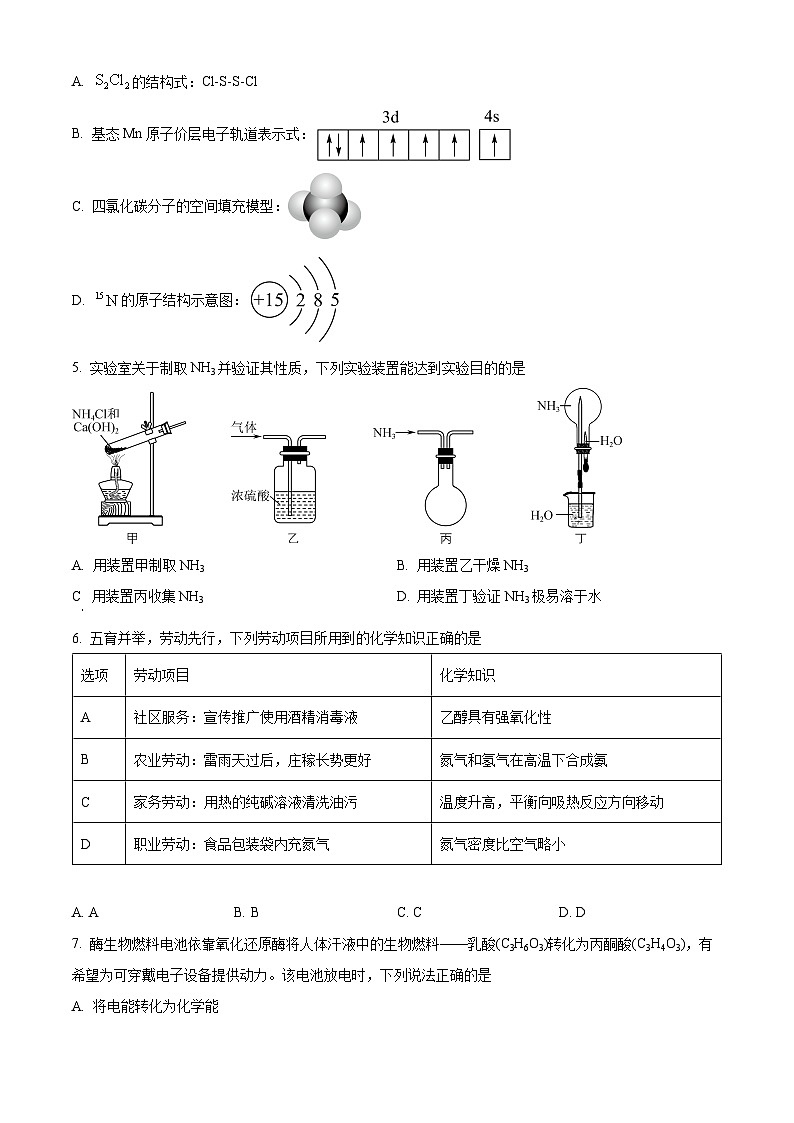
4. 下列化学用语表达正确的是
A. 的结构式:Cl-S-S-Cl
B. 基态Mn原子价层电子轨道表示式:
C. 四氯化碳分子的空间填充模型:
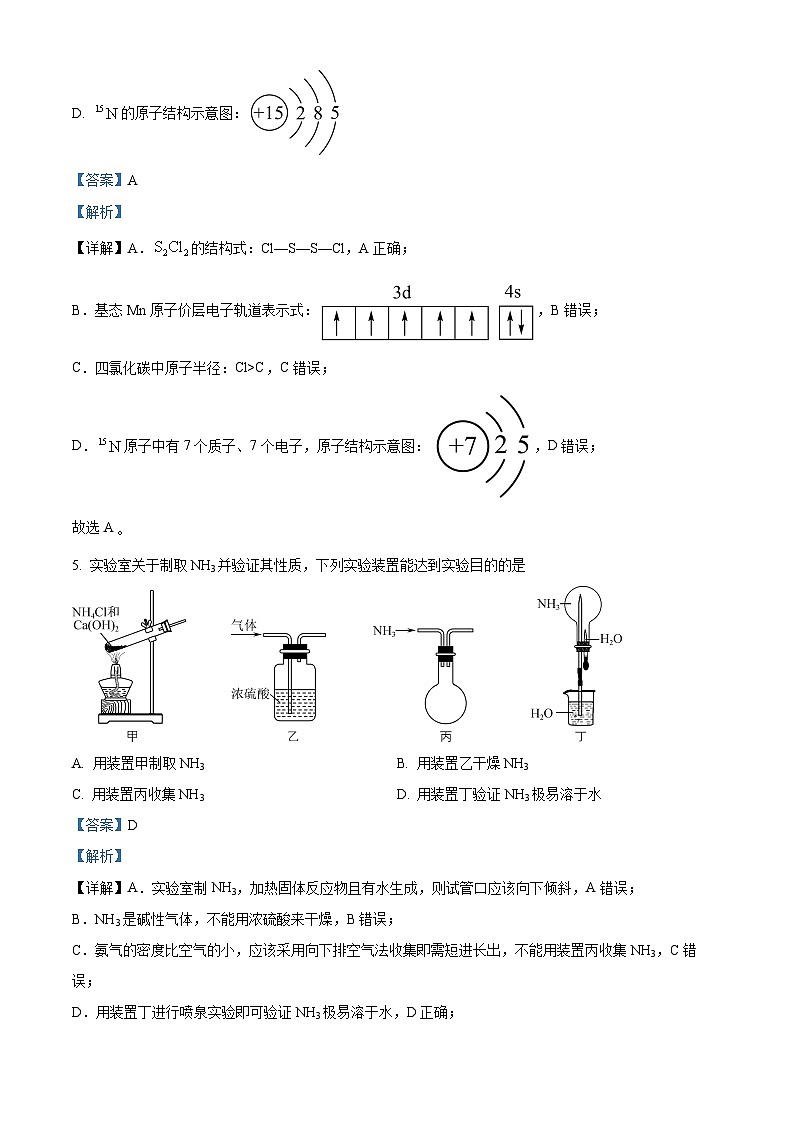
D. 的原子结构示意图:
5. 实验室关于制取NH3并验证其性质,下列实验装置能达到实验目的的是
A. 用装置甲制取NH3B. 用装置乙干燥NH3
C 用装置丙收集NH3D. 用装置丁验证NH3极易溶于水
6. 五育并举,劳动先行,下列劳动项目所用到的化学知识正确的是
A. AB. BC. CD. D
7. 酶生物燃料电池依靠氧化还原酶将人体汗液中的生物燃料——乳酸(C3H6O3)转化为丙酮酸(C3H4O3),有希望为可穿戴电子设备提供动力。该电池放电时,下列说法正确的是
A. 将电能转化为化学能
B. 电子移动方向:正极→汗液→负极
C. 正极上发生氧化反应
D. 乳酸在负极上失去电子
8. 下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是
A. AB. BC. CD. D
9. 部分含N物质及含S物质的分类与相应化合价之间的关系如图所示,下列推断错误的是
A. c′和d′分子中硫原子的杂化方式相同
B. c′通入到紫色石蕊溶液中,溶液只变红不褪色
C. 用两根玻璃棒分别蘸取浓的a溶液和浓的e′溶液,将两根玻璃棒靠近时有白烟产生
D. 常温下,可以用铁或铝制容器来盛装浓的e或e′溶液
10. 设为阿伏加德罗常数的值,下列说法错误的是
A. 50g质量分数为64%的甲醇水溶液中含有σ键数目为5
B. 一定条件下,5.6g Fe与0.1ml 充分反应,转移的电子数为0.2
C. 浓硝酸热分解生成、共69g时,转移电子数为1.5
D. 常温下,1L pH=2的稀盐酸中含有的H+数目为0.01
11. 聚碳酸酯(简称PC)广泛应用于玻璃装配业、汽车工业和电子、电器工业等领域,其合成方法和分子结构如图所示,下列说法错误的是
A. 化合物B的分子式为
B. 化合物A分子中所有碳原子不可能共平面
C. 可通过溶液检验A和B是否完全反应
D. 产物C可用作消毒剂
12. 模拟氨催化氧化法制硝酸的装置如图所示(无水CaCl2可用于吸收氨气),下列说法错误的是
A. 装置①、②、⑤依次盛装碱石灰、无水CaCl2、NaOH溶液
B. 装置③中气体呈红棕色
C. 通空气的主要作用是鼓出氨气,空气可用N2代替
D. 装置④中溶液可使紫色石蕊溶液变红,说明有HNO3生成
13. 乙烯氢化的热化学方程式为 ,使用不同含Au催化剂的反应历程如图所示。下列说法错误的是
A. 1ml 的能量小于1ml 与1ml 具有的能量之和
B. 该反应的焓变:
C. 过渡态物质的稳定性:过渡态1>过渡态2
D. 相应的活化能:催化剂AuF>催化剂
14. 美托拉宗临床用于治疗水肿及高血压,如图所示有机化合物是制备美托拉宗中间产物,其组成元素Z、X、Y、Q、M、W为原子序数依次增大的短周期非金属元素,X、Y、Q为同周期相邻元素。下列说法正确的是
A. 溶液在酸性条件下会产生黄色浑浊固体和无色气体
B. 该有机物中,各原子均满足8电子稳定结构
C. 元素X、Y、Qp电子总数均小于s电子总数
D. M、W均可与Q形成原子个数比为1∶2的化合物,两者漂白原理相同
15. 常温下,向10mL 0.1 溶液中滴入0.1 溶液,滴加过程中溶液中随滴入溶液体积的变化如图所示。下列叙述正确的是
A. 0.1的溶液中:
B. b点溶液中:
C. a、b、c三点溶液中,b点水的电离程度最大
D. c点溶液中:
16. 用如图装置电解制取,温度控制在10℃左右,持续通入,电解前后物质的量基本不变。下列说法正确的是
A. 电解过程中的移动方向是:甲室→乙室
B. 甲室产生的气体只有
C. 乙室电极反应为
D. 当乙室产生的气体体积为11.2L时,外电路转移电子数为4
二、非选择题:本题共4小题,共56分。
17. 硫代乙醇酸()可用作毛毯整理剂及冷烫液的原料,工业上可利用反应制备,实验室设计如图装置进行相关模拟实验(夹持装置省略)。
已知:(熔点-16.5℃、沸点123℃)在空气中迅速被氧化,在较高温度下受热分解产生有毒的硫化物烟气。
回答下列问题:
(1)可通过以下反应制备:。
①简述小于的原因:___________。
②属于___________(填“极性”或“非极性”)分子。
(2)该实验需要250mL 10ml/L NaOH溶液,配制该溶液时,下列操作正确的是___________(填标号)。
(3)检查完气密性后,关闭、、,添加实验药品,先制备NaHS。
①制备时,打开,使25%磷酸缓缓滴入浓溶液中,缓缓滴加优点是___________。
②实验时不能用25%硝酸代替装置A中25%磷酸的原因是___________。
③装置C的作用是___________。
④装置D中多孔球泡的作用是___________;写出装置D中刚开始反应的离子方程式:___________。
⑤经过一系列分离提纯可获得粗品,提纯需要采取减压精馏的原因是___________。
18. 是制造锌钡白和锌盐的主要原料,也可用作印染媒染剂,木材和皮革的保存剂。由菱锌矿(主要成分为,还含有少量:、、、、、PbO,、CdO和)制备流程如下:
已知:常温下,部分金属阳离子沉淀的pH如下表。
回答下列问题:
(1)加硫酸浸取后再调节pH=5,过滤获得的滤渣①的主要成分为、、、___________和___________。
(2)加入溶液后过滤可以得到和两种沉淀,发生反应的离子方程式为___________,常温下,此时溶液pH仍为5,则溶液残留的微量的浓度约为___________ml/L⋅,根据“转化过滤”过程,推测若Zn、稀硫酸、Cd形成原电池,则电势较高的一极为___________。
(3)“脱钙镁”后“过滤”所得的滤渣还可以和浓硫酸反应制备HF以循环使用,则该反应可以发生的原因是___________。
(4)脱完钙和镁之后的滤液中含有少量的,的溶解度曲线如图。由滤液④获得的具体操作为___________。
(5)ZnS存在如图所示的两种晶胞类型,则两种晶胞的密度之比为___________(用含a、b、c的代数式表示)。
19. 工业合成氨是人类科学技术的一项重大突破,选择高效催化剂实现降能提效是目前研究的重点。回答下列问题:
(1)合成氨反应为 ,理论上___________(填“高”或“低”,下同)温有利于提高反应速率,___________温有利于提高平衡转化率。
(2)合成氨反应在催化作用的化学吸附及初步表面反应历程如下:
注:方框内包含微粒种类及数目、微粒的相对总能量(括号里的数字单位:eV),TS表示过渡态,*表示吸附态。
①写出参与化学吸附的反应方程式:___________。
②以上历程须克服的最大能垒为___________eV。
(3)在t℃、压强为0.9MPa的条件下,向一恒压密闭容器中通入氢氮比为3的混合气体,体系中气体的含量与时间变化关系如图所示:
①反应20min达到平衡,试求0~20min内氨气的平均反应速率___________,该反应的___________(用数字表达式表示,为以分压表示的平衡常数,分压=总压×物质的量分数)。
②下列叙述能说明该条件下反应达到平衡状态的是___________(填标号)。
a.氨气的体积分数保持不变 b.容器中氢氮比保持不变
c.和的平均反应速率之比为1∶2 d.气体密度保持不变
③若起始条件相同,在恒容容器中发生反应,则达到平衡时H2的含量符合图中___________(填“d”“e”“f”或“g”)点。
20. 缓释布洛芬具有解热、镇痛、抗炎等功效,一种合成缓释布洛芬的路线如下:
回答下列问题:
(1)化合物Ⅰ的分子式为___________,缓释布洛芬的结构简式为___________。
(2)化合物Ⅱ易溶于水的原因是___________,化合物Ⅳ+Ⅴ→Ⅵ的反应类型是___________。
(3)根据化合物Ⅲ的结构特征,分析预测其可能的化学性质,完成下表。
(4)写出Ⅲ→Ⅳ的化学方程式:___________。
(5)同时满足下列条件的化合物Ⅴ的同分异构体共有___________种(不考虑立体异构),其中核磁共振氢谱中峰面积比为6∶3∶2∶2∶1的结构简式为___________。
①属于芳香族化合物;②苯环上含有两个取代基。商品
选项
A.纸张
B.铁器
C.丝绸
D.玉器
选项
劳动项目
化学知识
A
社区服务:宣传推广使用酒精消毒液
乙醇具有强氧化性
B
农业劳动:雷雨天过后,庄稼长势更好
氮气和氢气在高温下合成氨
C
家务劳动:用热的纯碱溶液清洗油污
温度升高,平衡向吸热反应方向移动
D
职业劳动:食品包装袋内充氮气
氮气密度比空气略小
选项
陈述Ⅰ
陈述Ⅱ
A
稀硝酸酸性比氢硫酸强
实验室用稀硝酸与FeS固体反应制取
B
淀粉遇变蓝色
碘易升华
C
氢氟酸能腐蚀玻璃
用塑料瓶或铅制容器保存HF
D
纯碱属于盐,可用于制玻璃
纯碱的焰色试验显黄色
操作
选项
a
b
c
d
金属阳离子
开始沉淀pH
6.2
7.4
2.2
7.7
9.1
8.1
3.4
沉淀完全pH
8.2
8.9
3.2
9.7
11.1
10.1
4.7
序号
结构特征
可反应的试剂
反应形成的新结构
反应类型
①
___________
___________、Ni
还原反应
②
___________
Na
___________
取代反应
相关试卷
这是一份2024广东省高三下学期百日冲刺联合学业质量监测试题(一模)化学含解析,共13页。试卷主要包含了满分100分,考试时间75分钟,本卷命题范围,下列化学用语表达正确的是,五育并举,劳动先行等内容,欢迎下载使用。
这是一份2024届广东省部分学校高三下学期百日冲刺联合学业质量监测(一模)化学试题+,共13页。试卷主要包含了满分100分,考试时间75分钟,本卷命题范围,下列化学用语表达正确的是,五育并举,劳动先行等内容,欢迎下载使用。
这是一份2024届广东部分学校高三百日冲刺联合学业质量监测(一模)化学试题,共13页。









