






还剩11页未读,
继续阅读
所属成套资源:全套人教版九年级化学上册单元课时教学课件
成套系列资料,整套一键下载
人教版九年级化学上册第3单元物质构成的奥秘课题2第2课时原子核外电子的排布与相对原子质量课件
展开
这是一份人教版九年级化学上册第3单元物质构成的奥秘课题2第2课时原子核外电子的排布与相对原子质量课件,共19页。
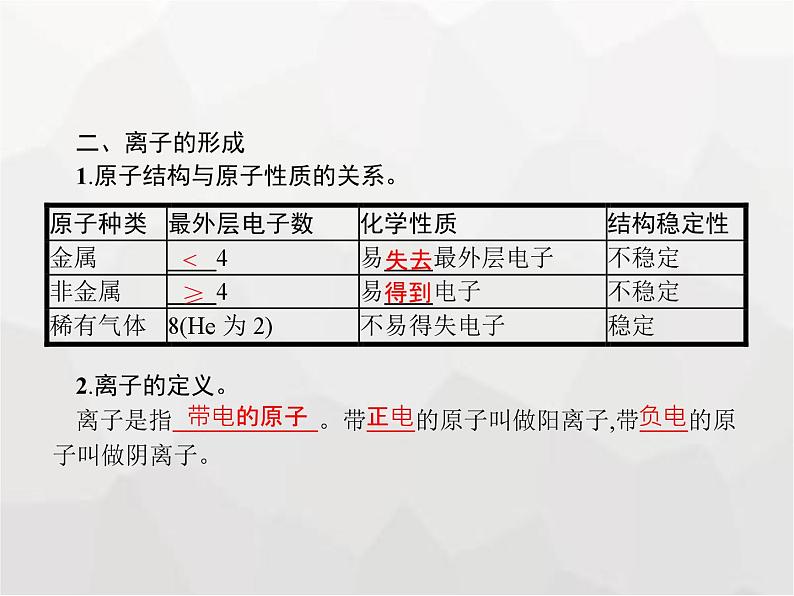
第2课时 原子核外电子的排布 与相对原子质量一、原子核外电子的排布1.核外电子的分层排布。在含有多个电子的原子中,核外电子具有不同的运动状态,离核近的电子能量较 ,离核越远,电子的能量越 。离核最近的电子层为第一层,次之为第二层,依次类推为第三、四、五、六、七层,离核最远的也叫 。核外电子的这种分层运动又叫分层排布。 2.电子层。原子核外电子最少的只有一层,最多的有七层,最外层电子不超过 个(只有一层的,电子不超过 个)。 低 高 最外层 8 2 3.原子结构示意图。上图是钠原子的原子结构示意图,圆圈及里面的数字表示 ;弧线表示 ;弧线上的数字表示 。 原子核以及核电荷数 电子层 该层的电子数 二、离子的形成1.原子结构与原子性质的关系。2.离子的定义。离子是指 。带 的原子叫做阳离子,带 的原子叫做阴离子。 < 失去 ≥ 得到 带电的原子 正电 负电 3.氯化钠的形成。每个钠原子失去1个电子,形成带一个单位正电荷的 ,每个氯原子得到1个电子,形成带一个单位负电荷的 。 和 相互作用形成了氯化钠。 如图所示:钠离子 氯离子 钠离子 氯离子 三、相对原子质量1.定义:以 作为标准,其他原子的质量与它相比较所得的比,作为这种原子的相对原子质量。 相对原子质量不是原子的实际质量,是一个比值。2.表达式:Ar= 3.与构成原子的粒子数之间的关系:相对原子质量≈ 数+ 数 质子 中子 一、原子结构示意图表达的信息原子中电子的排布通常用原子结构示意图表示。如:分析原子结构示意图获得的信息:(1)金属原子易失电子;(2)非金属原子易得电子;(3)稀有气体原子不易得电子,也不易失电子;(4)原子的化学性质主要是由原子的最外层电子数决定的。【例题1】 根据下列三种粒子结构示意图,所获取信息不正确的是( )A.②③化学性质相同B.②的结构是一种相对稳定的结构C.①表示的是原子,②表示的是离子D.③在化学反应中易失去最外层电子解析:本题考查同学们根据粒子的结构示意图中所给信息分析解题的能力。最外层的电子数是决定元素性质的主要因素,②③的最外层电子数不同,化学性质不同,A错误;②最外层有8个电子,该结构是一种相对稳定的结构,B正确;①中质子数=核外电子数,表示原子,②中质子数大于核外电子数,表示离子,C正确;③表示的原子的最外层电子数为3,小于4,易失去最外层电子,D正确。答案:A二、相对原子质量1.相对原子质量与原子质量的关系。原子质量和相对原子质量的关系,可用下图表示:2.近似计算。电子的质量相对于原子核来说很小,一个电子的质量约为一个中子或一个质子质量的 ,因此其质量可以忽略不计,所以原子的质量主要集中在原子核上,又因为质子和中子跟相对原子质量标准相比较,相对质量都约为1,所以可以得出:相对原子质量≈质子数+中子数。【例题2】 一种氧原子的相对原子质量为16,表示的意义是( )A.氧原子核中有16个质子B.一个氧原子的质量为16 gC.一个氧原子的质量是一个碳12原子质量的 的16倍D.一个氧原子的质量是一个碳12原子质量的16倍解析:相对原子质量是原子实际质量与标准的比值,不是核内质子数;相对原子质量不应带单位“g”;相对原子质量的标准是一个碳-12原子质量的 ,故选C。答案:C1.小美从某粒子结构示意图(如图)中,获取了下列信息,其中错误的是( )A.它有两个电子层 B.它的核电荷数为12C.它表示阴离子 D.它表示相对稳定结构 答案解析2.核电荷数大于核外电子数的粒子一定是( )A.分子 B.原子C.阴离子 D.阳离子 答案解析3.根据原子结构示意图,不能确定的是( )A.最外层电子数 B.中子数C.质子数 D.电子层数 答案4.已知某氧原子的相对原子质量为16,某硫原子的相对原子质量为32。如果该氧原子的质量为m,则该硫原子的质量为( )A.32m B.2mC.m D.不能确定 答案解析5.分析各组粒子结构示意图,与表示的意义一致的是( ) 答案解析6.已知一个碳-12原子的质量为1.993×10-26 kg,一个钬原子的质量是2.740×10-25kg,则钬的相对原子质量为 ;相同质量的钠、镁、铝含原子数目最多的是 (钠、镁、铝的相对原子质量分别是23、24、27)。 答案7.钠原子和氯原子的结构示意图如下:(1)氯原子的核电荷数是 。 (2)钠原子在化学反应中容易 (填“得到”或“失去”)一个电子。 (3)钠原子和氯原子相同的是 (填序号)。 ①质子数 ②电子数 ③电子层数 ④最外层电子数 答案
第2课时 原子核外电子的排布 与相对原子质量一、原子核外电子的排布1.核外电子的分层排布。在含有多个电子的原子中,核外电子具有不同的运动状态,离核近的电子能量较 ,离核越远,电子的能量越 。离核最近的电子层为第一层,次之为第二层,依次类推为第三、四、五、六、七层,离核最远的也叫 。核外电子的这种分层运动又叫分层排布。 2.电子层。原子核外电子最少的只有一层,最多的有七层,最外层电子不超过 个(只有一层的,电子不超过 个)。 低 高 最外层 8 2 3.原子结构示意图。上图是钠原子的原子结构示意图,圆圈及里面的数字表示 ;弧线表示 ;弧线上的数字表示 。 原子核以及核电荷数 电子层 该层的电子数 二、离子的形成1.原子结构与原子性质的关系。2.离子的定义。离子是指 。带 的原子叫做阳离子,带 的原子叫做阴离子。 < 失去 ≥ 得到 带电的原子 正电 负电 3.氯化钠的形成。每个钠原子失去1个电子,形成带一个单位正电荷的 ,每个氯原子得到1个电子,形成带一个单位负电荷的 。 和 相互作用形成了氯化钠。 如图所示:钠离子 氯离子 钠离子 氯离子 三、相对原子质量1.定义:以 作为标准,其他原子的质量与它相比较所得的比,作为这种原子的相对原子质量。 相对原子质量不是原子的实际质量,是一个比值。2.表达式:Ar= 3.与构成原子的粒子数之间的关系:相对原子质量≈ 数+ 数 质子 中子 一、原子结构示意图表达的信息原子中电子的排布通常用原子结构示意图表示。如:分析原子结构示意图获得的信息:(1)金属原子易失电子;(2)非金属原子易得电子;(3)稀有气体原子不易得电子,也不易失电子;(4)原子的化学性质主要是由原子的最外层电子数决定的。【例题1】 根据下列三种粒子结构示意图,所获取信息不正确的是( )A.②③化学性质相同B.②的结构是一种相对稳定的结构C.①表示的是原子,②表示的是离子D.③在化学反应中易失去最外层电子解析:本题考查同学们根据粒子的结构示意图中所给信息分析解题的能力。最外层的电子数是决定元素性质的主要因素,②③的最外层电子数不同,化学性质不同,A错误;②最外层有8个电子,该结构是一种相对稳定的结构,B正确;①中质子数=核外电子数,表示原子,②中质子数大于核外电子数,表示离子,C正确;③表示的原子的最外层电子数为3,小于4,易失去最外层电子,D正确。答案:A二、相对原子质量1.相对原子质量与原子质量的关系。原子质量和相对原子质量的关系,可用下图表示:2.近似计算。电子的质量相对于原子核来说很小,一个电子的质量约为一个中子或一个质子质量的 ,因此其质量可以忽略不计,所以原子的质量主要集中在原子核上,又因为质子和中子跟相对原子质量标准相比较,相对质量都约为1,所以可以得出:相对原子质量≈质子数+中子数。【例题2】 一种氧原子的相对原子质量为16,表示的意义是( )A.氧原子核中有16个质子B.一个氧原子的质量为16 gC.一个氧原子的质量是一个碳12原子质量的 的16倍D.一个氧原子的质量是一个碳12原子质量的16倍解析:相对原子质量是原子实际质量与标准的比值,不是核内质子数;相对原子质量不应带单位“g”;相对原子质量的标准是一个碳-12原子质量的 ,故选C。答案:C1.小美从某粒子结构示意图(如图)中,获取了下列信息,其中错误的是( )A.它有两个电子层 B.它的核电荷数为12C.它表示阴离子 D.它表示相对稳定结构 答案解析2.核电荷数大于核外电子数的粒子一定是( )A.分子 B.原子C.阴离子 D.阳离子 答案解析3.根据原子结构示意图,不能确定的是( )A.最外层电子数 B.中子数C.质子数 D.电子层数 答案4.已知某氧原子的相对原子质量为16,某硫原子的相对原子质量为32。如果该氧原子的质量为m,则该硫原子的质量为( )A.32m B.2mC.m D.不能确定 答案解析5.分析各组粒子结构示意图,与表示的意义一致的是( ) 答案解析6.已知一个碳-12原子的质量为1.993×10-26 kg,一个钬原子的质量是2.740×10-25kg,则钬的相对原子质量为 ;相同质量的钠、镁、铝含原子数目最多的是 (钠、镁、铝的相对原子质量分别是23、24、27)。 答案7.钠原子和氯原子的结构示意图如下:(1)氯原子的核电荷数是 。 (2)钠原子在化学反应中容易 (填“得到”或“失去”)一个电子。 (3)钠原子和氯原子相同的是 (填序号)。 ①质子数 ②电子数 ③电子层数 ④最外层电子数 答案
相关资料
更多









