所属成套资源:2025版高考化学一轮总复习教案(63份)
- 2025版高考化学一轮总复习教案第二章物质的量第六讲物质的量阿伏加德罗常数考点一物质的量气体摩尔体积 教案 0 次下载
- 2025版高考化学一轮总复习教案第二章物质的量第六讲物质的量阿伏加德罗常数考点二阿伏加德罗常数及计算 教案 0 次下载
- 2025版高考化学一轮总复习教案第二章物质的量第七讲一定物质的量浓度溶液的配制考点二一定物质的量浓度溶液的配制 教案 0 次下载
- 2025版高考化学一轮总复习教案第三章金属及其化合物第八讲钠及其重要化合物碱金属考点一钠及其氧化物 教案 0 次下载
- 2025版高考化学一轮总复习教案第三章金属及其化合物第八讲钠及其重要化合物碱金属考点二碳酸钠和碳酸氢钠碱金属 教案 0 次下载
2025版高考化学一轮总复习教案第二章物质的量第七讲一定物质的量浓度溶液的配制考点一物质的量浓度
展开
这是一份2025版高考化学一轮总复习教案第二章物质的量第七讲一定物质的量浓度溶液的配制考点一物质的量浓度,共2页。
知识梳理
1.物质的量浓度(cB)(从微观角度认识溶液的组成)
2.溶质的质量分数(w)(从宏观角度认识溶液的组成)
[微点归纳] 有关物质的量浓度计算的三个易错点
(1)溶液中溶质的判断
①与水发生反应的物质,溶质发生变化,水量减少,如:
②结晶水合物,溶质物质的量不变但水量增多,如CuSO4·5H2Oeq \(――→,\s\up7(水))CuSO4,FeSO4·7H2Oeq \(――→,\s\up7(水))FeSO4。
(2)混淆溶液的体积和溶剂的体积
①不能用溶剂的体积代替溶液的体积,尤其是固体、气体溶于水时,一般根据溶液的密度计算溶液的体积:V=eq \f(m气体或固体+m溶剂,ρ)。
②两溶液混合时,混合后溶液的体积并不是两液体体积的加和,应依据混合溶液的密度计算溶液的体积。
(3)部分与整体的关系
溶质的浓度和离子的浓度不一定相同,要注意根据化学式具体分析。如1 ml·L-1 Al2(SO4)3溶液中c(SOeq \\al(2-,4))=3 ml·L-1,c(Al3+)等于2 ml·L-1(考虑Al3+水解时,则其浓度小于2 ml·L-1)。Na、Na2O、Na2O2eq \(――→,\s\up7(水))NaOH
CO2、SO2、SO3eq \(――→,\s\up7(水),\s\d5(对应))H2CO3、H2SO3、H2SO4
NH3eq \(――→,\s\up7(水))NH3·H2O(溶质按NH3进行计算)
相关教案
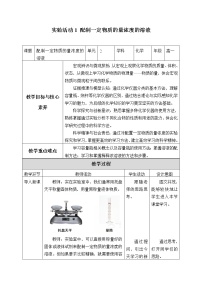
这是一份高中化学人教版 (2019)必修 第一册实验活动1 配制一定物质的量浓度的溶液教学设计,共8页。
这是一份高中实验活动1 配制一定物质的量浓度的溶液教学设计,共8页。
这是一份高中化学第三节 物质的量教学设计及反思,共11页。