





还剩22页未读,
继续阅读
所属成套资源:鲁教版化学九年级下册 课件
成套系列资料,整套一键下载
鲁教版化学九年级下册 第七单元 第四节 中和反应 课件
展开
这是一份鲁教版化学九年级下册 第七单元 第四节 中和反应 课件,共30页。
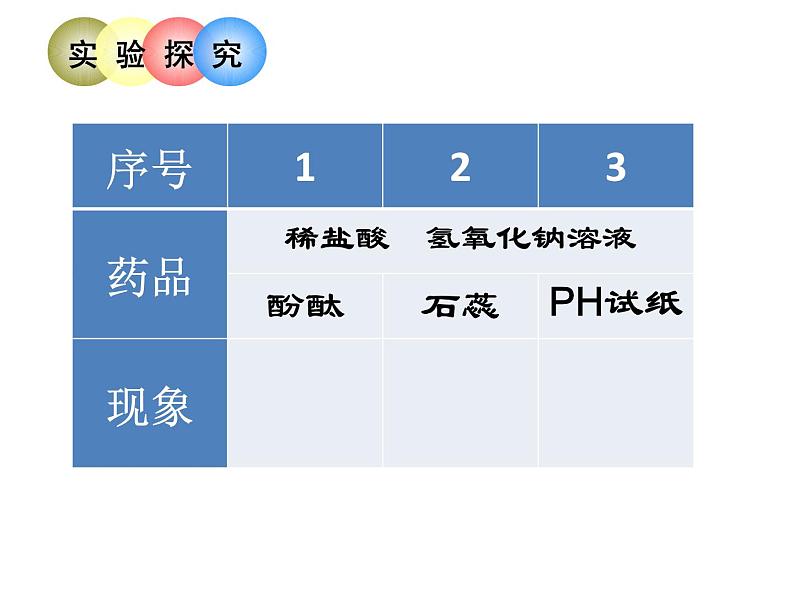
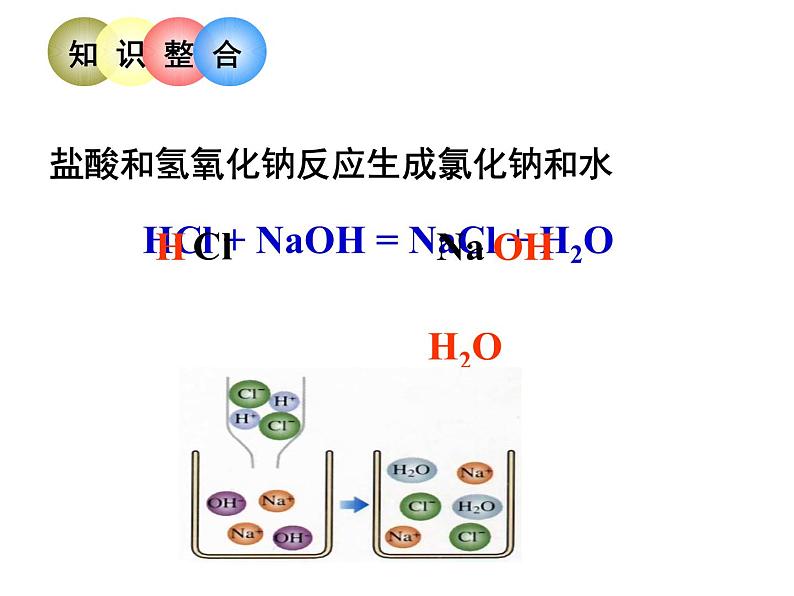
第七单元中和反应 一、酸和碱能发生化学反应吗?【实验探究1】 向盛有氢氧化钠的试管中滴加稀盐酸溶液 现象: 结论:无明显现象不能确定是否发生反应【实验探究2】 提出问题:盐酸和氢氧化钠能否发生反应 建立假设:盐酸和氢氧化钠 (能/不能) 发生反应 设计实验:?【实验探究2】 获得结论:盐酸和氢氧化钠能发生反应HCl + NaOH = NaCl + H2OHOH ClNa盐酸和氢氧化钠反应生成氯化钠和水 H2O盐:金属离子(铵根离子)和酸根离子构成的化合物 Na2CO3 CaCl2 NaCl Fe(NO3)3 酸根离子:Cl- NO3- SO42- CO32-盐中一定有金属离子吗?将下列物质分类H2CO3 CaCO3 CaO AgCl KOH H2SO4 Ca(OH)2 CuCl2 活动天地:寻找酸和碱反应的规律 ----请试着写一下盐酸和氢氧化钾:盐酸和氢氧化钡:硫酸和氢氧化钠:硫酸和氢氧化钡:酸+碱=盐+水中和反应:2HCl + Ba(OH)2 = BaCl2 + 2H2OHCl + KOH = KCl + H2O + ----- + 盐酸碱水3.所属反应类型复分解中和2.中和反应的实质: 1.中和反应的定义 酸 + 碱 盐 + 水H+ + OH- H2O复分解反应 两种化合物互相交换成分生成另外两种化合物的反应叫做复分解反应。NaOH+HCl==NaCl+H2O条件:产物沉淀、气体、水,必须有一种 否则反应不能发生 下列各组物质放入水中,必须借助酸碱指示剂才能判断反应发生的是( ) HCl + CaCO3 B. HCl + Fe2O3 C. H2SO4 + NaOH D. HCl + Fe 思考1:盐酸和氢氧化钠反应后的溶液一定是 中性的吗?ABC你能确定A、B、C三点的PH值和溶质组成吗?溶液的pH加入氢氧化钠溶液的体积/ml思考2:酸碱中和反应都一定没有现象吗?二、中和反应的应用1.应用于医药卫生胃酸的主要成分是盐酸3HCl + Al(OH)3 = AlCl3 + 3H2O农业上常用熟石灰来改良酸性土壤(硝酸)2HNO3+Ca(OH)2==Ca(NO3)2+2H2O2.改变土壤的酸碱性当污水中的含酸(硫酸)量超标时,可以利用熟石灰进行中和处理H2SO4 + Ca(OH)2 = CaSO4 + 2H2O3.处理工业废水2.关于中和反应的说法中错误的是( )A.中和反应一定要有酸和碱参加 B.中和反应属于复分解反应C.中和反应一定有盐和水生成 D.生成盐和水的反应一定是中和反应1.下列物质中属于盐的是( )A. NaOH B. H2SO4 C. Na2SO4 D. Ca(OH)2DC3.下列反应属于中和反应的是( )A.CO2 + 2NaOH == Na2CO3 + H2O B.CuO + H2SO4 == CuSO4 + H2OC.KOH + HNO3 == KNO3 + H2O D.Fe + 2HCl == FeCl2 + H2↑C4.中和反应在生产、生活、实验室中有广泛的用途,下列应用一定与中和反应原理无关的是( )A.施用熟石灰改良酸性土壤 B.服用含氢氧化铝的药物治疗胃酸过多C.用石灰石和稀盐酸制取二氧化碳 D.用氢氧化钠溶液洗涤石油产品中的残余硫酸C5.向某盐酸中逐滴加入NaOH溶液,所得溶液的与加入的NaOH溶液的质量关系曲线图合理的是6.要洗去烧水用的铝壶内壁上的水垢[主要含CaCO3和Mg(OH)2]可以用 除去,但加入该物质不能过量,原因用方程式表示 ,写出有关除水垢的化学方程式:(1) , (2) 。 稀盐酸2Al+6HCl=2AlCl3+3H2↑7.下图是盐酸滴入氢氧化钠溶液中,下列说法错误的是( )A.盐酸溶液中含有氢离子和氯离子B.氢氧化钠溶液中含有钠离子和氢氧根离子C.两种溶液混合时,氢离子与氢氧根离子结合生成 了水分子D.两种溶液混合时,钠离子与氯离子结合生成了氯 化钠分子8.从H、C、O、Na四种元素中选择适当的元素,组成符合下列要求的物质各一种,将化学式填在空格中。(1)氧化物: (2)酸: (3)碱: (4)盐: CO2 、H2O、Na2O、CO、H2O2H2CO3NaOHNa2CO3、NaHCO3
第七单元中和反应 一、酸和碱能发生化学反应吗?【实验探究1】 向盛有氢氧化钠的试管中滴加稀盐酸溶液 现象: 结论:无明显现象不能确定是否发生反应【实验探究2】 提出问题:盐酸和氢氧化钠能否发生反应 建立假设:盐酸和氢氧化钠 (能/不能) 发生反应 设计实验:?【实验探究2】 获得结论:盐酸和氢氧化钠能发生反应HCl + NaOH = NaCl + H2OHOH ClNa盐酸和氢氧化钠反应生成氯化钠和水 H2O盐:金属离子(铵根离子)和酸根离子构成的化合物 Na2CO3 CaCl2 NaCl Fe(NO3)3 酸根离子:Cl- NO3- SO42- CO32-盐中一定有金属离子吗?将下列物质分类H2CO3 CaCO3 CaO AgCl KOH H2SO4 Ca(OH)2 CuCl2 活动天地:寻找酸和碱反应的规律 ----请试着写一下盐酸和氢氧化钾:盐酸和氢氧化钡:硫酸和氢氧化钠:硫酸和氢氧化钡:酸+碱=盐+水中和反应:2HCl + Ba(OH)2 = BaCl2 + 2H2OHCl + KOH = KCl + H2O + ----- + 盐酸碱水3.所属反应类型复分解中和2.中和反应的实质: 1.中和反应的定义 酸 + 碱 盐 + 水H+ + OH- H2O复分解反应 两种化合物互相交换成分生成另外两种化合物的反应叫做复分解反应。NaOH+HCl==NaCl+H2O条件:产物沉淀、气体、水,必须有一种 否则反应不能发生 下列各组物质放入水中,必须借助酸碱指示剂才能判断反应发生的是( ) HCl + CaCO3 B. HCl + Fe2O3 C. H2SO4 + NaOH D. HCl + Fe 思考1:盐酸和氢氧化钠反应后的溶液一定是 中性的吗?ABC你能确定A、B、C三点的PH值和溶质组成吗?溶液的pH加入氢氧化钠溶液的体积/ml思考2:酸碱中和反应都一定没有现象吗?二、中和反应的应用1.应用于医药卫生胃酸的主要成分是盐酸3HCl + Al(OH)3 = AlCl3 + 3H2O农业上常用熟石灰来改良酸性土壤(硝酸)2HNO3+Ca(OH)2==Ca(NO3)2+2H2O2.改变土壤的酸碱性当污水中的含酸(硫酸)量超标时,可以利用熟石灰进行中和处理H2SO4 + Ca(OH)2 = CaSO4 + 2H2O3.处理工业废水2.关于中和反应的说法中错误的是( )A.中和反应一定要有酸和碱参加 B.中和反应属于复分解反应C.中和反应一定有盐和水生成 D.生成盐和水的反应一定是中和反应1.下列物质中属于盐的是( )A. NaOH B. H2SO4 C. Na2SO4 D. Ca(OH)2DC3.下列反应属于中和反应的是( )A.CO2 + 2NaOH == Na2CO3 + H2O B.CuO + H2SO4 == CuSO4 + H2OC.KOH + HNO3 == KNO3 + H2O D.Fe + 2HCl == FeCl2 + H2↑C4.中和反应在生产、生活、实验室中有广泛的用途,下列应用一定与中和反应原理无关的是( )A.施用熟石灰改良酸性土壤 B.服用含氢氧化铝的药物治疗胃酸过多C.用石灰石和稀盐酸制取二氧化碳 D.用氢氧化钠溶液洗涤石油产品中的残余硫酸C5.向某盐酸中逐滴加入NaOH溶液,所得溶液的与加入的NaOH溶液的质量关系曲线图合理的是6.要洗去烧水用的铝壶内壁上的水垢[主要含CaCO3和Mg(OH)2]可以用 除去,但加入该物质不能过量,原因用方程式表示 ,写出有关除水垢的化学方程式:(1) , (2) 。 稀盐酸2Al+6HCl=2AlCl3+3H2↑7.下图是盐酸滴入氢氧化钠溶液中,下列说法错误的是( )A.盐酸溶液中含有氢离子和氯离子B.氢氧化钠溶液中含有钠离子和氢氧根离子C.两种溶液混合时,氢离子与氢氧根离子结合生成 了水分子D.两种溶液混合时,钠离子与氯离子结合生成了氯 化钠分子8.从H、C、O、Na四种元素中选择适当的元素,组成符合下列要求的物质各一种,将化学式填在空格中。(1)氧化物: (2)酸: (3)碱: (4)盐: CO2 、H2O、Na2O、CO、H2O2H2CO3NaOHNa2CO3、NaHCO3
相关资料
更多









