



2024曲靖高三上学期第一次教学质量监测(一模)化学试题含解析
展开理科综合试题卷
可能用到的相对原子质量:H-1 O-16 S-32 Fe-56
第I卷(选择题,共126分)
一、选择题:(本题共13小题,每小题6分,共78分。在每小题给出的四个选项中,只有一项符合题目要求。)
1. 化学与生活、生产及科技密切相关。下列叙述错误的是
A. 利用聚合酶链反应使样本DNA在生物体外扩增,可以快速进行核酸检测
B. 低温石英(α-二氧化硅)具有手性结构,可用作压电材料制作石英手表
C. 我国科学家利用合成了脂肪酸,实现了无机小分子向有机高分子的转变
D. 储氢合金是一类能够大量吸收,并与结合成金属氢化物的材料,可用于以为燃料的汽车
2. 药物中间体Q的一种合成方法:
下列有关说法正确的是
A. Q的分子式为C16H17O3B. 两步反应类型均为加成反应
C. P分子存2个手性碳原子D. M可发生取代、加成和缩聚反应
3. 我国科学家在研究点击化学过程中,意外发现一种新化合物,其结构式如图所示,其中X、Y、Z和W是原子序数依次增大的短周期元素,Y与W是同一主族元素。下列说法正确的是
A. 第一电离能:
B. X的氢化物中只存在极性键
C. 电解Z的简单氢化物的水溶液可制得Z单质
D. W的最高价含氧酸根的空间构型为三角锥形
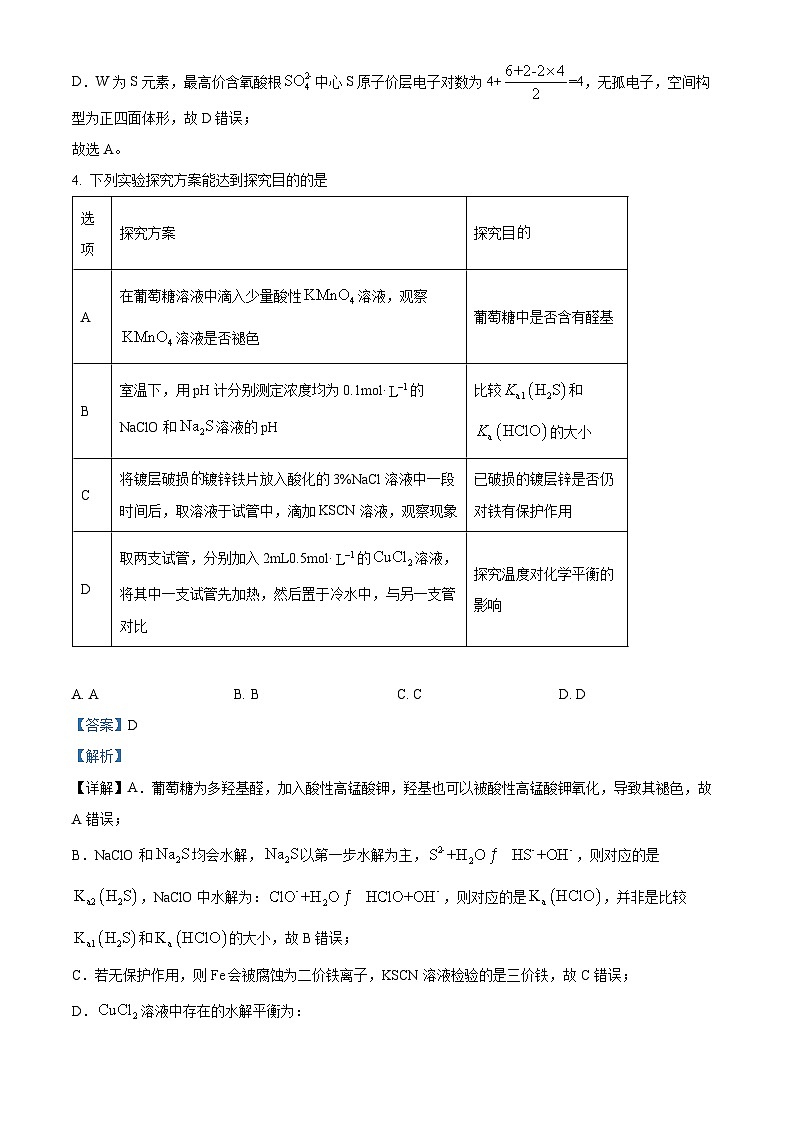
4. 下列实验探究方案能达到探究目的的是
A. AB. BC. CD. D
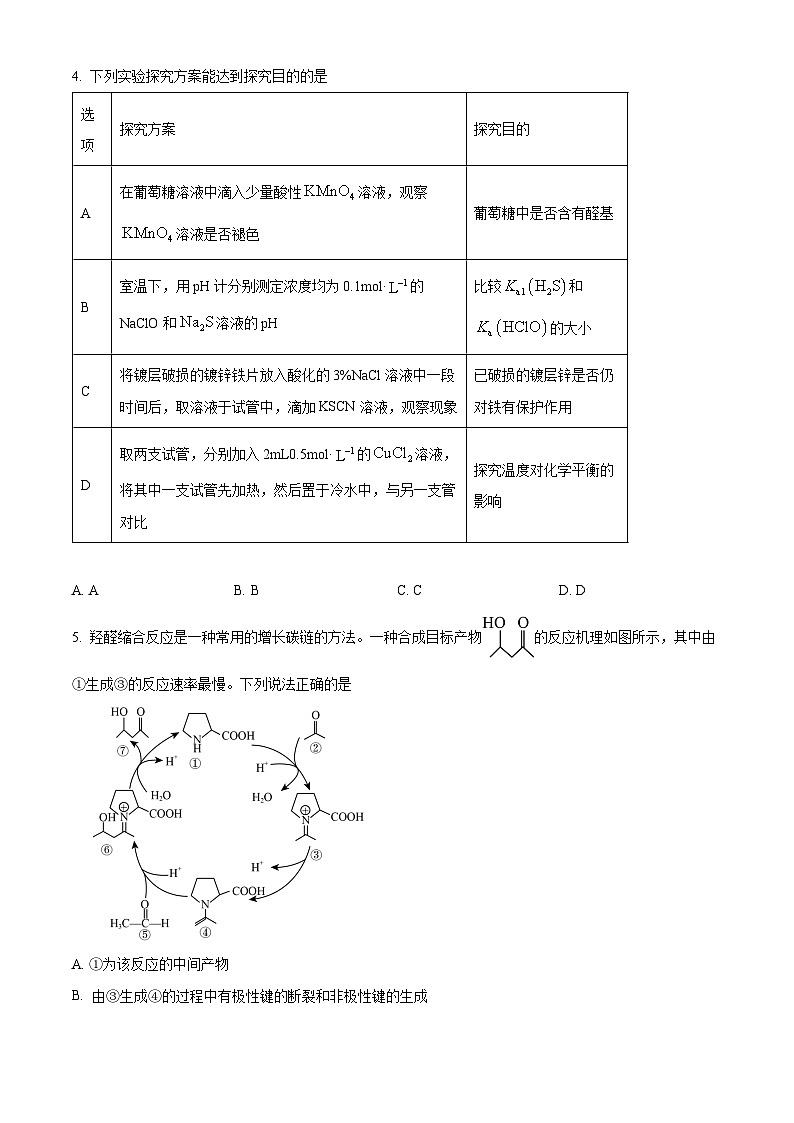
5. 羟醛缩合反应是一种常用的增长碳链的方法。一种合成目标产物的反应机理如图所示,其中由①生成③的反应速率最慢。下列说法正确的是
A. ①为该反应的中间产物
B. 由③生成④的过程中有极性键的断裂和非极性键的生成
C. 由①生成③的反应在各步骤中吸收的热量最多
D. 合成物质⑦的总反应为+2
6. 以光电极作辅助电极,溶液和NaI溶液为初始电解液组成二次电池装置如图所示,充电时光电极受光激发产生电子和空穴,在空穴作用下NaI转化为下列说法正确的是
A. 充电时,M极的电极反应式为
B. 放电时,流向M电极室
C. 空穴带正电荷,充电过程中能将还原为
D. 充电过程中能量转换形式为光能最终转化为电能
7. 向某、混合液中加入固体(忽略溶液体积、温度的变化),测得溶液中离子浓度变化如图所示。已知:为二元弱酸,,易溶于水且溶液呈碱性。下列说法正确的是
A. X点溶液可能呈酸性
B. X、Y、Z三点对应溶液pH大小顺序为:
C. Y点溶液中
D. 向溶液中加入等体积溶液有CaA沉淀生成
第II卷(非选择题,共14题,共174分。)
8. 过碳酸钠(2·,被称为固体双氧水,可在水中释放出活性氧而使其具有漂白和杀菌性能,是一种新型氧系漂白剂。过碳酸钠在异丙醇中的溶解度较低,实验室用和稳定剂的混合溶液与化合制备,反应原理为: ,装置如图所示。回答下列问题:
(1)盛装溶液的仪器名称为_______。
(2)下列可用作“稳定剂”的是_______(填字母)。
A. B. C. D.
(3)实验时,应打开磁力搅拌器并缓慢加入溶液的原因是____;反应结束后,停止搅拌,向反应液中加入异丙醇,静置、过滤、洗涤、干燥,获得过碳酸钠固体。加入异丙醇的目的是______。
(4)过碳酸钠是由和通过_______(填“化学键”、“氢键”或“分子间作用力”)形成的。过碳酸钠不稳定,在高温条件下,易发生分解,其反应方程式为_______。
(5)过碳酸钠活性氧含量的测定:准确称取试样2.0g于250mL锥形瓶中,加入40mL浓度为6%的硫酸溶液,水浴加热至,然后迅速用0.2000ml·的溶液滴定,至_______即为终点,消耗溶液30.00mL,该样品中的活性氧含量为_______(活性氧含量。
9. 硒化锌(ZnSe)常用作荧光粉、电子工业掺杂材料和高纯试剂,也是一种重要的半导体材料。其中以锌矿(主要成分是ZnS,含少量、CuS、NiS、等)为原料制备ZnSe的工艺流程如下图所示:
已知:pH较高时,FeOOH沉淀会转化成胶体。
(1)Se元素在周期表中的位置是_______,基态Zn原子的价层电子排布式为_______。
(2)写出气体X的一种用途_______。
(3)浸出液中含有,“除铁”步骤中通入氧气时发生反应的离子方程式为_______,同时需补充适量物质Y,Y是_______(写出一种即可)。“除铁”最佳pH为3.0,如果pH过高,会导致溶液中的含量降低,其主要原因是_______。
(4)“置换”时滤渣2的主要成分为_______。也可以在酸性含的溶液中加入锌粉和,生成,其离子方程式为_______。
(5)晶体与NaCl晶体的结构相似,晶胞为正方体,边长为apm。其结构如图所示:
晶胞密度ρ=_______g·列出计算式,阿伏加德罗常数的值为。
10. 氮的氧化物是大气主要污染物,研究含氮物质间的转化是环境科学的重要课题。
(1)①在恒温恒容的密闭容器中充入1ml和3ml发生反应生成,下列能说明反应达到平衡状态的是_______(填标号)。
A. B.容器内压强不变
C.气体的密度不再改变 D.容器内气体的平均摩尔质量不变
②以为还原剂,在催化剂作用下选择性地与发生氧化还原反应生成和。已知:
则与NO反应的热化学方程式的=_______kJ/ml(用含a、b的代数式表示)。
(2)已知反应历程分两步:
I.(快平衡)
Ⅱ.(慢反应)
决定NO氧化反应速率步骤是_______(填“I”或“Ⅱ”)。用表示的速率方程为;用表示的速率方程为,与分别表示速率常数(与温度有关),则与的关系为_______。
(3)将0.2mlNO(g)、0.1(g)和0.2mlHe(g)通入反应器,在温度T、压强条件下进行反应和(g)。tmin时达到化学平衡,NO的转化率为60%,且与的物质的量相等,则v=_______。该温度时,反应的平衡常数_______(分压=总压×物质的量分数)。
(4)利用与反应构成电池,能消除氮氧化物的排放,减轻环境污染,装置如图所示:
①电极B的电极反应式为_______。
②当有2.4ml通过阴离子交换膜时,理论上生成体积为_______(标准状况)。
11. 舒林酸K是一个活性极小的前体药,进入人体后代谢为有活性的硫化物,能够抑制环氧酶,具有镇痛、抗炎和解热作用。其合成路线如下:
回答下列问题:
(1)A的化学名称是_______。
(2)B生成C的反应类型为_______。
(3)D中官能团的名称为_______。
(4)E转化为F的化学方程式为_______。
(5)G中碳原子的轨道杂化类型有_______种。
(6)J的结构简式为_______。
(7)D的同分异构体中,同时满足下列条件的共有_______种。
①含有苯环;②取代基数目与D相同;③能与反应,且能在碱存在并加热的条件下水解生成NH3,其中在酸性条件下水解产物核磁共振氢谱显示为4组峰,且峰面积之比为的同分异构体的结构简式为_______(任写一种)。选项
探究方案
探究目的
A
在葡萄糖溶液中滴入少量酸性溶液,观察溶液是否褪色
葡萄糖中是否含有醛基
B
室温下,用pH计分别测定浓度均为0.1ml·的NaClO和溶液的pH
比较和的大小
C
将镀层破损的镀锌铁片放入酸化的3%NaCl溶液中一段时间后,取溶液于试管中,滴加KSCN溶液,观察现象
已破损的镀层锌是否仍对铁有保护作用
D
取两支试管,分别加入2mL0.5ml·的溶液,将其中一支试管先加热,然后置于冷水中,与另一支管对比
探究温度对化学平衡的影响
安徽省池州市2024届高三教学质量统一监测(二模)化学试题(含解析): 这是一份安徽省池州市2024届高三教学质量统一监测(二模)化学试题(含解析),共21页。试卷主要包含了单选题,解答题等内容,欢迎下载使用。
2024嘉兴高三上学期一模化学试题含解析: 这是一份2024嘉兴高三上学期一模化学试题含解析,文件包含浙江省嘉兴市2023-2024学年高三上学期12月月考化学试题卷含解析docx、浙江省嘉兴市2023-2024学年高三上学期12月月考化学试题卷无答案docx等2份试卷配套教学资源,其中试卷共37页, 欢迎下载使用。
2024绍兴高三上学期一模(期中)化学试题含解析: 这是一份2024绍兴高三上学期一模(期中)化学试题含解析,文件包含浙江省绍兴市2024届高三上学期一模期中化学试题原卷版docx、浙江省绍兴市2024届高三上学期一模期中化学试题含解析docx等2份试卷配套教学资源,其中试卷共39页, 欢迎下载使用。












