



还剩20页未读,
继续阅读
成套系列资料,整套一键下载
- 【分层练习】2.2 .4物质的量在化学方程式计算中的应用高一化学同步备课(人教版2019必修第一册)(原卷版+解析版) 试卷 4 次下载
- 【分层练习】2.3 .1 物质的量的单位——摩尔高一化学同步备课(人教版2019必修第一册)(原卷版+解析版) 试卷 6 次下载
- 【分层练习】2.3 .2 气体摩尔体积高一化学同步备课(人教版2019必修第一册)(原卷版+解析版) 试卷 4 次下载
- 【分层练习】2.3 .3 物质的量浓度高一化学同步备课(人教版2019必修第一册)(原卷版+解析版) 试卷 5 次下载
- 【同步课件】2.3 .4一定物质的量浓度溶液的配制高一化学同步备课(人教版2019必修第一册) 课件 6 次下载
【同步课件】2.3 .2 气体摩尔体积高一化学同步备课(人教版2019必修第一册)
展开
这是一份第二章第三节 第二课时 气体摩尔体积(同步课件)-2024-2025学年高一化学同步备课(人教版2019必修第一册),共28页。
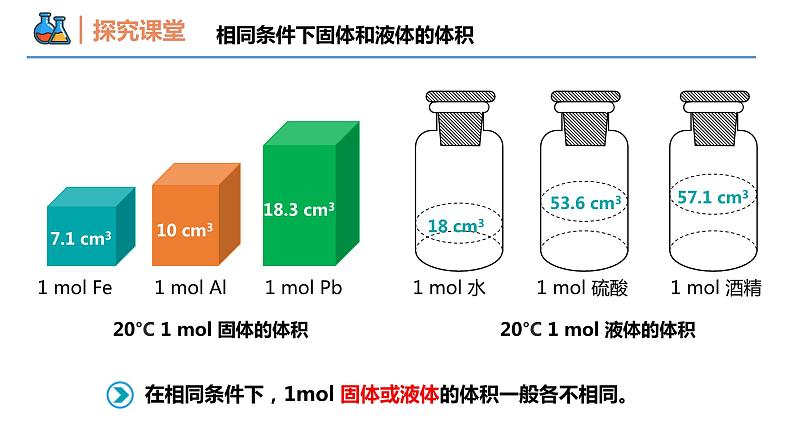
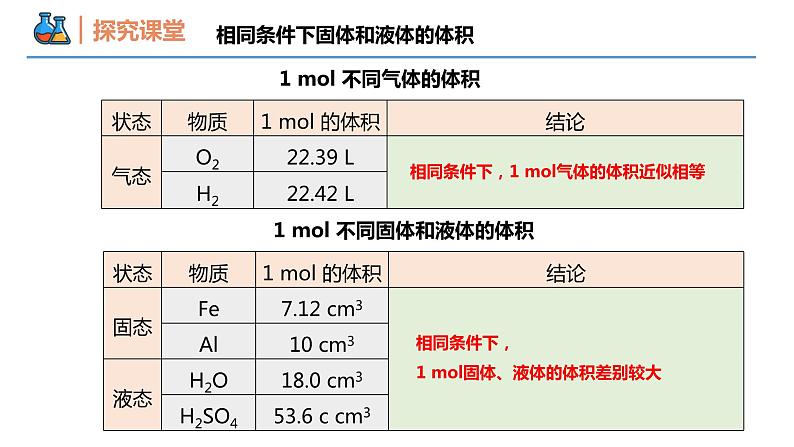
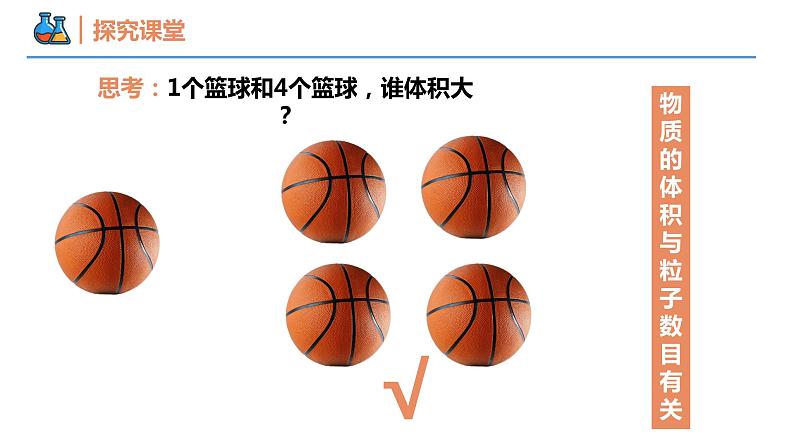
第二章 海水中的重要元素——钠和氯 第三节 物质的量 课时2 气体摩尔体积 壹贰叁影响物质体积的因素气体摩尔体积阿伏伽德罗定律本节重点本节难点气态物质,测量体积还是称量质量方便?实际生活中气体常见的计量方式Lm3相同条件下固体和液体的体积1 mol 不同气体的体积1 mol 不同固体和液体的体积相同条件下,1 mol气体的体积近似相等相同条件下,1 mol固体、液体的体积差别较大相同条件下固体和液体的体积 物质的体积与什么因素有关? 为什么相同条件下,1mol不同固体和液体的体积不同,而1mol不同气体的体积几乎相同?思考:1个篮球和1个乒乓球,谁体积大?物质的体积与粒子大小有关√思考:1个篮球和4个篮球,谁体积大?√物质的体积与粒子数目有关思考:4个乒乓球整齐排放与零乱分布,谁体积大?√物质的体积与粒子间距有关影响物质体积大小的因素气体物质粒子间距d气体粒子间的距离远大于粒子本身的直径固体液体粒子间的距离非常小影响物质体积大小的因素(微观分析) 同温同压下,任何气体粒子之间的距离几乎相等影响物质体积大小的因素(微观分析) 固体、液体物质粒子间间隔很小,在微粒数目相同的情况下,固体、液体的体积主要由粒子本身大小决定。气体物质分子间间隔远大于分子本身大小,在微粒数目相同的情况下,气体的体积主要由微粒间的距离大小决定,而分子间的平均距离受温度和压强的影响。影响物质体积大小的因素(微观分析) 气体摩尔体积1、概念与符号:单位物质的量的气体所占的体积。符号:Vm可理解成1mol气体的体积。单位:L/mol(L·mol-1)2、表达式与单位:3、数值:记住:标准状况(0℃即273K,101KPa) Vm≈22.4L/mol气体摩尔体积数的数值不是固定不变的,取决于气体所处的温度和压强。温度和压强一定时,气体摩尔体积为定值,但不一定相等。注意事项【例1】下列叙述正确的是( )A. 1mol任何气体的体积都为22.4LB. 1mol任何物质在标准状况下所占的体积都为22.4LC. 只有在标准状况下,气体摩尔体积才约为22.4L/molD. 标准状况下,22.4L任何气体的物质的量都是1mol D(0.8mol+0.4mol)×22.4L·mol-1=26.88L【例2】标准状况下,0.8molH2和0.4molO2的混合气的体积约为____________。26.88 L 1g氮气所占有的体积为VL,则该条件下氮气的摩尔体积为__________________。28V L·mol-1【变式2】标准状况下,由0.5 gH2、11g CO2和4 gO2组成的混合气体,其体积约为( )A.8.4 L B.11.2 L C.14.0 L D.16.8 L C【例3】在一定条件下,以过氧化氢为原料制取氧气(2H2O2 =2H2O+O2↑),当反应1 mol H2O2时,制得的氧气在标准状况下的体积为( )A.2.24L B.4.48L C.11.2L D.22.4L C阿伏加德罗定律1、概念:在相同的温度和压强下,相同体积的任何气体都含有相同数目的粒子。适用于气体,可以是单一气体,也可以是混合气体,对固体和液体不适用。2、适用范围:P为压强,V为体积,n为物质的量,T为温度,R为常数理想气体方程式:PV=nRT从PV=nRT可以得出:P、V、n、T四个变量中,如果固定其中三个变量的值,另一个变量会怎样?相等如果固定其中两个变量的值呢?其他两个一定成比例阿伏加德罗定律阿伏加德罗定律的推论及应用【例4】下列叙述正确的是( )A. 同温同压下,相同体积的物质,其物质的量一定相等B. 等物质的量的甲烷和一氧化碳所含的原子数相等C. 1L CO一定比1L O2的质量小D. 相同条件下的一氧化碳和氮气,若气体体积相等,则质量也相等 D【变式4】同温同压下,等质量的N2O4和NO2两种气体相比较,下列叙述正确的是( )A.体积比为2:1 B.分子个数之比为1:1C.原子个数之比为1:1 D.氮原子个数之比为2:1 C【例5】设NA表示阿伏加德罗常数,下列叙述中正确的是( )A. 常温常压下,11.2L CO2所含的原子数为1.5NAB. 常温常压下,48g O3含有的氧原子数为NAC. 标准状况下,22.4 L 水所含分子数为NAD. 常温常压下,32g O2与O3混合物含有的氧原子数为2NA D【变式5】下列说法正确的是( )A. 常温常压下,22.4LCO2中含有NA个CO2分子B. 标准状况下,22.4L空气含有NA个单质分子C. 22.4L Cl2中含有NA个Cl2分子D. 标准状况下,1.12 L O2和1.12 L CO2均含0.1NA个氧原子 D谢谢观看THANKS
第二章 海水中的重要元素——钠和氯 第三节 物质的量 课时2 气体摩尔体积 壹贰叁影响物质体积的因素气体摩尔体积阿伏伽德罗定律本节重点本节难点气态物质,测量体积还是称量质量方便?实际生活中气体常见的计量方式Lm3相同条件下固体和液体的体积1 mol 不同气体的体积1 mol 不同固体和液体的体积相同条件下,1 mol气体的体积近似相等相同条件下,1 mol固体、液体的体积差别较大相同条件下固体和液体的体积 物质的体积与什么因素有关? 为什么相同条件下,1mol不同固体和液体的体积不同,而1mol不同气体的体积几乎相同?思考:1个篮球和1个乒乓球,谁体积大?物质的体积与粒子大小有关√思考:1个篮球和4个篮球,谁体积大?√物质的体积与粒子数目有关思考:4个乒乓球整齐排放与零乱分布,谁体积大?√物质的体积与粒子间距有关影响物质体积大小的因素气体物质粒子间距d气体粒子间的距离远大于粒子本身的直径固体液体粒子间的距离非常小影响物质体积大小的因素(微观分析) 同温同压下,任何气体粒子之间的距离几乎相等影响物质体积大小的因素(微观分析) 固体、液体物质粒子间间隔很小,在微粒数目相同的情况下,固体、液体的体积主要由粒子本身大小决定。气体物质分子间间隔远大于分子本身大小,在微粒数目相同的情况下,气体的体积主要由微粒间的距离大小决定,而分子间的平均距离受温度和压强的影响。影响物质体积大小的因素(微观分析) 气体摩尔体积1、概念与符号:单位物质的量的气体所占的体积。符号:Vm可理解成1mol气体的体积。单位:L/mol(L·mol-1)2、表达式与单位:3、数值:记住:标准状况(0℃即273K,101KPa) Vm≈22.4L/mol气体摩尔体积数的数值不是固定不变的,取决于气体所处的温度和压强。温度和压强一定时,气体摩尔体积为定值,但不一定相等。注意事项【例1】下列叙述正确的是( )A. 1mol任何气体的体积都为22.4LB. 1mol任何物质在标准状况下所占的体积都为22.4LC. 只有在标准状况下,气体摩尔体积才约为22.4L/molD. 标准状况下,22.4L任何气体的物质的量都是1mol D(0.8mol+0.4mol)×22.4L·mol-1=26.88L【例2】标准状况下,0.8molH2和0.4molO2的混合气的体积约为____________。26.88 L 1g氮气所占有的体积为VL,则该条件下氮气的摩尔体积为__________________。28V L·mol-1【变式2】标准状况下,由0.5 gH2、11g CO2和4 gO2组成的混合气体,其体积约为( )A.8.4 L B.11.2 L C.14.0 L D.16.8 L C【例3】在一定条件下,以过氧化氢为原料制取氧气(2H2O2 =2H2O+O2↑),当反应1 mol H2O2时,制得的氧气在标准状况下的体积为( )A.2.24L B.4.48L C.11.2L D.22.4L C阿伏加德罗定律1、概念:在相同的温度和压强下,相同体积的任何气体都含有相同数目的粒子。适用于气体,可以是单一气体,也可以是混合气体,对固体和液体不适用。2、适用范围:P为压强,V为体积,n为物质的量,T为温度,R为常数理想气体方程式:PV=nRT从PV=nRT可以得出:P、V、n、T四个变量中,如果固定其中三个变量的值,另一个变量会怎样?相等如果固定其中两个变量的值呢?其他两个一定成比例阿伏加德罗定律阿伏加德罗定律的推论及应用【例4】下列叙述正确的是( )A. 同温同压下,相同体积的物质,其物质的量一定相等B. 等物质的量的甲烷和一氧化碳所含的原子数相等C. 1L CO一定比1L O2的质量小D. 相同条件下的一氧化碳和氮气,若气体体积相等,则质量也相等 D【变式4】同温同压下,等质量的N2O4和NO2两种气体相比较,下列叙述正确的是( )A.体积比为2:1 B.分子个数之比为1:1C.原子个数之比为1:1 D.氮原子个数之比为2:1 C【例5】设NA表示阿伏加德罗常数,下列叙述中正确的是( )A. 常温常压下,11.2L CO2所含的原子数为1.5NAB. 常温常压下,48g O3含有的氧原子数为NAC. 标准状况下,22.4 L 水所含分子数为NAD. 常温常压下,32g O2与O3混合物含有的氧原子数为2NA D【变式5】下列说法正确的是( )A. 常温常压下,22.4LCO2中含有NA个CO2分子B. 标准状况下,22.4L空气含有NA个单质分子C. 22.4L Cl2中含有NA个Cl2分子D. 标准状况下,1.12 L O2和1.12 L CO2均含0.1NA个氧原子 D谢谢观看THANKS
相关资料
更多










