






还剩16页未读,
继续阅读
成套系列资料,整套一键下载
【同步课件】3.1 .2 铁的重要化合物高一化学同步备课(人教版2019必修第一册)
展开
这是一份第三章第一节 第二课时 铁的重要化合物(同步课件)-2024-2025学年高一化学同步备课(人教版2019必修第一册),共24页。
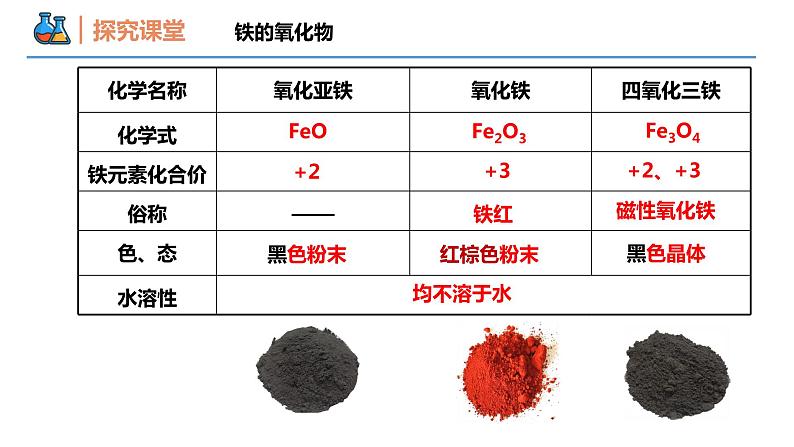
第三章 铁 金属材料 第一节 铁及其化合物 课时2 铁的重要化合物 壹贰铁的氧化物铁的氢氧化物本节重难点红砖的成分是粘土(主要是硅酸盐),红色来自于三氧化二铁。其中的主要反应是焦炭和水在高温下反应生成一氧化碳和氢气(又叫水煤气),两种气体都有还原性,在高温下降三价铁还原成二价得到氧化亚铁是黑色的——是青砖。出窑前不加水则得到三价铁的氧化物是红棕色的——是红砖。红砖青砖知多少丹霞地貌的岩层因含(Fe2O3)而呈红色丹霞地貌在我国广泛分布,如:四川的蜀南竹海、七洞沟;贵州赤水;广东丹霞山;江西龙虎山等。FeO Fe2O3Fe3O4+2 +3 铁红黑色粉末 红棕色粉末均不溶于水+2、+3磁性氧化铁黑色晶体铁的氧化物氧化亚铁(FeO)黑色粉末颜色、状态:溶解性:铁的价态:与H+反应的离子方程式:不溶于水+2FeO+2H+=Fe2++H2O稳定性:不稳定与CO、C、H2反应:生成单质铁及CO2或H2O——氧化性和还原性碱性氧化物铁的氧化物铁的氧化物氧化铁(Fe2O3)红棕色粉末颜色、状态:溶解性:铁的价态:与H+反应的离子方程式:不溶于水+3稳定性:稳定与CO、C、H2反应:生成单质铁及CO2或H2O——氧化性碱性氧化物铁红俗称:6H++Fe2O3=2Fe3++3H2O用途:Fe2O3常用作红色油漆与涂料,赤铁矿(主要成分是Fe2O3)是炼铁的原料。铁的氧化物四氧化三铁(Fe3O4)黑色晶体(有磁性)颜色、状态:溶解性:铁的价态:与H+反应的离子方程式:不溶于水+2、+3稳定性:稳定与CO、C、H2反应:生成单质铁及CO2或H2O特殊氧化物俗称:磁性氧化铁Fe3O4+8H+=2Fe3++Fe2++4H2O【例1】下列关于铁的氧化物说法正确的是( )A.“雨过天晴云破处”所描述的瓷器青色来自氧化铁B. Fe2O3是红棕色粉末,俗称磁性氧化铁,常用作红色油漆和涂料C. Fe3O4中Fe元素的化合价有+2价和+3价,因而Fe3O4是FeO与 Fe2O3的混合物D. FeO在空气中受热,能迅速被氧化成Fe3O4D 铁的氧化物【例2】准确称取某种铁的氧化物2.88 g,用足量的CO进行还原,将生成的CO2全部用足量的澄清石灰水吸收,得到沉淀4 g,则这种铁的氧化物为 ( )A.Fe3O4 B.Fe2O3C.FeO D.以上都不是C铁的氧化物铁的氢氧化物实验探究在两支试管中分别加入少量的FeCl3溶液和FeSO4溶液,然后各滴入NaOH溶液。观察并描述发生的现象。Fe(OH)3Fe(OH)2铁的氢氧化物铁的氢氧化物Fe3++3OH-=Fe(OH)3↓有红褐色沉淀铁的氢氧化物Fe2++2OH-=Fe(OH)2↓白色沉淀灰绿色红褐色 4Fe(OH)2+O2+2H2O=4Fe(OH)3铁的氢氧化物Fe(OH)3+3H+=Fe3++3H2O红褐色沉淀——铁的氢氧化物Fe(OH)2+2H+=Fe2++2H2O白色沉淀4Fe(OH)2+O2+2H2O=4Fe(OH)3——由实验可知,白色的Fe(OH)2会被溶解在溶液中的氧气氧化。那么,在实验室里,如何得到较纯净的Fe(OH)2呢?4Fe(OH)2+O2+2H2O=4Fe(OH)3铁的氢氧化物油封(有机物:苯、植物油、煤油等)将胶头滴管伸入FeSO4溶液底部,再挤出NaOH溶液。加热煮沸NaOH溶液或用煮沸过的蒸馏水配置溶液方法一:方法二:方法三:铁的氢氧化物方法四:利用N2、H2、CO2等,驱赶装置中的空气方法五: FeSO4溶液中加入Fe粉。2Fe3+ +Fe=3Fe2+铁的氢氧化物 【例3】有关铁的化合物的说法中,错误的是 ( ) A. Fe(OH)2是一种灰绿色沉淀,不稳定,在空气中易被氧化变为红褐色 B. 由图示操作可制取Fe(OH)2 C. Fe3O4、Fe(OH)3都可以由化合反应制得 D. Fe(OH)3胶体呈红褐色、透明,能发生丁达尔效应 A铁的氢氧化物【例4】铁屑溶于过量稀硫酸,过滤后向滤液中加入过量氨水,有白色沉淀生成,过滤,在空气中加热沉淀至质量不再发生变化为止,得到红棕色残渣,上述白色沉淀和残渣分别是( )A.Fe(OH)3;Fe2O3 B.Fe(OH)2;Fe2O3C.Fe(OH)2;Fe(OH)3、Fe3O4 D.Fe2O3;Fe(OH)3B铁的氢氧化物谢谢观看THANKS
第三章 铁 金属材料 第一节 铁及其化合物 课时2 铁的重要化合物 壹贰铁的氧化物铁的氢氧化物本节重难点红砖的成分是粘土(主要是硅酸盐),红色来自于三氧化二铁。其中的主要反应是焦炭和水在高温下反应生成一氧化碳和氢气(又叫水煤气),两种气体都有还原性,在高温下降三价铁还原成二价得到氧化亚铁是黑色的——是青砖。出窑前不加水则得到三价铁的氧化物是红棕色的——是红砖。红砖青砖知多少丹霞地貌的岩层因含(Fe2O3)而呈红色丹霞地貌在我国广泛分布,如:四川的蜀南竹海、七洞沟;贵州赤水;广东丹霞山;江西龙虎山等。FeO Fe2O3Fe3O4+2 +3 铁红黑色粉末 红棕色粉末均不溶于水+2、+3磁性氧化铁黑色晶体铁的氧化物氧化亚铁(FeO)黑色粉末颜色、状态:溶解性:铁的价态:与H+反应的离子方程式:不溶于水+2FeO+2H+=Fe2++H2O稳定性:不稳定与CO、C、H2反应:生成单质铁及CO2或H2O——氧化性和还原性碱性氧化物铁的氧化物铁的氧化物氧化铁(Fe2O3)红棕色粉末颜色、状态:溶解性:铁的价态:与H+反应的离子方程式:不溶于水+3稳定性:稳定与CO、C、H2反应:生成单质铁及CO2或H2O——氧化性碱性氧化物铁红俗称:6H++Fe2O3=2Fe3++3H2O用途:Fe2O3常用作红色油漆与涂料,赤铁矿(主要成分是Fe2O3)是炼铁的原料。铁的氧化物四氧化三铁(Fe3O4)黑色晶体(有磁性)颜色、状态:溶解性:铁的价态:与H+反应的离子方程式:不溶于水+2、+3稳定性:稳定与CO、C、H2反应:生成单质铁及CO2或H2O特殊氧化物俗称:磁性氧化铁Fe3O4+8H+=2Fe3++Fe2++4H2O【例1】下列关于铁的氧化物说法正确的是( )A.“雨过天晴云破处”所描述的瓷器青色来自氧化铁B. Fe2O3是红棕色粉末,俗称磁性氧化铁,常用作红色油漆和涂料C. Fe3O4中Fe元素的化合价有+2价和+3价,因而Fe3O4是FeO与 Fe2O3的混合物D. FeO在空气中受热,能迅速被氧化成Fe3O4D 铁的氧化物【例2】准确称取某种铁的氧化物2.88 g,用足量的CO进行还原,将生成的CO2全部用足量的澄清石灰水吸收,得到沉淀4 g,则这种铁的氧化物为 ( )A.Fe3O4 B.Fe2O3C.FeO D.以上都不是C铁的氧化物铁的氢氧化物实验探究在两支试管中分别加入少量的FeCl3溶液和FeSO4溶液,然后各滴入NaOH溶液。观察并描述发生的现象。Fe(OH)3Fe(OH)2铁的氢氧化物铁的氢氧化物Fe3++3OH-=Fe(OH)3↓有红褐色沉淀铁的氢氧化物Fe2++2OH-=Fe(OH)2↓白色沉淀灰绿色红褐色 4Fe(OH)2+O2+2H2O=4Fe(OH)3铁的氢氧化物Fe(OH)3+3H+=Fe3++3H2O红褐色沉淀——铁的氢氧化物Fe(OH)2+2H+=Fe2++2H2O白色沉淀4Fe(OH)2+O2+2H2O=4Fe(OH)3——由实验可知,白色的Fe(OH)2会被溶解在溶液中的氧气氧化。那么,在实验室里,如何得到较纯净的Fe(OH)2呢?4Fe(OH)2+O2+2H2O=4Fe(OH)3铁的氢氧化物油封(有机物:苯、植物油、煤油等)将胶头滴管伸入FeSO4溶液底部,再挤出NaOH溶液。加热煮沸NaOH溶液或用煮沸过的蒸馏水配置溶液方法一:方法二:方法三:铁的氢氧化物方法四:利用N2、H2、CO2等,驱赶装置中的空气方法五: FeSO4溶液中加入Fe粉。2Fe3+ +Fe=3Fe2+铁的氢氧化物 【例3】有关铁的化合物的说法中,错误的是 ( ) A. Fe(OH)2是一种灰绿色沉淀,不稳定,在空气中易被氧化变为红褐色 B. 由图示操作可制取Fe(OH)2 C. Fe3O4、Fe(OH)3都可以由化合反应制得 D. Fe(OH)3胶体呈红褐色、透明,能发生丁达尔效应 A铁的氢氧化物【例4】铁屑溶于过量稀硫酸,过滤后向滤液中加入过量氨水,有白色沉淀生成,过滤,在空气中加热沉淀至质量不再发生变化为止,得到红棕色残渣,上述白色沉淀和残渣分别是( )A.Fe(OH)3;Fe2O3 B.Fe(OH)2;Fe2O3C.Fe(OH)2;Fe(OH)3、Fe3O4 D.Fe2O3;Fe(OH)3B铁的氢氧化物谢谢观看THANKS
相关资料
更多










