






还剩15页未读,
继续阅读
成套系列资料,整套一键下载
【同步课件】3.1 .3 铁盐和亚铁盐高一化学同步备课(人教版2019必修第一册)
展开
这是一份第三章第一节 第三课时 铁盐和亚铁盐(同步课件)-2024-2025学年高一化学同步备课(人教版2019必修第一册),共23页。
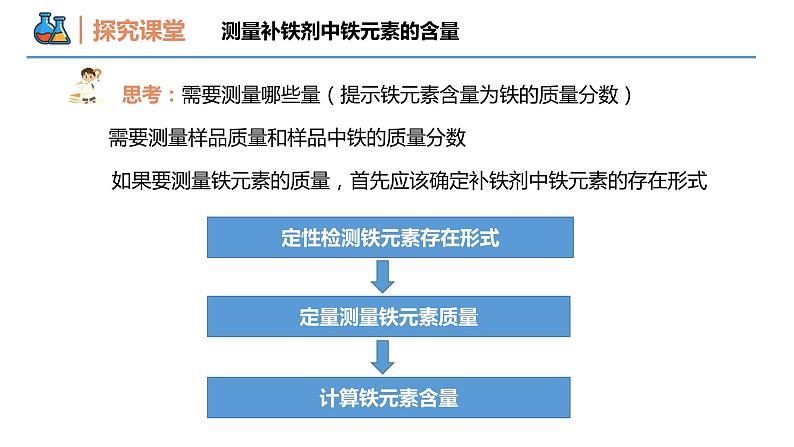
第三章 铁 金属材料 第一节 铁及其化合物 课时3 铁盐和亚铁盐 壹贰叁亚铁盐的性质铁盐的性质铁盐和亚铁盐的转化本节重难点铁是人体必需的微量元素中含量最多的一种(约4~5克)缺铁会导致人的记忆能力、免疫能力和对温度的适应能力等生理功能下降人体中的铁元素生活中的铁元素亚铁盐可以用来治疗缺铁性贫血。某补铁药物如图所示,其主要成分是硫酸亚铁。如果你是药品质检员,想要检测补铁剂中铁元素的含量,你会怎么做?测量补铁剂中铁元素的含量思考:需要测量哪些量(提示铁元素含量为铁的质量分数)需要测量样品质量和样品中铁的质量分数定性检测铁元素存在形式定量测量铁元素质量计算铁元素含量如果要测量铁元素的质量,首先应该确定补铁剂中铁元素的存在形式测量补铁剂中铁元素的含量将一片补铁剂用水溶解配成溶液,你认为样品中铁元素有哪些存在形式? Fe2+ Fe3+O2猜想1:样品中只含有Fe2+猜想2:样品中只含有Fe3+猜想3:样品中含有Fe2+和Fe3+针对猜想,请同学们设计实验加以验证定性检测铁元素存在形式方案评价:如果溶液中离子浓度很小,很难观察确认方案1:观察法,Fe2+溶液浅绿色,Fe3+ 溶液黄色定性检测铁元素存在形式方案2:首先确认Fe2+存在 ,利用Fe2+还原性取少量样品溶液于试管,滴加少量酸性高锰酸钾溶液,如果紫红色褪色,则溶液中含有Fe2+ ;如果无明显变化,则溶液中不含Fe2+5Fe2++MnO4-+8H+= 5Fe3+ +Mn2++4H2O定性检测铁元素存在形式方案2:其次确认Fe3+存在 铁盐和亚铁盐Fe2+Fe3+几滴KSCN溶液几滴KSCN溶液不变色变红色Fe3+ + 3SCN- = Fe(SCN)3 (红色液体) 检验Fe3+最灵敏的方法离子检验方法你还知道哪些试剂能将亚铁盐变成铁盐?写出反应的离子方程式2Fe2++Cl2= 2Fe3+ +2Cl- 氧化剂:Cl2、H2O2、HNO3、浓硫酸、KMnO4、O2等可将亚铁盐氧化为铁盐铁盐和亚铁盐铁盐和亚铁盐亚铁盐很容易被氧化为铁盐,如果重新将铁盐转变成亚铁盐,你会选择什么试剂?2Fe3++Cu= 2Fe2+ +Cu2+Fe3+Fe2+还原剂电子工业上常用覆铜板制作印刷电路板2Fe3++2I-= 2Fe2+ +I2引入新杂质碘水不易分离铁盐和亚铁盐铁盐和亚铁盐铁与过量稀硝酸反应方程式?Fe + 4HNO3 = Fe(NO3)3 + NO↑ + 2H2O过量铁与稀硝酸反应方程式?3Fe + 8HNO3 = 3Fe(NO3)2 + 2NO↑ + 4H2O铁盐和亚铁盐Fe3+Fe2+还原剂氧化剂元素价态是实现物质间转化的重要认知视角还原剂:金属单质如Fe和Zn等、 S2-、I-、SO32-等且还原性S2- >SO32- > I-氧化剂:Cl2、H2O2、HNO3、浓硫酸、KMnO4、O2等可将亚铁盐氧化为铁盐定量测量铁元素质量溶液中Fe2+、Fe3+的质量不易直接测量,可以将离子转化为沉淀,通过测量沉淀的质量来计算铁元素的质量。Fe3++3OH-=Fe(OH)3↓Fe2++2OH-=Fe(OH)2↓(3) 碱液法: 分别加入碱液(或氨水), 生成______色沉淀的溶液中含有Fe3+;先生成_____色沉淀, 又迅速转变为________色, 最后变为_______的溶液中含有Fe2+.(2) KSCN法: 滴入KSCN溶液, 呈 _____ 色的溶液中含有Fe3+。血红红褐白灰绿红褐(1) 颜色: Fe2+_________Fe3+_______.Fe 2+、Fe 3+的鉴别方法黄色浅绿色能否用KSCN法检验Fe2+?先滴入KSCN溶液, 无颜色变化,再加入氯水,溶液变红色。 【例1】下列离子的检验方法合理的是( ) A.向某溶液中滴入KSCN溶液呈红色,说明原溶液中不含Fe2+ B.向某溶液中通入Cl2,然后再加入KSCN溶液变红色,说明原溶液中 含有Fe2+ C.向某溶液中加入KSCN溶液呈红色,说明原溶液中含有Fe3+ D.向某溶液中加入NaOH溶液得白色沉淀,又观察到沉淀颜色逐渐变 为红褐色,说明原溶液中含有Fe2+, 不含有Mg2+C【例2】只用一种试剂或操作除去下列物质中的杂质(括号内为杂质),写出试剂或操作的名称、方法及有关反应的化学方程式或离子方程式。(1) FeCl2溶液(FeCl3)______________________; 化学方程式:__________________________。(2) Fe2O3[Fe(OH)3]__________; 化学方程式:_______________________________________。(3) FeSO4溶液(CuSO4)_________________________________; 化学方程式:_______________________________________。(4) FeCl3溶(FeCl2)________________________; 化学方程式:______________________________________。加足量铁粉,然后过滤2Fe3++Fe=3Fe2+ 加热加足量铁粉,充分反应后过滤Cu2++Fe=Fe2++Cu氯水或氯气2Fe2++Cl2=2Fe3++2Cl-”铁三角“的转化① 2Fe3++H2S = ② 2Fe3++SO2+2H2O = ③ 3Fe2++4H++NO3-= ④ 5Fe2++MnO4-+8H+= ⑤ 2Fe2++H2O2+2H+ = 用离子方程式表现转化2Fe2++S↓+2H+2Fe2++4H++SO42-3Fe3++2H2O+NO↑5Fe3++Mn2++4H2O2Fe3++2H2O谢谢观看THANKS
第三章 铁 金属材料 第一节 铁及其化合物 课时3 铁盐和亚铁盐 壹贰叁亚铁盐的性质铁盐的性质铁盐和亚铁盐的转化本节重难点铁是人体必需的微量元素中含量最多的一种(约4~5克)缺铁会导致人的记忆能力、免疫能力和对温度的适应能力等生理功能下降人体中的铁元素生活中的铁元素亚铁盐可以用来治疗缺铁性贫血。某补铁药物如图所示,其主要成分是硫酸亚铁。如果你是药品质检员,想要检测补铁剂中铁元素的含量,你会怎么做?测量补铁剂中铁元素的含量思考:需要测量哪些量(提示铁元素含量为铁的质量分数)需要测量样品质量和样品中铁的质量分数定性检测铁元素存在形式定量测量铁元素质量计算铁元素含量如果要测量铁元素的质量,首先应该确定补铁剂中铁元素的存在形式测量补铁剂中铁元素的含量将一片补铁剂用水溶解配成溶液,你认为样品中铁元素有哪些存在形式? Fe2+ Fe3+O2猜想1:样品中只含有Fe2+猜想2:样品中只含有Fe3+猜想3:样品中含有Fe2+和Fe3+针对猜想,请同学们设计实验加以验证定性检测铁元素存在形式方案评价:如果溶液中离子浓度很小,很难观察确认方案1:观察法,Fe2+溶液浅绿色,Fe3+ 溶液黄色定性检测铁元素存在形式方案2:首先确认Fe2+存在 ,利用Fe2+还原性取少量样品溶液于试管,滴加少量酸性高锰酸钾溶液,如果紫红色褪色,则溶液中含有Fe2+ ;如果无明显变化,则溶液中不含Fe2+5Fe2++MnO4-+8H+= 5Fe3+ +Mn2++4H2O定性检测铁元素存在形式方案2:其次确认Fe3+存在 铁盐和亚铁盐Fe2+Fe3+几滴KSCN溶液几滴KSCN溶液不变色变红色Fe3+ + 3SCN- = Fe(SCN)3 (红色液体) 检验Fe3+最灵敏的方法离子检验方法你还知道哪些试剂能将亚铁盐变成铁盐?写出反应的离子方程式2Fe2++Cl2= 2Fe3+ +2Cl- 氧化剂:Cl2、H2O2、HNO3、浓硫酸、KMnO4、O2等可将亚铁盐氧化为铁盐铁盐和亚铁盐铁盐和亚铁盐亚铁盐很容易被氧化为铁盐,如果重新将铁盐转变成亚铁盐,你会选择什么试剂?2Fe3++Cu= 2Fe2+ +Cu2+Fe3+Fe2+还原剂电子工业上常用覆铜板制作印刷电路板2Fe3++2I-= 2Fe2+ +I2引入新杂质碘水不易分离铁盐和亚铁盐铁盐和亚铁盐铁与过量稀硝酸反应方程式?Fe + 4HNO3 = Fe(NO3)3 + NO↑ + 2H2O过量铁与稀硝酸反应方程式?3Fe + 8HNO3 = 3Fe(NO3)2 + 2NO↑ + 4H2O铁盐和亚铁盐Fe3+Fe2+还原剂氧化剂元素价态是实现物质间转化的重要认知视角还原剂:金属单质如Fe和Zn等、 S2-、I-、SO32-等且还原性S2- >SO32- > I-氧化剂:Cl2、H2O2、HNO3、浓硫酸、KMnO4、O2等可将亚铁盐氧化为铁盐定量测量铁元素质量溶液中Fe2+、Fe3+的质量不易直接测量,可以将离子转化为沉淀,通过测量沉淀的质量来计算铁元素的质量。Fe3++3OH-=Fe(OH)3↓Fe2++2OH-=Fe(OH)2↓(3) 碱液法: 分别加入碱液(或氨水), 生成______色沉淀的溶液中含有Fe3+;先生成_____色沉淀, 又迅速转变为________色, 最后变为_______的溶液中含有Fe2+.(2) KSCN法: 滴入KSCN溶液, 呈 _____ 色的溶液中含有Fe3+。血红红褐白灰绿红褐(1) 颜色: Fe2+_________Fe3+_______.Fe 2+、Fe 3+的鉴别方法黄色浅绿色能否用KSCN法检验Fe2+?先滴入KSCN溶液, 无颜色变化,再加入氯水,溶液变红色。 【例1】下列离子的检验方法合理的是( ) A.向某溶液中滴入KSCN溶液呈红色,说明原溶液中不含Fe2+ B.向某溶液中通入Cl2,然后再加入KSCN溶液变红色,说明原溶液中 含有Fe2+ C.向某溶液中加入KSCN溶液呈红色,说明原溶液中含有Fe3+ D.向某溶液中加入NaOH溶液得白色沉淀,又观察到沉淀颜色逐渐变 为红褐色,说明原溶液中含有Fe2+, 不含有Mg2+C【例2】只用一种试剂或操作除去下列物质中的杂质(括号内为杂质),写出试剂或操作的名称、方法及有关反应的化学方程式或离子方程式。(1) FeCl2溶液(FeCl3)______________________; 化学方程式:__________________________。(2) Fe2O3[Fe(OH)3]__________; 化学方程式:_______________________________________。(3) FeSO4溶液(CuSO4)_________________________________; 化学方程式:_______________________________________。(4) FeCl3溶(FeCl2)________________________; 化学方程式:______________________________________。加足量铁粉,然后过滤2Fe3++Fe=3Fe2+ 加热加足量铁粉,充分反应后过滤Cu2++Fe=Fe2++Cu氯水或氯气2Fe2++Cl2=2Fe3++2Cl-”铁三角“的转化① 2Fe3++H2S = ② 2Fe3++SO2+2H2O = ③ 3Fe2++4H++NO3-= ④ 5Fe2++MnO4-+8H+= ⑤ 2Fe2++H2O2+2H+ = 用离子方程式表现转化2Fe2++S↓+2H+2Fe2++4H++SO42-3Fe3++2H2O+NO↑5Fe3++Mn2++4H2O2Fe3++2H2O谢谢观看THANKS
相关资料
更多










