
116,海南省海口市海南华侨中学2023-2024学年九年级下学期四月月考化学试题B卷
展开可能用到的相对原子质量:Ca 40 C 12 O 16 Na 23 Cu 64
一、选择题(共14小题,每小题3分,共42分)
1.能用于治疗胃酸过多症的盐是( )
A. 小苏打 B. 纯碱 C. 苛性钠 D. 氢氧化铝
2.下列说法正确的是( )
A. 海面上浪花朵朵,说明分子在不断地运动
B. 工业炼铁时,可利用一氧化碳将铁从铁矿石中置换出来
C. 不同的酸都具有相似的化学性质,是因为酸溶液中都含有H+
D. 向待测液中滴入几滴无色酚酞溶液后溶液不变色,则待测液显酸性
3.下列关于物质的用途,说法错误的是( )
A. 氯化钠用作消除积雪B. 碳酸钠用作生产洗涤剂
C. 碳酸钙用作补钙剂D. 熟石灰用作干燥气体
4.下列化学方程式书写正确的是( )
A.
B.
C.
D.
5.下列离子在水中能大量共存,得到澄清透明溶液的是( )
A. Cu2+、K+、Cl-、B. Ba2+、、OH-、
C. H+、Na+、、D. Al3+、Ag+、、Cl-
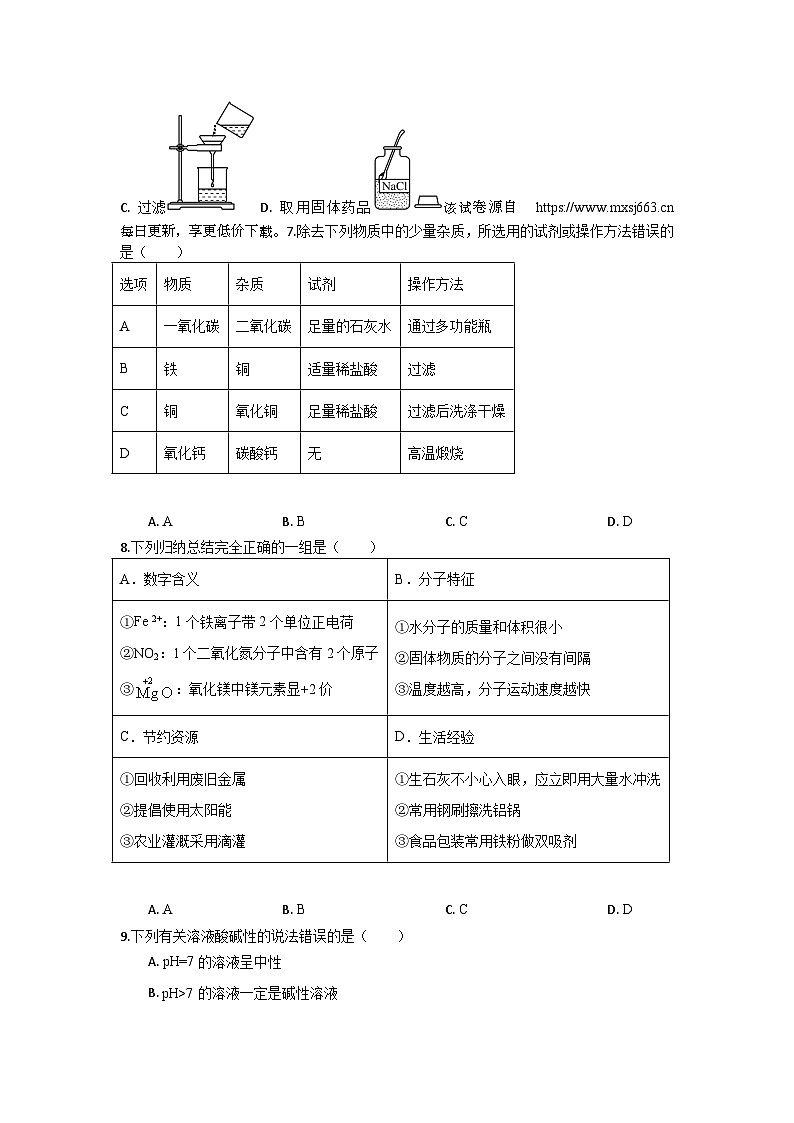
6.下图所示实验操作,正确的是( )
A. 配制 NaCl 溶液B. 稀释浓硫酸
C. 过滤D. 取用固体药品该试卷源自 每日更新,享更低价下载。7.除去下列物质中的少量杂质,所选用的试剂或操作方法错误的是( )
A. AB. BC. CD. D
8.下列归纳总结完全正确的一组是( )
A. AB. BC. CD. D
9.下列有关溶液酸碱性的说法错误的是( )
A. pH=7的溶液呈中性
B. pH>7的溶液一定是碱性溶液
C. 酸性溶液的pH<7
D. 饱和溶液一定是pH=7的溶液
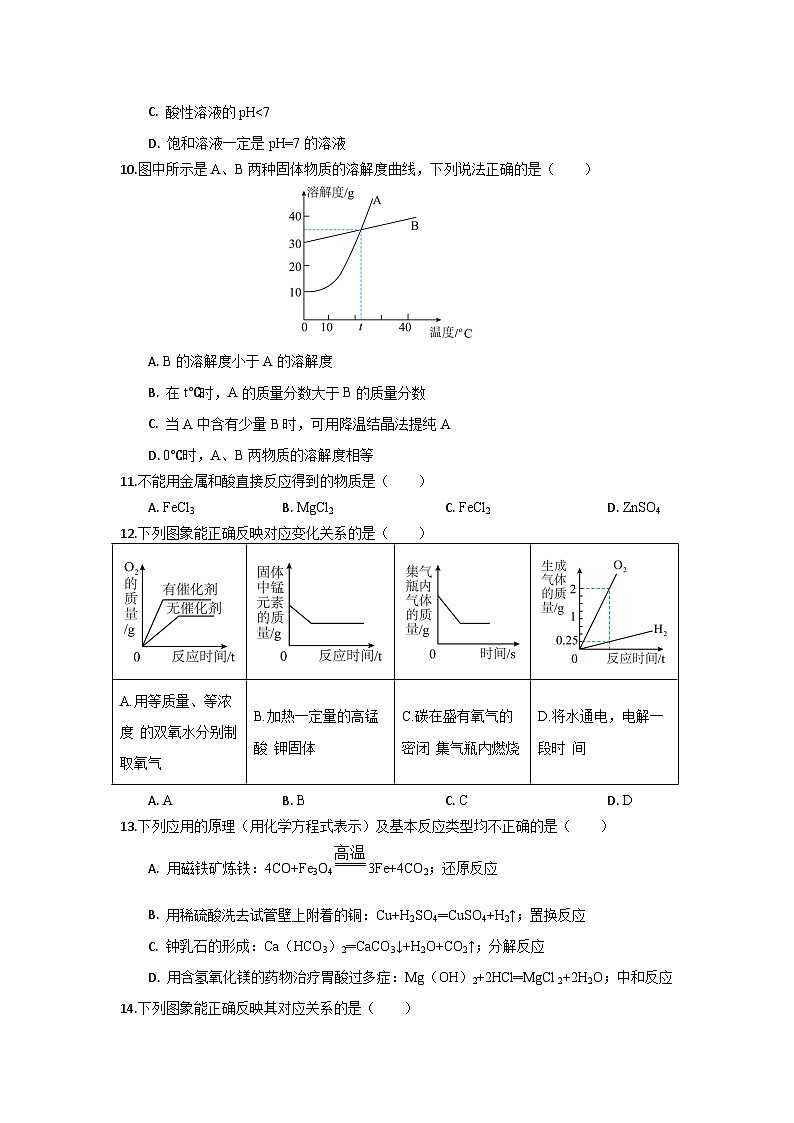
10.图中所示是A、B两种固体物质的溶解度曲线,下列说法正确的是( )
A. B的溶解度小于A的溶解度
B. 在t℃时,A的质量分数大于B的质量分数
C. 当A中含有少量B时,可用降温结晶法提纯A
D. 0℃时,A、B两物质的溶解度相等
11.不能用金属和酸直接反应得到的物质是( )
A. FeCl3B. MgCl2C. FeCl2D. ZnSO4
12.下列图象能正确反映对应变化关系的是( )
A. AB. BC. CD. D
13.下列应用的原理(用化学方程式表示)及基本反应类型均不正确的是( )
A. 用磁铁矿炼铁:4CO+Fe3O43Fe+4CO2;还原反应
B. 用稀硫酸洗去试管壁上附着的铜:Cu+H2SO4═CuSO4+H2↑;置换反应
C. 钟乳石的形成:Ca(HCO3)2═CaCO3↓+H2O+CO2↑;分解反应
D. 用含氢氧化镁的药物治疗胃酸过多症:Mg(OH)2+2HCl═MgCl2+2H2O;中和反应
14.下列图象能正确反映其对应关系的是( )
A. 恒温下,向一定质量的KNO3不饱和溶液中加入KNO3固体
B. 向一定量硝酸银溶液中加入一定量铜粉
C. 加热氯酸钾和二氧化锰的混合物
D. 向含有盐酸和CaCl2的混合溶液中逐渐滴加Na2CO3溶液
二、非选择题(共58分)
15.(8分)我国古代劳动人民在生产实践中积累了丰富的化学经验。
(1)《本草纲目》记载古法酸酒:“烧酒非古法也,自元时创始,其法用浓酒和博入瓶,蒸令气上、……其清如水,味极浓烈,盖洒露也”;
①古法酿酒所用原理与现代净水方法中的______相似,
②在甑桶中的淀粉粮食加入酒曲发酵酿酒发生______(填“缓慢氧化”或“剧烈氧化”)。
(2)《天工开物》就有以“煤饼烧石成灰,遇水为浆”的记载(注释:“石”指石灰石)。
①有关“煤饼烧石成灰”过程中的下列说法正确的是______,
A.煤作燃料
B.该过程只发生了放热反应
C.可能会造成大气污染
②“遇水为浆”所指反应的化学方程式为____________________________。
16.(10分)氢溴酸是一种和盐酸性质非常相似的酸。溴化氢(HBr)气体的水溶液是氢溴酸,无色液体,打开盛氢溴酸的试剂瓶盖,可以看到有白雾生成。已知,氢溴酸有强酸性,能与除铂、金等金属之外的很多金属发生反应,AgBr是一种难溶于硝酸的淡黄色沉淀,AgNO3溶液呈弱酸性。
(1)由“打开盛氢溴酸的试剂瓶盖看到白雾”这一现象推知氢溴酸具有______(填性质);(2)请写出氢溴酸和铁反应的化学方程式:______;
(3)下列试剂能将氢溴酸、氯化钠溶液、澄清石灰水三种溶液一次性鉴别出来的是______;
A. 稀硫酸B. 碳酸钠溶液C. 紫色石蕊溶液D. 酚酞溶液
(4)向一量的硝酸银溶液中通入HBr气体,下列图像正确的是______。
A. B. C.
17.(10分)制取干燥的二氧化碳气体,并验证二氧化碳气体与氢氧化钠溶液可以发生化学反应,设计如下探究实验。
【查阅资料】
(1)碳酸钠、水、二氧化碳可以化合生成碳酸氢钠。
(2)20℃,氢氧化钠、碳酸钠和碳酸氢钠的溶解度如下表所示
经测定,实验过程中装置D的温度保持20℃。
【定性探究】
(1)仪器a的名称是____________________;
(2)装置B中盛有 NaHCO3溶液,目的是吸收装置A中挥发出的HCl气体,写出B中发生反应的化学方程式:___________;
(3)装置C的作用是________,选择________(选填E、F)达到实验目的;
(4)在实验过程中装置D中观察到__________,说明CO2和NaOH溶液能发生反应。
【定量计算】
(5)装置D中盛有210g20℃NaOH饱和溶液中含有NaOH___________g;
(6)装置D中NaOH全部转化成Na2CO3时,理论上最多可以生成Na2CO3_______________克?
(7)当向装置D中通入足量的CO2时,可以将NaOH全部转化为NaHCO3,实验过程中会析出的 NaHCO3质量________g(不考虑结晶水)。
18.(10分)中华文化源远流长,早在西汉时期《淮南万毕术》一书中就有“曾青得铁则化为铜”的记载,这是我国现代“湿法炼铜”的先驱。某大型工厂利用此原理处理含硫酸铜的废液回收金属铜时,向100kg的废液中加入足量的铁粉,得到金属铜6.4kg。
(1)计算废液中硫酸铜的质量分数是多少?
(2)金属资源保护的有效途径之一是金属的回收再利用,其它有效途径还有_______(写一条)。
19.(10分)学校实验室的废液缸中收集了学生在实验室用锌粒和稀硫酸制取H2后的残留废液。某化学课外小组的同学想探究废液中溶质的成分,请我们共同参与探究并回答下列问题:
【提出问题】废液中的溶质是什么物质?
【作出猜想】甲同学认为废液中的溶质只有ZnSO4你认为还可能含有的溶质是______(化学式)。
【查阅资料】ZnSO4溶液呈中性。
【实验与结论】①甲同学取少量ZnSO4溶液和废液分别加入到2支试管中,并向其中分别滴加无色酚酞溶液作对比实验,结果两试管中溶液均为无色, 于是甲同学认为自己的猜想是正确的。
②你认为甲同学的实验______(填“能”或“不能”)证明他的猜想,理由是______。
③如果要证明你的猜想是正确的,你还可选择不同于上述类别的试剂是______(合理即可),反应的化学方程式为______,实验中可能观察到的现象是______。
【拓展与应用】①若实验证明你的猜想是正确的,想要处理废液只得到ZnSO4溶液,应向废液中加入过量的______,反应完全后过滤。
②通过以上探究,你认为实验室的废液未经处理直接倒入下水道,可能造成的危害是______。
20.(10分)为测定鸡蛋壳中钙元素的质量分数,小华同学取10g洗净、晾干并研磨成粉末的鸡蛋壳于烧杯中,向烧杯中加入稀盐酸,测得产生气体和加入稀盐酸的数据如下表(鸡蛋壳的主要成分是碳酸钙,其它成分不能与盐酸反应产生气体,也不含有钙元素)。
(1)鸡蛋壳中碳酸钙的质量是多少?(写出计算过程)
(2)实验过程中对测定钙元素的质量分数有影响的有______ ( 填序号);
A. 盐酸的浓度过大(浓盐酸具有挥发性)
B. 鸡蛋壳没有充分研磨
C. 鸡蛋壳没有晾干
(3)在图中画出鸡蛋壳加入稀盐酸质量为0~100g时产生的气体与加入稀盐酸变化______。
参考答案
15.【答案】(1) ①. 蒸馏 ②. 缓慢氧化
(2) ① AC ②. CaO+H2O=Ca(OH)2
【解析】【小问1详解】
①根据题中信息“其法用浓酒和博入瓶,蒸令气上”,由此可知古法酿酒所用原理与现代净水方法中的蒸馏相似。
②加入酒曲发酵酿酒发生的是不易察觉的缓慢氧化反应。
【小问2详解】
①A、“烧石成灰”指的是高温条件下碳酸钙转化为生石灰;这里的煤作为燃料,燃烧放热,提供热量,选项说法正确,符合题意;
B、煤燃烧放出热量,属于放热反应;“烧石成灰”指高温条件下碳酸钙转化为生石灰,属于吸热反应,选项说法错误,不符合题意;
C、煤的主要成分为碳,含有少量的N、S等元素,燃烧的过程中可能会产生二氧化硫、二氧化氮等有害气体,污染大气,选项说法正确,符合题意;
故选AC。
②“遇水成浆”是指氧化钙与水反应生成氢氧化钙,化学方程式为CaO+H2O=Ca(OH)2。
16.【答案】(1)挥发性 (2) (3)BC (4)C
【解析】【小问1详解】
由“打开盛氢溴酸的试剂瓶盖看到白雾”这一现象推知氢溴酸具有挥发性,挥发出的溴化氢与空气中的水蒸气结合成氢溴酸小液滴,形成白雾;
【小问2详解】
氢溴酸和铁反应生成溴化亚铁和氢气,该反应的化学方程式为:;
【小问3详解】
A、氢溴酸、氯化钠溶液和稀硫酸均不反应,均无明显现象,氢氧化钙和稀硫酸反应生成硫酸钙和水,无明显现象,无法区分,不符合题意;
B、碳酸钠能与氢溴酸反应生成溴化钠、二氧化碳和水,产生气泡,碳酸钠和氯化钠不反应,无明显现象,碳酸钠和氢氧化钙反应生成碳酸钙和氢氧化钠,产生白色沉淀,现象不同,可以去区分,符合题意;
C、氢溴酸显酸性,能使紫色石蕊试液变红,氯化钠溶液显中性,不能使紫色石蕊试液变色,澄清石灰水显碱性,能使紫色石蕊试液变蓝,现象不同,可以区分,符合题意;
D、氢溴酸显酸性,氯化钠溶液显中性,均不能使无色酚酞试液变色,澄清石灰水显碱性,能使无色酚酞试液变红,无法区分氢溴酸和氯化钠溶液,不符合题意
故选BC;
【小问4详解】
A、硝酸银溶液显酸性,pH<7,通入HBr气体,溴化氢溶于水形成氢溴酸,氢溴酸和硝酸银反应生成溴化银和硝酸,pH始终小于7,不符合题意;
B、通入HBr气体,溴化氢溶于水形成氢溴酸,氢溴酸和硝酸银反应生成溴化银和硝酸,即,由化学方程式可知,溶液质量逐渐减小,待完全反应后,继续通入溴化氢,溴化氢溶于水形成氢溴酸,溶液质量又逐渐增加,不符合题意;
C、硝酸银和氢溴酸反应生成溴化银和硝酸,实质是银离子和溴离子结合生成溴化银,故银离子数目逐渐减小至零,硝酸根离子没有参与反应,离子数目不变,符合题意。
故选C。
17.【答案】①. 长颈漏斗 ②. NaHCO3+HCl==NaCl+H2O+CO2↑ ③. 吸收二氧化碳中混有的水蒸气 ④. E ⑤. 有固体析出 ⑥. 110 ⑦. 145.75g ⑧. 221.4g
【解析】【详解】本题考查了气体的净化和干燥,溶解度的应用和计算,化学方程式的计算等。
(1)仪器a的名称是长颈漏斗;
(2)装置B中盛有 NaHCO3溶液,目的是吸收装置A中挥发出的HCl气体,NaHCO3和HCl反应生成氯化钠、水和二氧化碳,反应的化学方程式:NaHCO3+HCl==NaCl+H2O+CO2↑;
(3)欲制得干燥的二氧化碳气体,装置C的作用是吸收二氧化碳中混有的水蒸气,浓硫酸具有吸水性且不与二氧化碳反应,选择E达到实验目的;
(4)若NaOH与二氧化碳反应,生成碳酸钠和水,碳酸钠、水、二氧化碳可以化合生成碳酸氢钠,碳酸氢钠的溶解度较小,易在溶液中析出。在实验过程中装置D中观察到有固体析出,说明CO2和NaOH溶液能发生反应。
(5) 20℃NaOH的溶解度为110g,即20℃时100g水与110gNaOH形成210g饱和溶液。210g20℃NaOH饱和溶液中含有NaOH110g;
(6)设:110 g的NaOH能生成碳酸钠的质量为x
2NaOH+CO2=Na2CO3+H2O
80 106
110g x
x=145.75g
(7)设:145.75g 的碳酸钠能生成碳酸氢钠的质量为y
Na2CO3+H2O+CO2=2NaHCO3
106 168
145.75g y
y=231g,根据方程式可知在反应中水没有增加也没有减小仍为100g,溶液中溶解的NaHCO3的质量为9.4g,实验过程中会析出的 NaHCO3质量=231g-9.6g=221.4g。
18.【答案】(1)设废液中硫酸铜的质量为x
废液中硫酸铜的质量分数为
答:废液中含硫酸铜的质量分数为16%。
(2)防止金属锈蚀(或寻找金属替代品;有计划合理开采)(答案合理即得分)
【解析】【分析】硫酸铜和铁反应生成硫酸亚铁和铜。
【详解】(1)见答案。
(2)金属资源保护的有效途径之一是金属的回收再利用,其它有效途径还有防止金属锈蚀(或寻找金属替代品;有计划合理开采)。
19.【答案】 ①. H2SO4 ②. 不能 ③. 酚酞在中性、酸性溶液中均是无色 ④. 碳酸钠溶液 ⑤. ⑥. 有气泡产生 ⑦. 锌 ⑧. 腐蚀下水道
【解析】作出猜想:若是反应后硫酸剩余,则溶质除了ZnSO4还有H2SO4;
实验与结论:②由于酚酞试液在中性、酸性溶液中均为无色,故甲同学的实验不能证明他的猜想;
③要证明含有硫酸,则可以选择碳酸钠,因为碳酸钠能与硫酸反应生成硫酸钠、水、二氧化碳气体,反应的化学方程式为:,实验中可能观察到的现象是有气泡产生;
拓展与应用:①要处理废液只得到ZnSO4溶液,可以应废液中加入过量的锌,锌和硫酸反应生成硫酸锌和氢气,反应完全后过滤;
②实验室的废液未经处理直接倒入下水道,可能造成下水道的腐蚀。
20.【答案】(据表格数据可知,鸡蛋壳中碳酸钙完全反应产生气体二氧化碳质量是3.96g。
设鸡蛋壳中碳酸钙的质量是。
答:鸡蛋壳中碳酸钙的质量是9g。 (2)AC
(3)
【解析】【小问1详解】
详见答案。
【小问2详解】
A、浓盐酸具有挥发性,会增加排出气体质量,会导致实验过程中测定的钙元素的质量分数偏大。A符合题意;
B、鸡蛋壳没有充分研磨不会影响生成二氧化碳的质量,不符合题意;
C、鸡蛋壳没有晾干增加了样品质量,会导致实验过程中测定钙的元素的质量分数偏小。C符合题意。
综上所述:选择AC。
【小问3详解】
由实验数据可知,每消耗20g盐酸,产生二氧化碳0.88g,产生3.96g二氧化碳消耗盐酸质量=。所以产生气体质量与加入稀盐酸质量变化如图所示。选项
物质
杂质
试剂
操作方法
A
一氧化碳
二氧化碳
足量的石灰水
通过多功能瓶
B
铁
铜
适量稀盐酸
过滤
C
铜
氧化铜
足量稀盐酸
过滤后洗涤干燥
D
氧化钙
碳酸钙
无
高温煅烧
A.数字含义
B.分子特征
①Fe 2+:1个铁离子带2个单位正电荷
②NO2:1个二氧化氮分子中含有2个原子
③:氧化镁中镁元素显+2价
①水分子的质量和体积很小
②固体物质的分子之间没有间隔
③温度越高,分子运动速度越快
C.节约资源
D.生活经验
①回收利用废旧金属
②提倡使用太阳能
③农业灌溉采用滴灌
①生石灰不小心入眼,应立即用大量水冲洗
②常用钢刷擦洗铝锅
③食品包装常用铁粉做双吸剂
A.用等质量、等浓度 的双氧水分别制取氧气
B.加热一定量的高锰酸 钾固体
C.碳在盛有氧气的密闭 集气瓶内燃烧
D.将水通电,电解一段时 间
物质
NaOH
Na2CO3
NaHCO3
溶解度/g
110
21.8
9.6
加入稀盐酸质量/g
20
40
60
80
100
产生的气体质量/g
0.88
1.76
2.64
3.52
3.96
海南省海口市海南华侨中学2023-2024学年九年级下学期四月月考化学试题B卷(原卷版+解析版): 这是一份海南省海口市海南华侨中学2023-2024学年九年级下学期四月月考化学试题B卷(原卷版+解析版),文件包含海南省海口市海南华侨中学2023-2024学年九年级下学期四月月考化学试题B卷原卷版docx、海南省海口市海南华侨中学2023-2024学年九年级下学期四月月考化学试题B卷解析版docx等2份试卷配套教学资源,其中试卷共23页, 欢迎下载使用。
海南省海口市海南华侨中学2023-2024学年九年级下学期四月月考化学试题A卷(原卷版+解析版): 这是一份海南省海口市海南华侨中学2023-2024学年九年级下学期四月月考化学试题A卷(原卷版+解析版),文件包含海南省海口市海南华侨中学2023-2024学年九年级下学期四月月考化学试题A卷解析版docx、海南省海口市海南华侨中学2023-2024学年九年级下学期四月月考化学试题A卷原卷版docx等2份试卷配套教学资源,其中试卷共20页, 欢迎下载使用。
海南省海口市第一中学2023-2024学年九年级下学期四月月考化学试题B卷: 这是一份海南省海口市第一中学2023-2024学年九年级下学期四月月考化学试题B卷,共11页。试卷主要包含了下列显示实验操作中,正确的是,酸是一类重要的物质,下列物质的应用正确的是等内容,欢迎下载使用。












