




高教版(2021)化学通用类第一节 原子结构优质课ppt课件
展开主题一 原子结构与化学键 1.1 原子结构
1.通过分析原子的结构、组成,结合相对原子质量的计算,掌握原子的构成,发展宏观辨识与微观探析、现象观察与规律认知等化学学科核心素养。2.通过发现核外电子排列规律,掌握 1~20 号元素的原子结构示意图,明确最外层电子数与元素种类的联系,深化结构决定性质的化学观念,发展宏观辨识与微观探析、现象观察与规律认知等化学学科核心素养。3.通过了解原子结构模型演变的历史,体会科学家严谨求实的科学态度和不畏失败的科学精神;通过了解同位素在生产、生活中的作用,体会化学在人类社会文明进步中的巨大推动作用,发展科学态度与社会责任等化学学科核心素养。
铜 氯化钠 水
1.观看图片,想一想构成氯化钠、铜和水的基本微粒是什么?构成物质的微粒有哪些?氯化钠由氯离子和钠离子构成,铜由铜原子构成,水由水分子构成;构成物质的微粒有离子、原子、分子。2.这三种微粒之间有何联系?分子由原子构成,离子由原子得失电子形成。【总结】原子是构成物质的基本微粒。
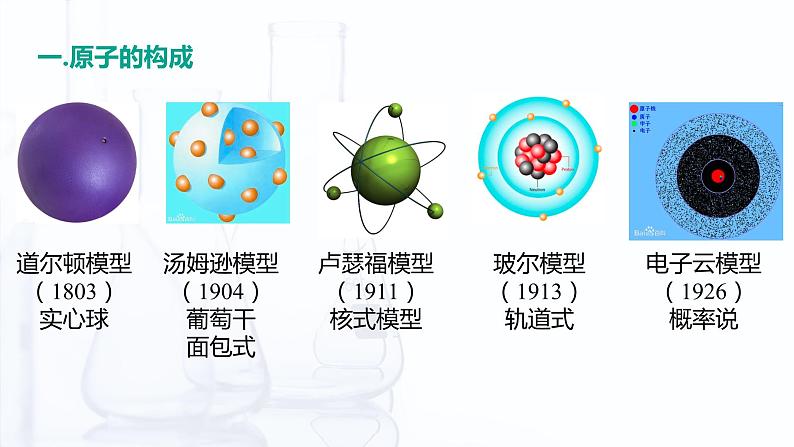
道尔顿模型(1803)实心球
汤姆逊模型(1904)葡萄干面包式
卢瑟福模型(1911)核式模型
玻尔模型(1913)轨道式
电子云模型(1926)概率说
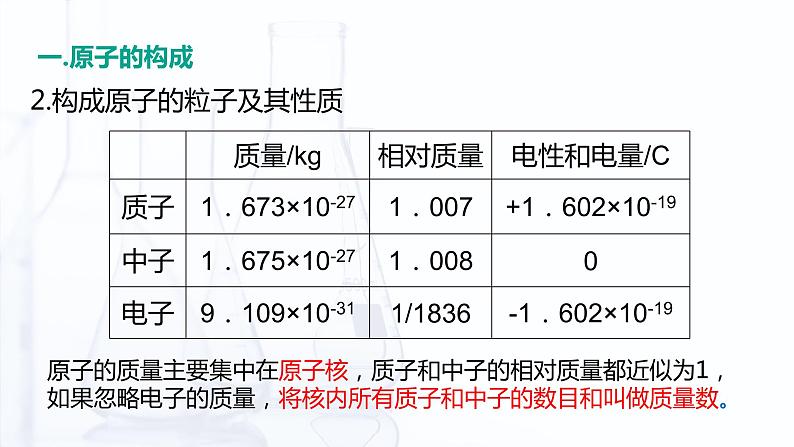
2.构成原子的粒子及其性质
原子的质量主要集中在原子核,质子和中子的相对质量都近似为1,如果忽略电子的质量,将核内所有质子和中子的数目和叫做质量数。
3.构成原子或离子的微粒间的数量关系
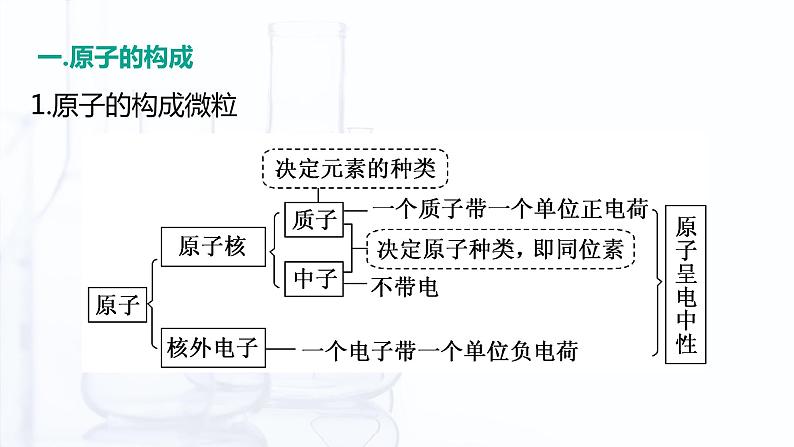
①原子中:质子数(Z)=核电荷数= =原子序数。②质量数(A)=质子数(Z)+中子数(N)。③阳离子的核外电子数=质子数- 所带电荷数。如Mg2+的核外电子数是10。④阴离子的核外电子数=质子数+ 所带电荷数。如Cl-的核外电子数是18。
①原子中:质子数(Z)=核电荷数= =原子序数。②质量数(A)=质子数(Z)+中子数(N)。
二.原子核外电子的排布
在多电子的原子里,电子分别在能量不同的区域内运动,在离核较近的区域内运动的电子能量较 ,在离核较远的区域内运动的电子能量较 ,把不同的区域简化为不连续的壳层,也称作 (如右图)。电子总是先从 层排起,这又叫核外电子的分层排布。
K L M N O P Q
电子层数越小,能量越低;电子层数越大,能量越高
表1-1-3 核电荷数 1 ~ 18 的元素原子核外电子的排布
表1-1-4 稀有气体元素原子核外电子的排布
稀有气体元素的原子最外层电子数是8 (氦是2)
结合表1-1-3、1-1-4,元素原子核外电子的排布,思考并小组讨论:①每个电子层最多容纳的电子数是多少?②最外层电子数不超过几个?③次外层电子数不超过几个?
1.核外电子排布的规律
(1)各电子层最多容纳 个电子;(2)最外层电子数不超过____个 (K层为最外层时不超过____个);(3)次外层电子数不超过___个;倒数第三层电子数不超过___个(4)核外电子总是尽先排布在能量 的电子层,然后由里向外,依次排布在能量逐步 的电子层。
结构示意图包括原子结构示意图和离子结构示意图。(1)在原子结构示意图中,“圈”表示原子核及核内质子数,“弧”表示各电子层,弧线上的数字表示该电子层上的电子数,核内质子数与核外电子数相等。(2)在离子结构示意图中,核内质子数与核外电子数不相等。
利用原子核外电子排布规律,分析溴原子的核外电子排布。
3.核外电子排布规律应用
最外层电子数大于或等于4。
最外层电子数是8或2(氦是2)。
金属元素最外层电子数较少,容易失去电子;非金属元素最外层电子数较多,容易得到电子;稀有气体元素最外层电子数是被填满的稳定结构,极不容易发生化学反应。原子的最外层电子数这一微观结构决定了元素原子的宏观性质,这就是“微观联系宏观”、“结构决定性质”。
试用原子结构示意图表示下列粒子:Na+、O、S2-、Cl
观察表1-1-5氢元素的3种原子的构成,找出这3种原子构成的相同点和不同点。
1.随着自然科学的发展,科学家们依据实验事实,提出了各种假说和原子结构模型,其中提出“带核原子结构模型”的科学家是A.汤姆生B.波尔 C.卢瑟福 D.道尔顿【答案】C
2.原子核外电子是分层排布的,在不同电子层上运动着的电子能量是不同的,下列电子层上运动的电子能量最低的是A.A层B.K层C.N层D.M层【答案】B
3.根据核外电子排布规律,M层最多容纳的电子数是A.8 B.10 C.18 D.32【答案】C
4.下列有关原子核外电子的说法错误的是A.每个电子层作为最外层时,最多可容纳8个电子B.电子在核外是分层排布的C.电子不停地做高速运动D.离原子核近的电子能量低,离原子核远的电子能量高【答案】A
5.元素的原子最外层电子得到或失去后,一定不会改变的是①元素种类;②化学性质;③相对原子质量;④微粒电性;⑤原子核;⑥电子层数;⑦最外层电子数;⑧核外电子总数。A.②③⑤B.②④⑥⑧C.②⑤D.①③⑤【答案】D
业精一分汗禾滴,爱心一颗花万朵。
P12,1.2.3
化学加工制造类学生实验 常见生物分子的性质优质ppt课件: 这是一份化学加工制造类<a href="/hx/tb_c4035025_t3/?tag_id=26" target="_blank">学生实验 常见生物分子的性质优质ppt课件</a>,共14页。PPT课件主要包含了学习目标与核心素养,实验用品,糖类的性质,蛋白质的性质,练一练等内容,欢迎下载使用。
中职化学高教版(2021)加工制造类学生实验三 溶液pH的测定备课ppt课件: 这是一份中职化学高教版(2021)加工制造类<a href="/hx/tb_c4035012_t3/?tag_id=26" target="_blank">学生实验三 溶液pH的测定备课ppt课件</a>,共1页。
中职化学高教版(2021)加工制造类第一节 原子结构精品课件ppt: 这是一份中职化学高教版(2021)加工制造类<a href="/hx/tb_c4034996_t3/?tag_id=26" target="_blank">第一节 原子结构精品课件ppt</a>,文件包含主题一第一节原子结构课件中职专用高中化学高教版2021加工制造类pptx、主题一第一节原子结构习题中职专用高中化学高教版2021加工制造类原卷版docx、主题一第一节原子结构习题中职专用高中化学高教版2021加工制造类解析版docx等3份课件配套教学资源,其中PPT共0页, 欢迎下载使用。












