

2024届广东省江门市新会华侨中学高三下学期二模考试化学试题(含答案)
展开注意事项:
1.答题前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.可能用到的相对原子质量:H 1 Be 9 C 12 O 16 Na 23 S 32 Cu 64 Zn 65
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.挖掘文物价值,讲好中国故事。下列文物不会发生电化学腐蚀的是( )
2.第十三届国际天然气转化研讨会于2024年4月底在我国举办,本次大会的主题是“迈向碳中和”,下列叙述错误的是( )
A.分子的VSEPR模型为正四面体形
B.分子是由极性键构成的非极性分子
C.的二卤代物只有1种结构
D.天然气和沼气都是可再生能源
3.下列有关物质用途及性质都正确但是二者不匹配的是选项( )
4.实验室用和浓盐酸制备(若需要加热,加热仪器已省略),最好选用( )
A.B.C.D.
5.美食是幸福生活的重要组成部分。下列有关广东美食的叙述错误的是( )
A.梅香咸鱼:鱼肉的主要成分是蛋白质
B.竹升面:制作面条时加入的“碱”指烧碱
C.肠粉:主要原料淀粉是天然高分子化合物
D.客家娘酒:制作过程中包括物理变化和化学变化
6.下列化学事实不符合“事物的双方既相互对立又相互统一”的哲学观点的是( )
A.小苏打溶液中存在电商和水解平衡
B.若硫化氢和浓硫酸反应后的含硫产物只有,既是氧化产物,又是还原产物
C.电解饱和食盐水时阴极和阳极反应同时发生
D.、、的氧化性随着卤素原子序数的增大而减弱
7.香港城市大学、中国科学院深圳先进技术研究院和深圳大学合作,证明了纳米片在酸性条件下具有本征差的析氢活性,展现出快速选择性地将硝酸根离子还原为氦的催化性能。下列有关装置放电过程(如图所示)的叙述错误的是( )
A.电子由a极经用电器流向b极
B.a极为负极,b极发生还原反应
C.b极上的电极反应式为
D.a极质量减少2.60g时,双极膜中有0.08ml 向a极区迁移
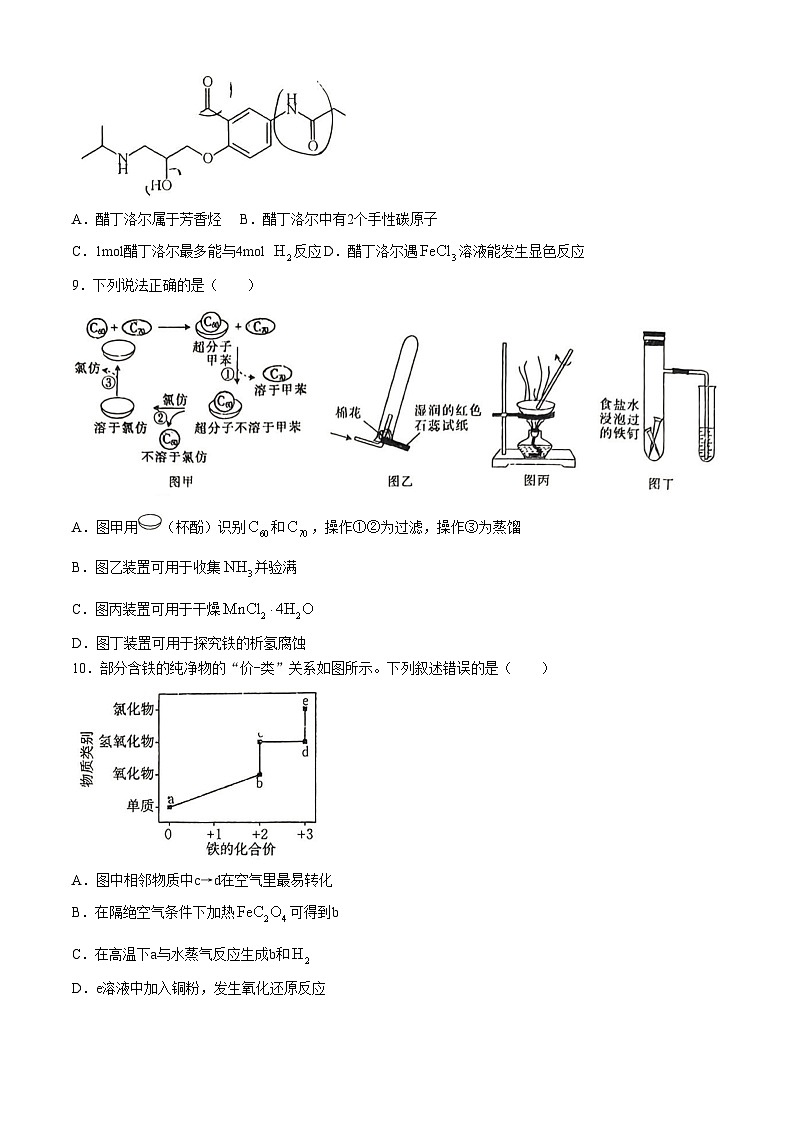
8.醋丁洛尔是治疗心动过速的阻滞剂,结构如图所示。下列叙述正确的是( )
A.醋丁洛尔属于芳香烃B.醋丁洛尔中有2个手性碳原子
C.1ml醋丁洛尔最多能与4ml 反应D.醋丁洛尔遇溶液能发生显色反应
9.下列说法正确的是( )
A.图甲用(杯酚)识别和,操作①②为过滤,操作③为蒸馏
B.图乙装置可用于收集并验满
C.图丙装置可用于干燥
D.图丁装置可用于探究铁的析氢腐蚀
10.部分含铁的纯净物的“价-类”关系如图所示。下列叙述错误的是( )
A.图中相邻物质中c→d在空气里最易转化
B.在隔绝空气条件下加热可得到b
C.在高温下a与水蒸气反应生成b和
D.e溶液中加入铜粉,发生氧化还原反应
11.代表阿伏加德罗常数的值。下列说法正确的是( )
A.1ml Na在空气中受热完全转化成,转移电子的数目为2
B.电解精炼粗铜时,阳极质量减少6.4g,外电路中通过电子的数目为0.2
C.标准状况下,22.4L 和44.8L 在光照下充分反应后分子数仍为3
D.0.2 溶液中含有和的总物质的量为0.6ml
12.根据下列实验操作及现象,能得出正确结论的是( )
13.一种新型的葡萄糖辅助Cu(Ⅰ)/Cu(Ⅱ)氧化还原耦合制氢系统工作原理如图所示。下列说法错误的是( )
A.M极为电源负极
B.P极的电极反应式为
C.电解过程中Q极发生氧化反应
D.理论上消耗18g葡萄糖,可制得0.2ml
14.X、Y、Z、W、Q是原子序数依次增大的前四周期元素且只有Q为金属元素,基态X原子核外电子占据3个能级且每个能级上的电子数相等,Z是地壳中含量(质量分数)最高的元素,基态W原子p轨道上的电子数比s轨道上的电子数多4,Q的原子序数为X、Y、W原子序数的总和。下列说法正确的是( )
A.Q位于元素周期表的ds区
B.第一电离能:X<Y<Q
C.简单氢化物的沸点:Z<Y
D.氧化物对应水化物的酸性:Y<W<X
15.烯烃是一种应用广泛的化学原料。烯烃之间存在下列三个反应:
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
在压强为pkPa的恒压密闭容器中,反应达到平衡时,三种组分的物质的量分数x随温度T的变化关系如图所示。
下列说法错误的是( )
A.反应Ⅲ的
B.700K时反应Ⅱ的平衡常数
C.欲提高的物质的量分数,需研发低温条件下活性好且耐高压的催化剂
D.超过700K后曲线a下降的原因可能是随着温度升高反应Ⅰ逆向移动,反应Ⅱ正向移动
16.常温下,将pH相同、体积均为的NaOH溶液和MOH(一元弱碱)溶液分别加水稀释至V,pH随的变化如图所示。下列说法正确的是( )
A.曲线Ⅰ表示NaOH溶液
B.未稀释前,
C.a、c两点溶液的离子总浓度相同
D.加水稀释过程中,逐渐增大
二、非选择题:本题共4小题,共56分。
17,(14分)亚硫酸钠()常作抗氧化剂、稳定剂和漂白剂。某小组拟对亚硫酸钠展开探究,回答下列问题:
实验(一) 探究水解的影响因素。
Ⅰ.配制250mL 0.1 溶液。
(1)称取固体的质量为____________g。
(2)配制该溶液不需要选择下列仪器中的____________(填标号)。
Ⅱ.实验方案如下:
(3)实验①④_____________(填“能”或“不能”)得出单一变量对实验结果的影响规律。
(4)实验①和②的目的是_______________________________________。
(5)某同学预测,实验测得,。理论预测与实际矛盾的原因可能是________________________________(答1条)。将实验③的溶液降温至25℃(标记为⑤),测得溶液pH为,小于,请你猜想可能的原因:________________________________,设计实验证明你的猜想:________________________________,猜想成立。
实验(二) 测定样品纯度。
称取wg 样品溶于水配制成100mL溶液,准确量取25.00mL制得的溶液于锥形瓶中,滴加2滴淀粉溶液,用标准c 溶液滴定至终点,消耗滴定液的体积为VmL。
(6)该样品纯度为____________%,若滴定前仰视读数,滴定终点俯视读数,则测得的结果____________(填“偏高”“偏低”或“无影响”)。
18.(14分)铍广泛用于火箭、原子能、电子工业等领域。以铍矿石(主要成分是,含少量MnO)为原料制备Be的工艺流程如图所示。
回答下列问题:
(1)“烧结”之前,将铍矿石转化成铍矿石粉的目的是________________________,浸渣的主要成分是_________________(填化学式)。
(2)“除锰”过程发生反应的离子方程式为__________________________________。
(3)制备无水过程:将溶于盐酸,蒸发浓缩、冷却结晶得到,加热和的混合物得到无水。和反应的化学方程式为______________,也可以用固体代替,的作用是_______________。
(4)Be与反应能得到BeO,如果将这个反应设计成原电池,Be极为___________极,发生___________(填“氧化”或“还原”)反应。
(5)铍和铝的性质相似。下列叙述错误的是___________(填标号)。
A.铍是一种轻金属,能与冷水反应
B.常温下,溶液的pH<7
C.氧化铍具有高熔点、耐酸碱性质
(6)离子晶体中稳定配位多面体的理论半径比如表所示。
已知:铍离子、氧离子的半径依次为45pm、140pm,预测BeO的配位多面体为_______形。
(7)铍晶胞为六方堆积结构,如图所示,铍晶体密度为__________(用含a、的代数式表示)。已知:为阿伏加德罗常数的值,晶胞底边边长为anm,高为2anm。
19.(14分)是一种对环境友好的新型能源,可直接作内燃机燃料,也可以作燃料电池的直接能量来源。基于载氮体的碳基化学链合成氨过程如下:
吸氮反应:
释氮反应:
(1)已知总反应) ,该反应能自发进行的条件为_____________(填“高温”“低温”或“任意温度”);吸氮反应正反应的活化能__________(填“>”“<”或“=”)逆反应的活化能。
(2)与传统工业合成氨相比,该工艺的优点是____________。
(3)不同碳源的吸氮反应的lnk(k为速率常数)随温度倒数的关系如图所示。已知,其中为活化能,C为截距。
吸氮反应中最好的碳源为_______________,原因是____________________。
(4)T℃下,将1ml 和足量的、放入一容积可变的密闭容器内,在催化剂作用下仅发生反应,实验测得平衡体系中气体组分的物质的量分数随压强的变化如图。
= 1 \* GB3 ①表示的物质的量分数随压强变化的曲线为____________(填“”“”或“”),理由是_________________________________________。
②该反应在b点对应条件下的压强平衡常数_________(为用分压表示的平衡常数,分压=总压×物质的量分数,用含的式子表示,列出计算式即可);达到平衡点b后,保持其他条件不变,再向容器中充入0.25ml 和0.25ml ,此时______________(填“>”“<”或“=”)。
20.(14分)一种新型镇静催眠药昂地普隆(F)的合成路线如图,请回答下列问题:
已知:①DMFDMA的结构简式为。
= 2 \* GB3 ②。
(1)A中含氧官能团的名称为_____________。
(2)B的化学式为_______________________________________。
(3)多原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可在多个原子间运动,形成离域π链,如苯分子中的离域π键可表示为,则(噻吩)中的离域π键可表示为____________。
(4)A有多种同分异构体,符合下列条件的A的同分异构体有____________种。
①与溶液发生显色反应
②含有—SH结构
(5)试剂H可通过如下流程制得。
= 1 \* GB3 ①写出反应Ⅰ的化学方程式:____________________________,该反应的反应类型为_________________。
②写出K的结构简式:______________________,K分子所含元素的电负性能由大到小的顺序为______________________。
高三化学参考答案
1.C 2.D 3.D 4.D 5.В 6.D 7.D 8.C 9.A 10.C 11.C 12.D 13.D 14.A
15.D 16.C
17.(1)6.3(1分)
(2)A(1分)
(3)不能(1分)
(4)探究浓度对水解的影响(2分)
(5)升温,部分被氧化成,降低了浓度(或升温,水的离子积常数增大等合理答案,2外);部分被氧化,使浓度降低(2外);取等体积 = 1 \* GB3 ①⑤溶液,加入足量盐酸酸化和足量,溶液,过滤、洗涤、干燥、称重,⑤的质量大于 = 1 \* GB3 ①(2分)
(6)(2分);偏低(1分)
18.(1)增大接触面积,提高反应速率(或使反应更充分等合理答案,1分);(1分)
(2)(2分)
(3)(2分);分解产生HCl,抑制水解(1分)
(4)负(1分);氧化(1分)
(5)AC(2分)
(6)四面体(1分)
(7)(2分)
19.(1)高温(1分);>(1分)
(2)条件要求低,原料廉价易得(或其他合理答案,2分)
(3)炭黑(1分);斜率越大,活化能越低,反应越容易进行(2分)
(4)(2升);该反应(气体)>0,随着压强增大,平衡逆向移动,的物质的量分数减小,且平衡时其含量小于CO(2分)
= 2 \* GB3 ②(或其他合理形式,2分);>(1分)
20.(1)酮羰基(1分)
(2)(S、N、O三种元素不分先后顺序,写对均可,2分)
(3)(2分)
(4)3(2分)
(5)①(2分);取代反应(1分)
②(2分);O>N>C>H(2分)选项
A
B
C
D
文物
名称
曾侯乙编钟
越王勾践剑
元青花四爱图梅瓶
铜鼎
选项
用途
性质
A
做豆腐时“点卤”
卤能使蛋白质聚沉
B
口服小苏打水可缓解服用阿司匹林引发的酸中毒
能与酸反应
C
脲醛塑料作电器开关和插座
脲醛的绝缘性好、耐溶剂性好
D
丁基羟基茴香醚(BHA)作脂肪制品的抗氧化剂
BHA具有可燃性
选项
实验操作及现象
结论
A
向含、的溶液中滴加溶液,先产生砖红色沉淀
B
向酸性溶液中滴加邻甲基苯胺,溶液褪色
邻甲基苯胺中氨基表现还原性
C
向碳酸钙中滴加浓硝酸,产生的气体通入溶液,产生白色沉淀
酸性:
D
将丁烷裂解产生的气体通入溴的四氯化碳溶液中,溶液褪色
丁烷裂解产物中含不饱和键
序号
0.1 溶液/mL
水/mL
水浴温度/℃
测得pH
= 1 \* GB3 ①
10.0
0
25
②
5.0
5
25
③
10.0
0
40
④
8.0
2
35
配位多面体空间结构
配位数
半径比()
平面三角形
3
0.15~0.225
四面体形
4
0.225~0.414
八面体形
6
0.414~0.732
广东省江门市新会第一中学2023-2024学年高一下学期期中考试化学试题: 这是一份广东省江门市新会第一中学2023-2024学年高一下学期期中考试化学试题,共8页。试卷主要包含了单选题,非选择题等内容,欢迎下载使用。
广东省江门市新会第一中学2023-2024学年高二上学期期末考试化学试题: 这是一份广东省江门市新会第一中学2023-2024学年高二上学期期末考试化学试题,共7页。
广东省江门市新会第一中学2023-2024学年高三上学期9月月考化学试题(无答案): 这是一份广东省江门市新会第一中学2023-2024学年高三上学期9月月考化学试题(无答案),共9页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。












