

浙江省精诚联盟2024届高三下学期三模化学试卷(Word版附解析)
展开高三化学学科试题
考生须知:
1.本试题卷共8页,满分100分,考试时间90分钟。
2.答题前,在答题卷指定区域填写班级、姓名、考场号、座位号及准考证号。
3.所有答案必须写在答题卷上,写在试卷上无效。
4.考试结束后,只需上交答题卷。
5.可能用到的相对原子质量:H 1;C 12;O 16;Mg 24;Cl 35.5。
选择题部分
一、选择题(本大题共16小题,每小题3分,共48分。每小题列出的四个备选项中只有一个是符合题目要求的,不选、多选、错选均不得分)
1.下列物质不能用作金属冶炼还原剂的是( )
A.CB.COC.D.S
2.铝可溶于NaOH溶液:,下列说法正确的是( )
A.工业上可借助此反应规模化制备B.中Al原子为杂化
C.反应后溶液碱性增强D.Al是一种两性化合物
3.下列化学用语或符号,正确的是( )
A.提示实验中要配带护目镜:
B.的价层电子对互斥模型(VSEPR)模型:
C.新戊烷的结构简式:
D.用电子式表示的形成过程:
4.在溶液中能大量共存的离子组是( )
A.、、、B.、、、
C.、、、D.、、、
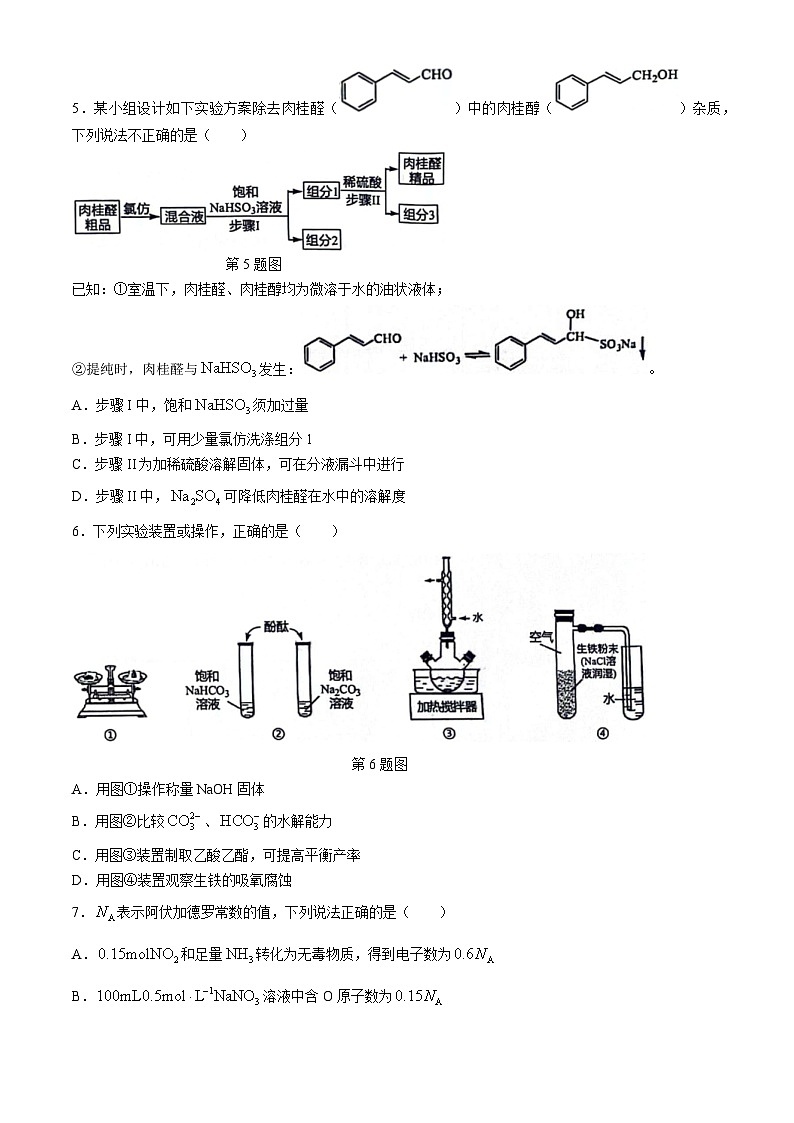
5.某小组设计如下实验方案除去肉桂醛()中的肉桂醇()杂质,下列说法不正确的是( )
第5题图
已知:①室温下,肉桂醛、肉桂醇均为微溶于水的油状液体;
②提纯时,肉桂醛与发生:。
A.步骤I中,饱和须加过量
B.步骤I中,可用少量氯仿洗涤组分1
C.步骤II为加稀硫酸溶解固体,可在分液漏斗中进行
D.步骤II中,可降低肉桂醛在水中的溶解度
6.下列实验装置或操作,正确的是( )
第6题图
A.用图①操作称量NaOH固体
B.用图②比较、的水解能力
C.用图③装置制取乙酸乙酯,可提高平衡产率
D.用图④装置观察生铁的吸氧腐蚀
7.表示阿伏加德罗常数的值,下列说法正确的是( )
A.和足量转化为无毒物质,得到电子数为
B.溶液中含O原子数为
C.含个键的气体占据体积为2.24L
D.1mlCO和个的质量比为7:4
8.下列关于有机物的说法不正确的是( )
A.可用水鉴别苯、四氯化碳和乙醇三种无色液体
B.聚苯乙烯在氯仿中因分子链之间的缠绕状态被破坏而溶解
C.纤维素乙酸酯易燃烧,是生产炸药的重要原料
D.除去乙炔中的杂质气体可选用NaOH溶液
9.表示下列过程的方程式不正确的是( )
A.乙烯加聚:
B.酸化的碘化钾淀粉试纸检验食盐中的碘:
C.一元弱酸电离:
D.氯化氢将硅与杂质分离:
10.甲基丙烯酸甲酯是合成有机玻璃的单体,可用如下方法合成:
第10题图
下列说法正确的是( )
A.试剂a是酸性溶液B.有机物X不易溶于水
C.有机物Z是D.催化剂反应前后质量不变
11.室温离子液体L由X、Y、Z、M、W五种原子序数依次增大的短周期元素组成,结构如图所示。已知Y、Z、M位于同一周期且基态原子中未成对电子数各不相同,Z与W同主族。下列说法正确的是( )
第11题图
A.室温下,L的导电性强于X、Z、M组成的盐
B.室温下,相同浓度的含氧酸的pH:
C.电负性:
D.Y或Z与M元素均不能形成平面形分子
12.下列关于电解质溶液的说法不正确的是( )
A.室温下,弱酸HA的,HA的电离度为1%
B.室温下,稀溶液中,
C.室温下,的溶液的
D.室温下,加水稀释溶液,持不变
13.中国古典科技文献《墨娥小录》记载颜料铜青的制法:“硇砂二两,明矾三两,好醋三升,二味为末,入醋内浸。次将熟铜板十斤,…‥以炭火烧通红,入药蘸……另用好醋槽一斗入盆内,将铜板子用草板子隔放,淹三日,一度刮,故名长生柜。”下列说法正确的是( )
已知:铜青的组成可能是或。
A.若用铁盆盛“醋槽”,可加速铜青的形成
B.负极电极反应式可能为
C.“草板子”作正极材料,同时可加大铜片与空气的接触面积
D.用X射线衍射法分析铜青,无法确定铜青的组成
14.镍催化下,可还原苯甲腈为苯甲胺,反应过程如下:
第14题图
下列说法不正确的是( )
A.反应过程说明苯环是一个很稳定的结构
B.中加入少量,可抑制副反应发生
C.控制pH使苯甲胺转化为可溶性胺盐,与副产物分离
D.苯甲亚胺分子的所有原子可能在同一平面
15.25℃,一定压强的某密闭容器中加入溶液,滴加盐酸或NaOH溶液(此时全溶于水且全部视作),溶液中三种含碳粒子的分布系数随溶液pOH变化如下图。下列说法不正确的是( )
第15题图
A.B.a点:
C.b点NaOH的体积小于10.00mLD.c点:
16.下列实验中,操作、现象、解释或结论均正确的是( )
非选择题部分
二、非选择题(本大题共5小题,共52分)
17.(10分)金属及其化合物是物质世界的重要组成部分。请回答:
(1)锶(Sr)、钛(Ti)、氧(O)组成的晶体的立方体晶胞如图所示,其中Sr、Ti与O的间距均相等,且Sr与O的最小间距要大于Ti与O的最小间距。
第17(1)题图
①该晶体属于________(写晶体类型名称)。
②请用小黑点在晶胞示意图中标出O所在的位置。
(2)具有高能量密度的是值得深入研究的电池正极材料。
①与C、Ni位于同一周期且同一族的元素是________(填写元素符号)。
②基态C原子的核外电子排布式是________。
(3)下列说法正确的是________(填序号)。
A.离子势:
B.与Al同周期且第一电离能小于Al的元素有2种
C.基态O原子中s能级电子数与p能级电子数相等
D.离子键百分比:
(4)金属与的配合物在一定条件下可发生如下转化:
第17(4)题图
①当分子中有个配位键时,的物质的量是________ml。
②与Na反应后,结构模型中所示的∠1将会________(选填“增大”“减小”或“不变”),原因是________。
18.(10分)某矿石的组成为,以此为原料实现如下转化:
第18题图
已知:矿石与HF反应时,元素化合价均未发生变化。
请回答:
(1)下列说法正确的是________(填序号)。
A.是由极性键形成的极性分子
B.的氧化性弱于
C.矿石中Si与O形成相互独立的正四面体结构
D.固体A中含有
(2)与矿石中金属阳离子的配位能力由强到弱的顺序是________。
(3)生成深蓝色溶液的化学方程式为________。
(4)遇酸会迅速分解,请设计实验证明氧化产物与还原产物________。遇酸分解的离子方程式为________。
19.(10分)具备高储氢密度和低成本优势,被认为是极具应用潜力的储氢材料。请回答:
(1)通过水解反应可高效制氢,反应有:
反应1:
反应2:
反应3:
则: ________
(2)等质量的在不同环境下发生反应I的产氢率如下图所示:
第19(2)题图
①在下发生水解,前3min放出(已换算为标准状况),则水解反应中消耗速率为________(计算结果保留3位小数)。
②在溶液中的产氢率明显快于纯水,已知该现象只与有关。溶液能加快产氢速率的原因是________。
(3)在300-400℃和2.4~4MPa氢气压强下,Mg可与反应:。
①恒容密闭容器中加入及足量,在四种温度下反应5min,的转化率如下表所示:
第19(3)题表
400℃时,压强平衡常数________(是用组分的平衡压强代替浓度而求得的平衡常数),下列说法正确的是________(填序号)。
A.与的总能量低于的能量
B.若在350℃下应5min,转化率大于50%
C.若360℃时反应持续至10min,转化率增大
D.将中的化学能转化为电能时,参与负极反应
②贮氢合金中氢镁原子个数比为,当氢镁原子个数比为时恒温压缩容器,请画出气体压强p与x的变化曲线。
第19(3)题图
20.(10分)二氧化氯是一种绿色氧化剂,可作漂白剂和饮用水消毒剂。易溶于水(相同条件下,在水中的溶解度约为的5倍,与水的反应可忽略)。某兴趣小组采用如下装置制备,原理为:。
第20题图
请回答:
(1)装稀硫酸的仪器的名称是________。
(2)抽气泵作用是:①抽入空气稀释气体;②________。
(3)在水中的溶解度大于的原因是________。
(4)已知:、被还原的程度随pH的不同而变化,具体情况如下:
①;②。
取装置II中的溶液1.00mL,稀释至20.00mL,加过量KI后用标准溶液滴定,消耗标准液amL。将滴定后溶液用稀硫酸调溶液pH至,补加KI且除酸后再次滴定,又消耗标准溶液bmL(注:两次滴定均只发生反应)。求纯度________(用含a、b的式子表示)。
(5)装置III中可加入的试剂有________(填序号)。
A.饱和食盐水B.溶液
C.NaOH和溶液D.溶液
(6)下列说法不正确的是________(填序号)。
A.垫上石棉网,用酒精灯煮沸装置I内溶液以加快反应
B.抽气泵的抽气速率对的产率没有影响
C.待装置II的进气管中不再产生气泡,再关闭抽气泵
D.冷却装置I中反应后的溶液,得到的晶体可作化肥
21.(12分)有机物X是一种重要的医药中间体,一种合成路线如下:
第21题图
已知:。
请回答:
(1)B的官能团名称是________。
(2)C的结构简式是________。
(3)下列说法正确的是________(填序号)。
A.甲苯转化为A的反应条件为
B.B可通过分子内反应生成盐
C.D在酸性条件下水解会生成
D.E→X转化只涉及取代反应
(4)写出G→H的化学方程式________。
(5)设计以A和HCHO为有机原料合成B的路线(用流程图表示,无机试剂任选)________。
(6)写出4种同时符合下列条件的甲苯的同分异构体的结构简式________(不考虑立体异构)。
①分子有2个环且环间共用2个碳原子,不存在“”结构。
②核磁共振氢谱显示分子中有3种不同氢原子。
2023学年第二学期浙江精诚联盟适应性联考
高三化学学科参考答案及解析
一、选择题(本大题共16小题,每小题3分,共48分。每小题列出的四个备选项中只有一个是符合题目要求的,不选、多选、错选均不得分)
1.选D。S与金属反应生成硫化物,不能作金属冶炼的还原剂。
【备注】本题源于《化学2》第98页。
2.选B。工业生产Al要消耗大量电能,再用Al制备成本太高,A项错误。中Al原子的VSEPR为4,为杂化,B项正确。反应后降低,溶液碱性减弱,C项错误。Al是单质,D项错误。
3.选A。的O原子的VSEPR为4,为正四面体,B项错误。新戊烷是:,C项错误。的形成过程,D项错误。
4.选D。
与会发生双水解而不能大量共存,A项错误。与会形成沉淀,B项错误。与会生成而不能大量共存,C项错误。
【备注】本题AB项源于《化学反应原理》第77、90页。
5.选C。肉桂醛与的反应为可逆反应,须过量以提高肉桂醛的转化率,A项正确。据流程图可知,肉桂醇可溶于氯仿、不溶于氯仿,故可用少量氯仿洗去固体表面的杂质,B项正确。分液漏斗不能作为反应容器,C项符合题意。可提高溶剂的极性,降低极性较弱的有机物肉桂醛在水中的溶解度,D项正确。
6.选D。NaOH固体易吸水潮解,称量NaOH固体须放在烧杯或称量瓶中,A项错误。饱和、的浓度不同,无法比较、的水解能力,B项错误。本装置中的冷凝管,或者酯会被冷凝回流,或者是酯逸出后无法收集,C项错误。Fe吸氧腐蚀后试管内压强减小,试管中的水会被压入导管,D项正确。
【备注】本题D项源于《化学反应原理》第90页。
7.选A。据题意,转化为和,据化合价知,1个可得4个电子,A项正确。溶液中,、中均有O原子,B项错误。1个分子中有3个键,但在标准状况下才是2.24L,C项错误。1mlCO的质量为28g,个的质量为8g,D项错误。
8.选C。苯不溶于水且密度比水小;不溶于水且密度比水大;乙醇能溶于水,A项正确。聚苯乙烯为线型高分子材料,其溶解是因分子链的缠绕状态被破坏而溶入有机溶剂,B项正确。纤维素乙酸酯不易燃烧,C项符合题意。呈酸性,乙炔不与NaOH反应,D项正确。
【备注】本题BC项源于《有机化学基础》第138,100页。
9.选A。乙烯加聚的方程式:,A项符合题意。据提示,是一元酸,又B元素周围只有6个电子,电离实质结合水给出的,C项正确。
【备注】本题ABD项源于《化学2》第69、22、124页。
10.选C。酸性会使双键断裂,A项错误。丙酮能与水互溶,B项错误。Y在作用下先水解再酯化,所以Z是,C项正确。Y水解时会生成,与作用生成,D项错误。
【备注】本题情境及CD项源于《化学2》第121页;AB项源于《有机化学基础》第85、71页。
11.选A。【元素推断】据离子液体的结构,X可形成1个共价键,为H、F、Cl;Y形成4个共价键,为C、Si;Z形成3个共价键,为N、P;W形成5个共价键,为N或P;又“Y、Z、M的基态原子中未成对电子数各不相同”,未成对电子数应是1,2,3个。所以X、Y、Z、M、W五种原子分别是H、C、N、F、P。
【解析】离子液体L室温下呈液态,呈固体,A项正确。B项未说明是“最高价含氧酸”,B项错误。根据元素周期律,电负性,C项错误。Y、Z与M形成、,分子中均有双键,均为平面形分子,D项错误。
12.选B。电离度,A项正确。溶液中,,,B项符合题意。,又,所以,C项正确。由元素质量守恒可知,,D项正确。
13.选B。铜板与铁盆接触,会形成牺牲阳极保护法,A项错误。由题意可知,Cu腐蚀后生成,B项符合题意。“草板子”不导电,不能作正极(正极是铜板中的杂质),C项错误。用X射线衍射法分析铜青,可确定晶体组成。
【备注】D项源于《物质结构与性质》第75页、《有机化学基础》第20页。
14.选C。在Ni催化下,苯环不能参与加成反应,表现出稳定性,A项正确。第(4)步反应有生成,所以在中加入少量,可抑制副反应,B项正确。苯甲基是给电子基团,所以二苯甲胺的碱性强于苯甲胺,当苯甲胺参与反应时,碱性更强的二苯甲胺早已转化为胺盐,C项符合题意。苯环与双键可能在同一平面上,D项正确。
【备注】A项源于《化学2》第71页。
15.选C。【原理分析】根据横坐标及图像,以最高点为界,左侧表示加NaOH,右侧表示加盐酸。
加盐酸: ;
加NaOH: 。
由图中横坐标可知,(据坐标7.7的交点)。又
(据坐标5.7的交点),解得。
【解析】由前面分析可知,当时,代入得,,A项正确。
据溶液电中性可得:。据元素质量守恒可得:。整理得:。又a点,所以。因溶液呈酸性,故,所以,B项正确。
假设NaOH用量为10.00mL,反应结束瞬间。因水解程度大于的电离、水解程度,故重新平衡后。所以需要再加少量NaOH使转化为,C项符合题意。
由c点坐标可得,【因为在同一份溶液中,忽略体积因素】,因,将、代入表达式,,所以,故c点有,D项正确。
16.选B。中和滴定时,锥形瓶未采取保温措施,A项错误。等pH时,酸越弱,浓度越大,反应速率越快,B项正确。加生成的黑色沉淀是CuS,C项错误。光照褪色,可能是HBrO见光分解造成持续与水反应,D项错误。
二、非选择题(本大题共5小题,共52分)
17.(10分)
(1)①离子晶体(1分)【只写“离子”得0分】
②(如图,2分)
【个数或位置错得0分,Sr与0的连线有无不作评分标准】
(2)①Fe(1分)【写名称得0分】
②或(1分)【有错得0分】
(3)AC(2分)【漏选得1分,错选得0分】
(4)①(1分)【0.09也得1分】
②减小(1分)【错选得0分】
反应时Mn得到电子,形成孤电子对,对共用电子对排斥作用增大,∠1变小(1分)【没有提到“孤电子对”得0分】
【解析】
(1)①晶体中含有Sr,根据元素周期律,Sr是活泼金属,故为离子晶体。②因“Sr、Ti、O三种粒子的间距均相等”,所以O位于面心或棱心,又“Sr与O的间距要大于Ti与O的间距”,所以O位于棱心。又一个晶胞中有3个O,故晶胞的12条棱心都有O。据此作图。
(2)①C、Ni属于第VIII族元素,所以同一周期同一族的元素是Fe。②基态C原子的核外电子排布式是。
(3)根据元素周期律和定义,半径,A项正确。与Al同周期且第一电离能小于Al的只有Na元素,B项错误。基态O原子核外电子排布为,C项正确。根据“对角线原则”,Li与Mg相似,离子键百分比:,D项错误。
(4)①1个分子中有11个配位键【5个Mn←C、Mn→H、5个C←O】,所以当存在个配位键时,为。②与Na反应后变成阴离子,Mn元素有一孤电子对,对共用电子对的排斥力增大,导致∠1减小。
18.(10分)
(1)BD(2分)【漏选得1分,错选得0分】
(2)(2分)【离子符号或顺序错即得0分】
(3)(2分)
【物质化学式有错得0分,物质化学式全对但未配平得1分,写成也可以】
(4)取少量固体,加稀硫酸溶解,用带火星的木条检验气体,复燃,说明是氧化产物;取反应后的溶液,加KSCN,变红,说明还原产物是(2分)
【成功检出一种产物得1分。用盐酸溶解,则按检出失败评论。离子符号错,其它正确得1分,若连续操作但顺序错即得0分】
(2分)
【物质化学式有错得0分,物质化学式全对但未配平得1分】
【解析】
(1)呈正四面体,是极性键形成的非极性分子,A项错误。形成配合物后,中心离子的电子云密度增大,对电子吸引力减小,氧化性弱于,B项正确。如果是独立的正四面体,则8个Si原子需要32个O原子,C项错误。由固体组成可知,Fe元素呈+2、+3价,故固体A中含有,D项正确。
(2)由可知,不能与形成配合物。的配体可被替代,而不能,故与配位能力:。
(3)生成蓝色溶液是转化为,据此可写出方程式:。
(4)由氧化还原知识可知,分解生成与,据此可设计实验进行证明:取少量固体,加稀硫酸溶解,用带火星的木条检验气体,复燃,说明氧化产物是;取反应后的溶液,加KSCN,变红,说明还原产物是。相应的方程式。
19.(10分)
(1)-283(1分)【带单位不扣分】
(2)①0.037(2分)【带单位不扣分,多于或少于3位小数得0分,误差在得1分】
②水解使溶液呈酸性,浓度增大,增强了氧化性,加快了生成速率;能溶解表面沉积的保护层,促进与水接触,提高了水解速率。(2分)
【写出一个原因得1分,其它酌情给分】
(3)①0.5(1分)【写成1/2也得1分】BD(2分)【漏选得1分,错选得0分】
②(2分)【趋势1分;前后压强相等1分】
【解析】
(1)据盖斯定律,。
(2)①生成标况下需要固体0.11g,所以反应速率为0.037g/mim。②据题意反应速率加快与“与有关”,在水中会发生水解使溶液呈酸性,据此可知:水解使溶液呈酸性,浓度增大,增强了氧化性,加快了生成速率;能溶解表面沉积的保护层,促进与水接触,提高了水解速率。
(3)①由表中数据可知,400℃时已达平衡状态,。由表格中数据可知,温度升高,平衡转化率减小,故反应为放热反应,即生成物总能量高于反应物总能量,A项错误。从速率角度看,升温,速率加快,转化率高于330℃;从平衡角度分析,降低温度,平衡转化率增大。故在350℃下应5min,转化率大于50%,B项正确。360℃时反应已达平衡,延长反应时间,转化率不变,C项错误。在原电池中,发生氧化反应,作负极,D项正确。
(4)增大压强,平衡右移,x值增大。平衡后不变,即不变,据此作图。
20.(10分)
(1)分液漏斗(1分)【字有错得0分】
(2)装将装置I中的抽入装置II中(1分)
【促进产生的溶于装置II中等合理即给分】
(3)为V形分子,是极性分子,更易溶于水等极性溶剂(2分)
【“极性分子”1分;“更易溶”或“相似相溶”1分】
(4)(2分)【有错得0分】
(5)BC(2分)【漏选得1分,错选得0分】
(6)ABC(2分)【漏选1个得1分,漏选2个或错选得0分】
【解析】
(2)通过抽气,使空气进入装置,防止浓度过高而爆炸;另一个作用是通过抽气,使装置内气体有序流动,由装置I进入装置II中溶解。
(3)根据“相似相溶”原理,极性大的溶质易溶于极性溶剂。因为V形分子,极性大,故更易溶于水。
(4)接近中性时,发生反应:、。调节pH后发生反应:。设有,,则:,,解得,,所以纯度为。
(5)装置III的作用是除去尾气中的、,因两者均有氧化性,可选择除去;可与NaOH反,具有漂白性可氧化,可用为组合试剂除去。
(6)煮沸,会导致水解成和,降低的产率,A项符合题意。抽气速率过快,不能充分溶解,B项符合题意。抽气过程中,装置II中的进气管一直有气泡,C项符合题意。装置I中的溶液有、,可作氮肥和钾肥,D项正确。
21.(12分)
(1)羧基、氨基(1分)【漏写或错写得0分】
(2)(1分)【书写合理即可得1分,位置错得0分】
(3)BC(2分)【漏选得1分,错选得0分】
(4)(2分)
【物质化学式有错、漏写得0分,条件不作要求】
(5)(3分)
【物质化学式有错得0分,合成苯乙醛、羟基苯丙酸、苯丙胺酸各得1分。其它方案合理即可,是否考虑与羧基反应均可】
(6)、、、(3分)
【合理即可。写出1个得0分,写出两个给1分,写出3个给2分,全对给3分】
【解析】
(3)甲基发生取代,反应条件为/光照,A项错误。B中含有羧基、氨基,能发生反应生成盐,B项正确。D中含有酯基、酰胺基,水解后生成,可放出,C项正确。E→F为还原反应,D项错误。
(5)逆推+顺推法。要合成,根据题给信息,需合成。为羟基羧酸,可通过HCN反应实现,需合成。可通过催化氧化得到。可通过与HCHO加成后水解得到,据此可写出合成流程。
(6)甲苯的分子式为。根据信息:“分子有2个环且环间共用2个碳原子”可推知存在结构(波浪线表示未知,该结构),说明还有2个碳碳双键。又有“3种不同氢原子”,说明分子具有对称性,据此可尝试写出同分异构体。序号
操作
现象
解释或结论
A.
用NaOH标准溶液滴定稀硫酸待测液时,用温度传感器采集锥形瓶内溶液温度变化
记录温度传感器显示的起始温度、最高温度
用计算反应中的热量变化
B.
室温下,将等质量镁(足量)分别放入等体积的HA、HB两种酸溶液中
只生成,且2分钟后酸HA收集到的更多
酸性:
C
溶液中加入足量溶液,再加入溶液
先出现白色沉淀,后变生黑色沉淀
相同温度下,
D.
将己烷与溴水的混合液置于光亮处
一段时间后,溴水褪色
己烷与在光照下发生了取代反应
温度/℃
300
330
360
400
转化率
10%
50%
50%
33.3%
浙江省精诚联盟2023届高三化学三模试题(Word版附解析): 这是一份浙江省精诚联盟2023届高三化学三模试题(Word版附解析),共23页。试卷主要包含了考试结束后,只需上交答题卷, 下列说法不正确的是等内容,欢迎下载使用。
浙江省精诚联盟2023届高三三模化学试题 Word版含解析: 这是一份浙江省精诚联盟2023届高三三模化学试题 Word版含解析,文件包含浙江省精诚联盟2023届高三三模化学试题Word版含解析docx、浙江省精诚联盟2023届高三三模化学试题Word版无答案docx等2份试卷配套教学资源,其中试卷共34页, 欢迎下载使用。
浙江省精诚联盟2023届高三三模化学试题(含解析): 这是一份浙江省精诚联盟2023届高三三模化学试题(含解析),共25页。试卷主要包含了单选题,结构与性质,元素或物质推断题,原理综合题,实验题,有机推断题等内容,欢迎下载使用。












