




广西南宁市第二中学2024届高三下学期5月月考化学试题(原卷版+解析版)
展开
这是一份广西南宁市第二中学2024届高三下学期5月月考化学试题(原卷版+解析版),文件包含广西南宁市第二中学2024届高三下学期5月月考化学试题原卷版docx、广西南宁市第二中学2024届高三下学期5月月考化学试题解析版docx等2份试卷配套教学资源,其中试卷共33页, 欢迎下载使用。
本试卷满分100分,考试用时75分钟。
注意事项:
1.答题前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将答题卡交回。
4.可能用到的相对原子质量:H 1 N14 O 16 Mg 24 Fe 56
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题意。
1. 陆川青砖青瓦烧制技艺、横州铜器制作技艺、东兰壮族服饰制作技艺、桂平乳泉井酒酿造技艺等入选了广西第九批区级非遗代表性项目。下列描述错误的是
A. 陆川青砖青瓦呈现青色的原因是含有二价铁
B. 横州出土的“鸟纹变形羽人纹铜鼓”表面的铜绿主要成分是碱式碳酸铜
C. 东兰壮族服饰原材料的主要成分为棉、麻,点燃时有烧焦羽毛的气味
D. 桂平乳泉井酒的酿造过程涉及蒸馏操作
【答案】C
【解析】
【详解】A.青砖青瓦在烧制的过程中,粘土中含有的铁未被完全氧化,还含有二价铁,A正确;
B.铜绿是因为铜与空气中的、、反应生成,B正确;
C.壮族服饰的主要原材料棉、麻的成分为纤维素,点燃没有烧焦羽毛的气味,C错误;
D.桂平乳泉井酒酿造过程中要得到高度数的白酒,需要涉及蒸馏的操作,D正确;
故选C。
2. 化学语言是表达化学思想不可缺少的重要工具。下列说法正确的是
A. AB. BC. CD. D
【答案】A
【解析】
【详解】A.HCl中共价键的电子云图,A正确;
B.硼原子序数为5,核外电子排布,最后一个电子占据2p能级简并轨道,是基态硼原子的电子排布图,B错误;
C.H2S为共价化合物,电子式:,C错误;
D.中心原子O价层电子对数:,含2对孤电子对,模型,D错误;
答案选A。
3. 下列实验装置或操作不能达到实验目的的是
A. 图甲的操作为将定容后的溶液摇匀
B. 图乙操作可用于氢氧化钠标准溶液滴定未知浓度的盐酸
C. 用丙装置观察钠在空气中燃烧的现象
D. 用丁装置检验浓硫酸与铜反应后的产物中是否含有
【答案】D
【解析】
【详解】A.配制一定物质的量浓度的溶液,定容后,反复上下颠倒,摇匀,A项正确;
B.聚四氟乙烯不和碱反应,氢氧化钠标准溶液可以盛放在使用聚四氟乙烯活塞的酸式滴定管中,B项正确;
C.可在坩埚中进行钠与氧气加热时的反应,C项正确;
D.因为反应后仍有浓硫酸,需将反应后的混合物沿烧杯内壁注入水中,边加边搅拌,D项错误;
故选D。
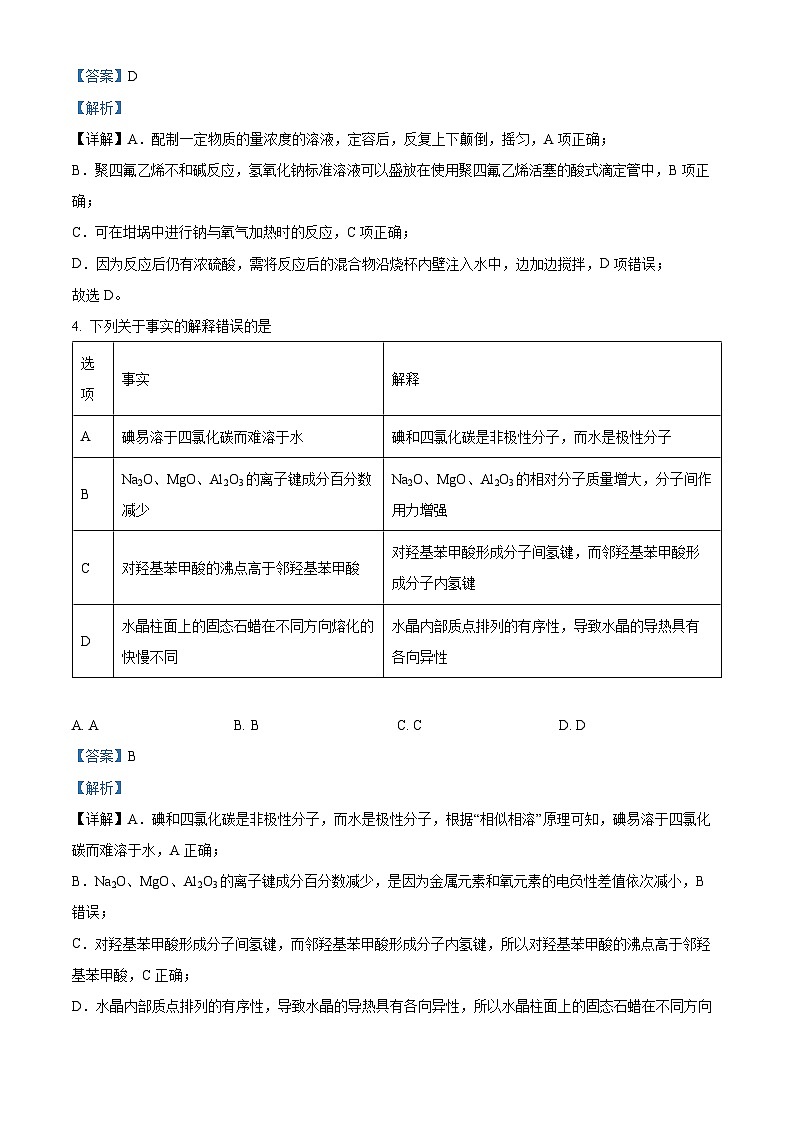
4. 下列关于事实的解释错误的是
A. AB. BC. CD. D
【答案】B
【解析】
【详解】A.碘和四氯化碳是非极性分子,而水是极性分子,根据“相似相溶”原理可知,碘易溶于四氯化碳而难溶于水,A正确;
B.Na2O、MgO、Al2O3的离子键成分百分数减少,是因为金属元素和氧元素的电负性差值依次减小,B错误;
C.对羟基苯甲酸形成分子间氢键,而邻羟基苯甲酸形成分子内氢键,所以对羟基苯甲酸的沸点高于邻羟基苯甲酸,C正确;
D.水晶内部质点排列的有序性,导致水晶的导热具有各向异性,所以水晶柱面上的固态石蜡在不同方向熔化的快慢不同,D正确;
答案选B。
5. X、Y、Z、W是原子序数依次增大的前20号元素,常温下只有一种元素的单质为气态。基态X原子s轨道上的电子数是p轨道上的2倍,Y的简单氢化物与其最高价含氧酸反应会产生白烟,Z与X形成的某种化合物常温下为液体,基态W原子有1个未成对电子。下列说法正确的是
A. 离子半径:W>Z>YB. 氢化物的沸点:Y>Z>X
C. 最简单氢化物的键角:X>Y>ZD. 上述四种元素分别与氢元素形成的化合物都是共价化合物
【答案】C
【解析】
【分析】由题意可知,Y的简单氢化物与其最高价含氧酸反应会产生白烟,则Y为N元素;基态X原子s轨道上的电子数是p轨道上的2倍,X的原子序数比Y小,则X的电子排布式为:1s22s22p2,为C元素;Z与C形成的某种化合物为CCl4或CS2,由于四种元素中只有一种元素的单质为气态,则Z为S元素;基态W原子有1个未成对电子,为K元素。
【详解】A.电子层数越多,离子半径越大,电子层数相同,原子序数越大,离子半径越小,则离子半径:,A错误;
B.C元素的氢化物有很多种,沸点可能很大,B错误;
C.CH4中心原子C上无孤电子对,NH3中心原子N上含1对孤电子对,H2S中心原子S上含2对孤电子对,孤电子对数越多,键角越小,C正确;
D.K元素与H元素形成KH,属于离子化合物,D错误;
答案选C。
6. 荜茇酰胺是一种有抗癌活性的天然生物碱,其结构如图所示。下列有关该化合物的说法正确的是
A. 含有5种官能团
B. 存在顺反异构和手性碳原子
C. 可发生加聚反应和水解反应
D. 1ml该物质最多消耗7mlH2
【答案】C
【解析】
【详解】A.根据结构简式可知,分子中含酮羰基、碳碳双键和酰胺基3中官能团,A错误;
B.形成碳碳双键的碳原子连接不同的原子或原子团,存在顺反异构;手性碳原子是指连接4个不同的原子或原子团的碳原子,根据结构简式可知,不存在手性碳原子,B错误;
C.分子中存在碳碳双键,可发生加聚反应,存在酰胺基,可发生水解反应,C正确;
D.1个分子中含1个苯环和2个碳碳双键,1ml该物质最多消耗5mlH2,D错误;
答案选C。
7. 芬顿法常用于废水的处理,反应为:NH4OCN+3H2O2=N2↑+CO2↑+5H2O,设NA为阿伏加德罗常数,下列有关说法正确的是
A. 100g质量分数为17%的H2O2溶液中,氧原子总数为NA
B. 0℃,101KPa下,22.4L CO2中含有σ键数目为4NA
C. 25℃,101KPa下,20g D2O中含有中子数目为10NA
D. 1ml NH4OCN参与反应时转移电子数为3NA
【答案】C
【解析】
【详解】A.100g质量分数为17%的H2O2溶液中,,,含氧原子数,溶液中H2O也含氧原子,所以氧原子总数大于,A错误;
B.每个CO2中含2个σ键,则0℃,101KPa下,22.4L CO2物质的量为1ml,含σ键数目为2NA,B错误;
C.每个D2O中含有中子数为10,20g D2O物质的量为1ml,含有中子数目为10NA,C正确;
D.NH4OCN中N元素化合价为-3价,反应生成氮气,N元素化合价升高至0价,1ml NH4OCN参与反应时转移电子数为6NA,D错误;
答案选C。
8. 明矾是一种常用的净水剂,以废易拉罐(含有Al和少量Fe、Mg杂质)为原料制取明矾的实验流程如图。下列说法错误的是
A. 滤渣的主要成分是Fe(OH)3和Mg(OH)2
B. “碱溶”步骤中发生反应的离子方程式为2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑
C. 上述流程中可用过量CO2代替NH4HCO3
D. “一系列操作”为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
【答案】A
【解析】
【分析】废易拉罐(含有Al和少量Fe、Mg杂质),可选择浓NaOH溶解,得到四羟基合铝酸钠溶液,并通过过滤除去不溶于碱的杂质Fe、Mg, 滤液中加入NH4HCO3溶液后,促进[Al(OH)4]-水解生成Al(OH)3沉淀,过滤后将沉淀溶解在稀硫酸中,得到硫酸铝溶液,添加K2SO4溶液后蒸发浓缩并冷却结晶得到晶体明矾,据此分析回答问题。
【详解】A.由分析可知,滤渣的主要成分是Fe和Mg,A错误;
B.“碱溶”步骤中Al和NaOH溶液反应生成Na[Al(OH)4]和H2,离子方程式为:2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑,B正确;
C.碳酸的酸性强于Al(OH)3,向Na[Al(OH)4]溶液中通入二氧化碳也能将[Al(OH)4]-转化为Al(OH)3,C正确;
D.操作a为从溶液中析出明矾晶体,由分析可知,包含蒸发浓缩、冷却结晶、过滤、洗涤、干燥等,D正确;
故选A。
9. 化学是一门以实验为基础的学科。下列实验操作或方法可达到目的的是
A. AB. BC. CD. D
【答案】D
【解析】
【详解】A.一般用质谱法测定有机物的相对分子质量,测定分子空间结构最普遍的方法X射线衍射,故A错误;
B.氢氧化铝能溶于强碱,不与弱碱氨水反应,则向浓度均为和溶液中滴加浓氨水至过量都生成白色沉淀,无法比较Mg和Al的金属性强弱,故B错误;
C.压缩容积,二氧化氮浓度变大,混合气体的颜色变深,无法证明是平衡移动造成的浓度变化,故C错误;
D.向5mL0.2ml/LMgCl2溶液中滴加少量NaOH溶液,氢氧化钠全部转化成氢氧化镁,振荡充分后,再滴加几滴0.2ml/LCuCl2溶液,如果白色沉淀转化成蓝色沉淀,说明氢氧化镁的溶度积大于氢氧化铜的溶度积,故D正确;
故选D。
10. -种能捕获和释放的电化学装置如下图所示。其中a、b均为惰性电极,电解质溶液均为KCl溶液。当K连接时,b极区溶液能捕获通入的。
下列说法不正确的是
A. K连接时,b极发生反应:
B. K连接时。a连接电源正极
C. K连接时,a极区的值增大
D. 该装置通过“充电”和“放电”调控b极区溶液pH,捕获和释放
【答案】C
【解析】
【分析】当K连接时,b极区溶液能捕获通入的,右侧为b极,充电时b为阴极,得电子发生还原反应,a为阳极失电子发生氧化反应;放电时a为正极发生还原反应,得电子,b为负极发生氧化反应,失电子,据此分析解题。
【详解】A.K连接时,为电解池,阴极得电子,发生还原反应, b极发生反应:,A正确;
B.K连接时,a为阳极,与连接电源正极相连,B正确;
C.K连接时,为原电池,a极为正极,发生还原反应,得电子,,a极区的值减小,C错误;
D.该装置通过“充电”和“放电”OH-浓度调控b极区溶液pH,捕获和释放,D正确;
故选C。
11. 氨氮废水是造成水体富营养化的原因之一,下图为处理氨氮废水的流程。
下列离子方程式书写错误的是
A. 过程I将转化为NH3:+OH-NH3↑+H2O
B. 过程II将残留的NH3∙H2O转化N2:3ClO-+2NH3∙H2O=3Cl-+N2↑+5H2O
C. 过程III将残留的NaClO转化NaCl:ClO-+SO=Cl-+SO
D. Na2SO3溶液呈碱性的原因:SO+2H2O=H2SO3+2OH-
【答案】D
【解析】
【分析】废水中与NaOH在加热下转化为NH3和水,NaClO与NH3∙H2O发生氧化还原反应生成NaCl和N2,亚硫酸钠将NaClO还原为NaCl,自身被氧化为硫酸钠;
【详解】A.过程I中与NaOH在加热下转化为NH3和水,离子方程式为+OH-NH3↑+H2O,故A正确;
B.过程II中NaClO具有氧化性,与NH3∙H2O发生氧化还原反应生成NaCl和N2,反应的离子方程式3ClO-+2NH3∙H2O=3Cl-+N2↑+5H2O,故B正确;
C.亚硫酸钠具有还原性,过程III 亚硫酸钠将NaClO还原为NaCl,自身被氧化为硫酸钠,离子方程式:ClO-+ =Cl-+,故C正确;
D.Na2SO3溶液中亚硫酸根离子发生两步水解反应,呈碱性的原因:+H2O +OH-、+H2OH2SO3+OH-,故D错误;
故答案选D。
12. 铁与镁组成的储氢合金的立方晶胞结构如图所示。铁原子位于顶点和面心的位置,镁原子位于将晶胞平分为8个立方单位的体心位置,NA为阿伏加德罗常数的值。下列说法正确的是
A. 该晶体中存在金属阳离子,所以该合金属于离子晶体
B. 该晶体密度为g·cm-3
C. 距离Fe原子最近的Mg原子数为4
D. 晶体储氢时,H2在晶胞的体心和棱的中心位置,则储氢后化学式为FeMg2H
【答案】B
【解析】
【详解】A.晶体中存在金属阳离子,没有阴离子,有自由电子,所以该合金是金属晶体,故A选项错误;
B.由晶胞结构可知,晶胞中位于顶点和面心的铁原子个数为8×18+6×12=4,位于体内的镁原子个数为8,晶胞参数为bnm,代入晶胞密度公式可得,故B选项正确;
C.由晶胞结构可知,位于顶点的铁原子与位于体对角线上镁原子的距离最近,则铁原子的配位数为8,故C选项错误;
D.由晶胞结构可知,晶胞中位于顶点和面心的铁原子个数为8×18+6×12=4,位于体内的镁原子个数为8,位于体心和棱的中心位置的氢分子个数为12×14+1=4,氢后化学式为FeMg2H2,故D选项错误;
故答案选B。
13. 将催化转化成CO是实现资源化利用的关键步骤,发生的反应有
反应Ⅰ:
反应Ⅱ:
反应Ⅲ: ,0.1MPa,在密闭容器中按投料,平衡时各组分的摩尔分数[物质i的摩尔分数:,未计入]随温度的变化如图。下列说法不正确的是
A. 低温下有利于反应Ⅱ正向进行B. 曲线b为
C. P点时反应Ⅰ的约为D. 900℃时,适当增大体系压强,保持不变
【答案】C
【解析】
【分析】反应Ⅰ为吸热反应,反应Ⅱ和反应Ⅲ是放热反应,升高温度反应Ⅰ平衡正向移动,反应Ⅱ和反应Ⅲ平衡逆向移动,CO和H2的摩尔分数增大,且H2的摩尔分数大于CO,曲线b代表,a代表CO,以此解答。
【详解】A.由盖斯定律可知,反应Ⅰ+反应Ⅲ可得反应Ⅱ, =-163.9,该反应为放热反应,低温下有利于反应Ⅱ正向进行,A正确;
B.由分析可知,曲线b代表,B正确;
C.由分析可知,曲线b代表,a代表CO,当x(CO)=x(CO2)时,温度高于500℃,x(H2)>x(H2O),反应I的平衡常数Kp= ,p点温度低于500℃,反应I是吸热反应,温度降低平衡常数减小,则P点时反应I的Kp
相关试卷
这是一份重庆市第八中学校2024届高三下学期高考适应性月考(七)化学试题(原卷版+解析版),文件包含重庆市第八中学校2024届高三下学期高考适应性月考七化学试题原卷版docx、重庆市第八中学校2024届高三下学期高考适应性月考七化学试题解析版docx等2份试卷配套教学资源,其中试卷共37页, 欢迎下载使用。
这是一份上海市曹杨第二中学2024届高三下学期五月份月考化学试题(原卷版+解析版),文件包含上海市曹杨第二中学2024届高三下学期五月份月考化学试题原卷版docx、上海市曹杨第二中学2024届高三下学期五月份月考化学试题解析版docx等2份试卷配套教学资源,其中试卷共21页, 欢迎下载使用。
这是一份广西南宁市2024届高三下学期二模考试化学试题(原卷版+解析版),文件包含广西南宁市2024届高三下学期二模考试化学试题原卷版docx、广西南宁市2024届高三下学期二模考试化学试题解析版docx等2份试卷配套教学资源,其中试卷共35页, 欢迎下载使用。








