





还剩17页未读,
继续阅读
所属成套资源:全套人教版九年级化学单元复习课件
成套系列资料,整套一键下载
- 人教版九年级化学第七单元复习课件 课件 0 次下载
- 人教版九年级化学第八单元复习课件 课件 0 次下载
- 人教版九年级化学第十单元复习课件 课件 0 次下载
- 人教版九年级化学第十一单元复习课件 课件 0 次下载
- 人教版九年级化学第十二单元复课件 课件 0 次下载
人教版九年级化学第九单元复习课件
展开
这是一份人教版九年级化学第九单元复习课件,共25页。
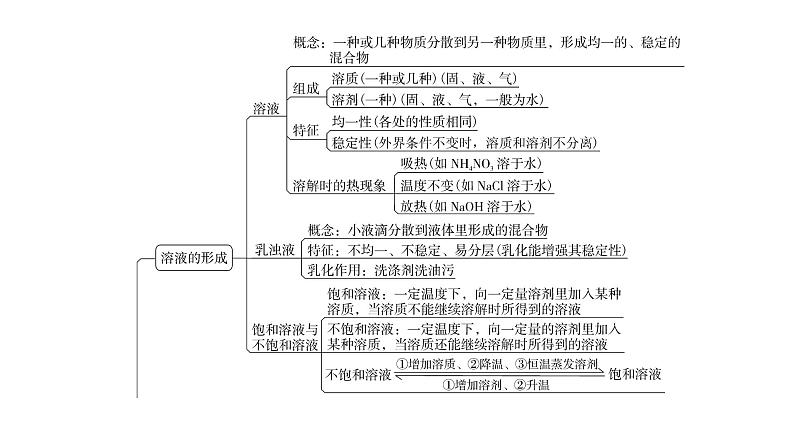
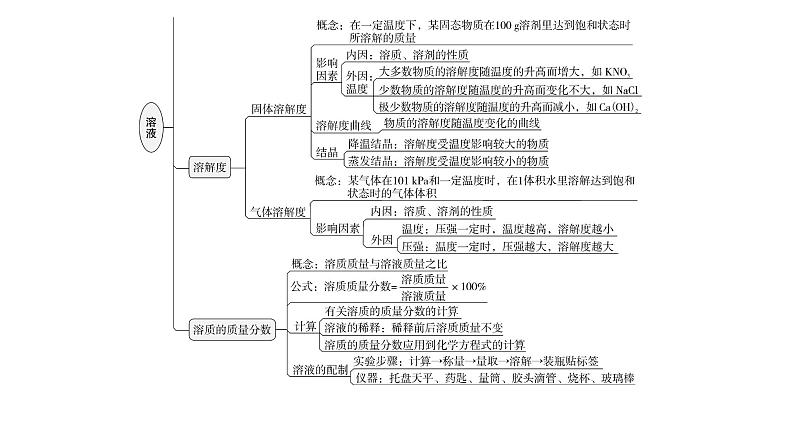
单 元 复 习第九单元复习01思维导图02易错点透析03重点突破易错点1 对溶质的质量分数理解不透彻 溶质的质量分数是溶质质量与溶液质量的比值,在计算溶质质量与溶液质量时要具体情况具体分析,如有时加入的溶质不一定能全部溶解;温度变化,有晶体析出时,此时溶质与溶液质量都有变化。【例1】下列有关溶液的说法正确的是( )易错提醒:题目中的溶液既没有指明是哪种溶液,也没有指明溶液饱不饱和,所以向其中加入溶质或升温或恒温蒸发溶剂,都要分情况分析。正解:A. 溶液中加入溶剂,溶液质量一定增大,故A正确;B. 若是饱和溶液时,向该饱和溶液中恒温加入溶质,溶质不会再溶解,所以溶质的质量分数不变,故B错误;C. 溶液升温,溶液中无晶体析出时,溶质的质量分数不变;溶液中有晶体析出时,溶质的质量分数减小,故C错误;D. 恒温蒸发溶剂,若是饱和溶液,析出部分晶体后,溶液仍为饱和溶液,相同温度下的同种物质的饱和溶液溶质质量分数因溶解度相同而相等,故D错误。答案:A1. 下列有关溶液的说法中,正确的是( )A易错点2 未能正确认识和使用溶解度曲线 溶解度曲线表示的是溶解度随温度变化的曲线,线上的点和线上面区域的点表示的是该温度下的饱和溶液,而线下面的区域对应的是该温度下的不饱和溶液。【例2】X、Y、Z三种物质的溶解度曲线如图9-F-1所示,下列说法正确的是( )图9-F-1易错提醒:对溶解度的描述和比较,一定要指明温度,否则没有意义。正解:A. 溶解度与温度有关,没有指明温度,无法确定Y的溶解度,故A错误;B. t2 ℃时,X、Y两种物质的溶解度均为50 g,溶解度相等,故B正确;C. t1 ℃时,图中Y曲线的位置最高,溶解度最大,X、Z的曲线相交,说明X、Z两种物质的溶解度相等,则t1 ℃时,X、Y、Z三种物质的溶解度由大到小顺序是Y>X=Z,故C错误;D. t2 ℃时,X的溶解度为50 g,50 g水与50 g X混合,最多只能溶解25 g X,得到75 g的饱和溶液,故D错误。答案:B学以致用2. 如图9-F-2是a、b、c三种物质的溶解度曲线,下列说法不正确的是( D )图9-F-2D重点1 溶液的形成1. 溶液对自然界中的生命活动和人类的生产活动具有重要意义。下列说法正确的是( D )D2. 如图9-F-3所示甲、乙试管中分别盛有硝酸钾、氢氧化钙的饱和溶液,试管底部均有未溶解的固体。若向试管外盛有水的烧杯中加入少量氢氧化钠,下列分析正确的是( D )D图9-F-33. 乳化在工农业生产和日常生活中有十分广泛的应用。下列应用与乳化现象无关的是 ( B )B重点2 饱和溶液与不饱和溶液4. 将200 g溶有物质M的溶液从95 ℃降低到10 ℃,不同温度时析出物质M的质量如下表所示。下列说法正确的是( D )D5. 20 ℃时,向盛有72 g水的烧杯中加入18 g固体M,充分溶解,进行如图9-F-4所示实验(不考虑水分蒸发)。下列说法正确的是( C )图9-F-4C重点3 溶解度与溶解度曲线6. 碳酸钠的溶解度曲线如图9-F-5所示。下列说法正确的是( B )B图9-F-57. A、B、C三种固体物质的溶解度曲线如图9-F-6所示,请回答下列问题。图9-F-6(1)t3 ℃时,A、B、C三种物质的溶解度由大到小的顺序是 A>B>C 。(2)t2 ℃时,配制140 g A物质的饱和溶液需要 40 g A物质。(3)现有t1 ℃接近饱和的C溶液,在不改变溶液中溶质的质量分数的前提下,要使其变为饱和溶液,可采取的一种措施是 升高温度 。(4)若B溶液中含有少量的A物质,可采用 蒸发结晶方法提纯。A>B>C 40 升高温度 蒸发结晶重点4 溶质的质量分数8. 下列图像能正确反映对应关系的是( A )A9. 分别向装有等量水的 A、B、C 烧杯中加入 10 g、20 g、25 g 某种固体,充分溶解后,现象如图9-F-7甲所示。图9-F-7(1)三个烧杯中溶质质量分数最大的是溶液 C (填“A”“B”或“C”)。(2)烧杯 A、B、C 中的溶液一定属于饱和溶液的是 B (填“A”“B”或“C”)。C B (3)图9-F-7乙中能表示该固体溶解度曲线的是 Ⅰ (填“Ⅰ”或“Ⅱ”)。图9-F-7Ⅰ (4)由图9-F-7乙分析,若分别将100 gⅠ、Ⅱ的饱和溶液从t2 ℃降温到t1 ℃,对所得溶液的叙述正确的 cd (填字母,多选)。Ⅰ、Ⅱ都是饱和溶液 b. 溶液质量:Ⅰ>Ⅱc. 所含溶剂质量:Ⅰ<Ⅱ d. 溶质质量分数:Ⅰ>Ⅱcd
单 元 复 习第九单元复习01思维导图02易错点透析03重点突破易错点1 对溶质的质量分数理解不透彻 溶质的质量分数是溶质质量与溶液质量的比值,在计算溶质质量与溶液质量时要具体情况具体分析,如有时加入的溶质不一定能全部溶解;温度变化,有晶体析出时,此时溶质与溶液质量都有变化。【例1】下列有关溶液的说法正确的是( )易错提醒:题目中的溶液既没有指明是哪种溶液,也没有指明溶液饱不饱和,所以向其中加入溶质或升温或恒温蒸发溶剂,都要分情况分析。正解:A. 溶液中加入溶剂,溶液质量一定增大,故A正确;B. 若是饱和溶液时,向该饱和溶液中恒温加入溶质,溶质不会再溶解,所以溶质的质量分数不变,故B错误;C. 溶液升温,溶液中无晶体析出时,溶质的质量分数不变;溶液中有晶体析出时,溶质的质量分数减小,故C错误;D. 恒温蒸发溶剂,若是饱和溶液,析出部分晶体后,溶液仍为饱和溶液,相同温度下的同种物质的饱和溶液溶质质量分数因溶解度相同而相等,故D错误。答案:A1. 下列有关溶液的说法中,正确的是( )A易错点2 未能正确认识和使用溶解度曲线 溶解度曲线表示的是溶解度随温度变化的曲线,线上的点和线上面区域的点表示的是该温度下的饱和溶液,而线下面的区域对应的是该温度下的不饱和溶液。【例2】X、Y、Z三种物质的溶解度曲线如图9-F-1所示,下列说法正确的是( )图9-F-1易错提醒:对溶解度的描述和比较,一定要指明温度,否则没有意义。正解:A. 溶解度与温度有关,没有指明温度,无法确定Y的溶解度,故A错误;B. t2 ℃时,X、Y两种物质的溶解度均为50 g,溶解度相等,故B正确;C. t1 ℃时,图中Y曲线的位置最高,溶解度最大,X、Z的曲线相交,说明X、Z两种物质的溶解度相等,则t1 ℃时,X、Y、Z三种物质的溶解度由大到小顺序是Y>X=Z,故C错误;D. t2 ℃时,X的溶解度为50 g,50 g水与50 g X混合,最多只能溶解25 g X,得到75 g的饱和溶液,故D错误。答案:B学以致用2. 如图9-F-2是a、b、c三种物质的溶解度曲线,下列说法不正确的是( D )图9-F-2D重点1 溶液的形成1. 溶液对自然界中的生命活动和人类的生产活动具有重要意义。下列说法正确的是( D )D2. 如图9-F-3所示甲、乙试管中分别盛有硝酸钾、氢氧化钙的饱和溶液,试管底部均有未溶解的固体。若向试管外盛有水的烧杯中加入少量氢氧化钠,下列分析正确的是( D )D图9-F-33. 乳化在工农业生产和日常生活中有十分广泛的应用。下列应用与乳化现象无关的是 ( B )B重点2 饱和溶液与不饱和溶液4. 将200 g溶有物质M的溶液从95 ℃降低到10 ℃,不同温度时析出物质M的质量如下表所示。下列说法正确的是( D )D5. 20 ℃时,向盛有72 g水的烧杯中加入18 g固体M,充分溶解,进行如图9-F-4所示实验(不考虑水分蒸发)。下列说法正确的是( C )图9-F-4C重点3 溶解度与溶解度曲线6. 碳酸钠的溶解度曲线如图9-F-5所示。下列说法正确的是( B )B图9-F-57. A、B、C三种固体物质的溶解度曲线如图9-F-6所示,请回答下列问题。图9-F-6(1)t3 ℃时,A、B、C三种物质的溶解度由大到小的顺序是 A>B>C 。(2)t2 ℃时,配制140 g A物质的饱和溶液需要 40 g A物质。(3)现有t1 ℃接近饱和的C溶液,在不改变溶液中溶质的质量分数的前提下,要使其变为饱和溶液,可采取的一种措施是 升高温度 。(4)若B溶液中含有少量的A物质,可采用 蒸发结晶方法提纯。A>B>C 40 升高温度 蒸发结晶重点4 溶质的质量分数8. 下列图像能正确反映对应关系的是( A )A9. 分别向装有等量水的 A、B、C 烧杯中加入 10 g、20 g、25 g 某种固体,充分溶解后,现象如图9-F-7甲所示。图9-F-7(1)三个烧杯中溶质质量分数最大的是溶液 C (填“A”“B”或“C”)。(2)烧杯 A、B、C 中的溶液一定属于饱和溶液的是 B (填“A”“B”或“C”)。C B (3)图9-F-7乙中能表示该固体溶解度曲线的是 Ⅰ (填“Ⅰ”或“Ⅱ”)。图9-F-7Ⅰ (4)由图9-F-7乙分析,若分别将100 gⅠ、Ⅱ的饱和溶液从t2 ℃降温到t1 ℃,对所得溶液的叙述正确的 cd (填字母,多选)。Ⅰ、Ⅱ都是饱和溶液 b. 溶液质量:Ⅰ>Ⅱc. 所含溶剂质量:Ⅰ<Ⅱ d. 溶质质量分数:Ⅰ>Ⅱcd
相关资料
更多









