

48,广东省佛山市南海区石门中学2023-2024学年高一下学期5月期中考试化学试题
展开
这是一份48,广东省佛山市南海区石门中学2023-2024学年高一下学期5月期中考试化学试题,共20页。试卷主要包含了5 Fe-56, 下列化学用语使用正确的是, 化学反应A+B→C分两步进行等内容,欢迎下载使用。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 A1-27 C1-35.5 Fe-56
第Ⅰ卷(共44分)
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1. 中国三峡博物馆是重庆最大的综合性博物馆。下列馆藏精品中,主要成分为传统无机非金属材料的是
A. AB. BC. CD. D
【答案】B
【解析】
【详解】A.商青铜三羊尊是合金,不是非金属材料,A不选;
B.陶瓷是传统无机非金属材料,B选;
C.琴的主要成分为纤维素,属于有机物,C不选;
D.丝绸的主要成分为蛋白质,属于有机物,D不选;
故选B。
2. 下列化学用语使用正确的是
A. 乙烯的结构简式:CH2CH2B. 质量数为2的氢核素:
C. 丙烷分子的空间填充模型:D. Cl-结构示意图:
【答案】B
【解析】
【详解】A.乙烯的结构简式为CH2=CH2,碳碳双键不能省略,故A错误;试卷源自 期末大优惠,全站资源一元不到!即将回复原价。B.H为第1号元素,质量数为2的氢核素表示为,故B正确;
C.是丙烷的球棍模型,故C错误;
D.氯离子的结构示意图 ,故D错误;
故答案选B。
3. 下列各组物质的相互关系描述正确的是
A. 和互为同位素
B. 甲烷、乙烷、丙烷互同分异构体
C. 金刚石、、石墨互为同素异形体
D. 和互为同系物
【答案】C
【解析】
【详解】A.和是单质,不属于同位素,A项错误;
B.甲烷、乙烷、丙烷结构相似,分子式不同,不属于同分异构体,B项错误;
C.金刚石、、石墨均是C元素形成的不同单质,互为同素异形体,C项正确;
D.和结构不相似,不是同系物,D项错误;
答案选C。
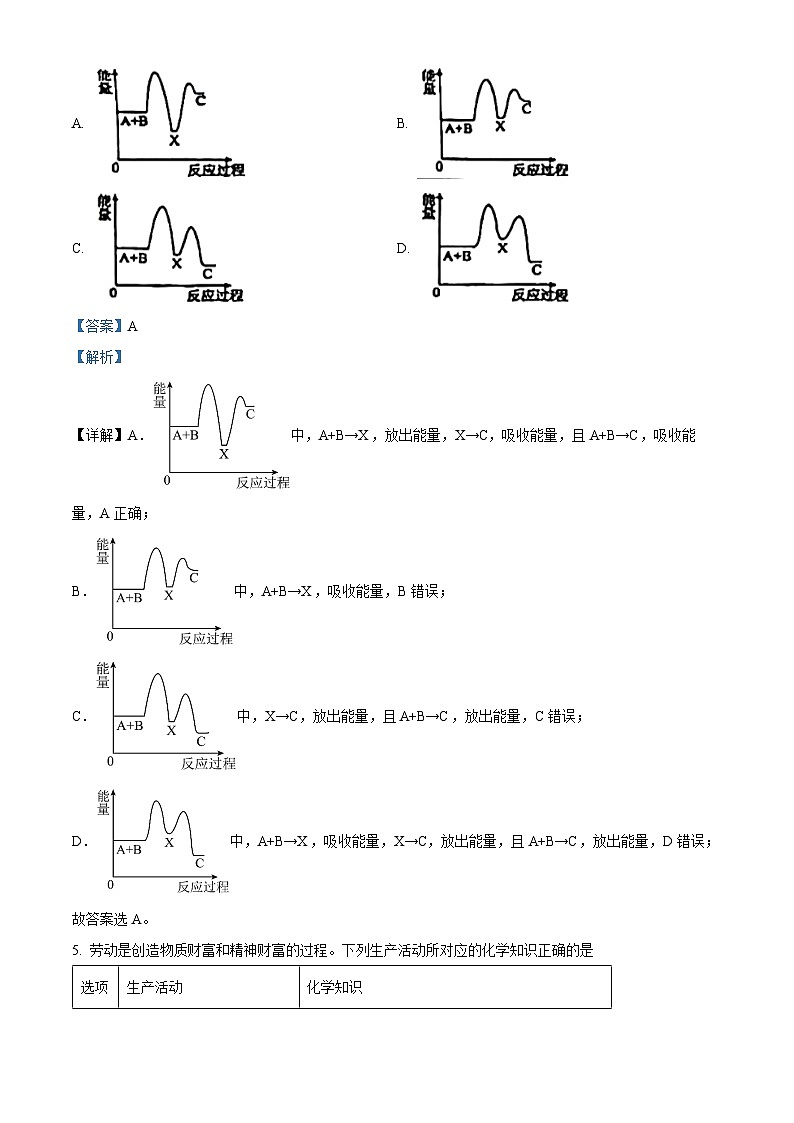
4. 化学反应A+B→C(△H>0)分两步进行:①A+B→X(△H0)。下列示意图中表示总反应过程中能量变化正确的图像是
A. B.
C. D.
【答案】A
【解析】
【详解】A.中,A+B→X,放出能量,X→C,吸收能量,且A+B→C,吸收能量,A正确;
B.中,A+B→X,吸收能量,B错误;
C.中,X→C,放出能量,且A+B→C,放出能量,C错误;
D.中,A+B→X,吸收能量,X→C,放出能量,且A+B→C,放出能量,D错误;
故答案选A。
5. 劳动是创造物质财富和精神财富的过程。下列生产活动所对应的化学知识正确的是
A. AB. BC. CD. D
【答案】C
【解析】
【详解】A.利用FeCl3溶液刻蚀印刷电路板,2Fe3++Cu=2Fe2++Cu2+,Cu做还原剂,Fe2+是还原产物,还原性比Fe2+的还原性强,不能说明Fe的活动性比Cu强,A错误;
B.用小苏打蒸馒头,碳酸氢钠受热分解为碳酸钠和水、二氧化碳,碳酸钠受热不分解,B错误;
C.氮磷钾是植物所需的营养元素,磷酸氢二铵为复合肥,C正确;
D.漂白粉中的次氯酸钙具有强氧化性,能杀菌消毒,不是氯化钙,D错误;
故答案选C。
6. 阿司匹林是一种重要的药物,化学名称为乙酰水杨酸(),水杨酸()和乙酸酐()在一定的条件下发生取代反应可制得乙酰水杨酸及物质X,下列说法正确的是
A. 水杨酸含有三种官能团
B. 乙酰水杨酸的分子式为
C. 物质X为
D. 标准状况下,1ml水杨酸和金属钠完全反应能产生11.2L氢气
【答案】C
【解析】
【详解】A.含有羟基和羧基两种官能团,A错误;
B.乙酰水杨酸的分子式为C9H8O4,B错误;
C.水杨酸()和乙酸酐()在一定的条件下发生取代反应生成乙酰水杨酸()和X,由取代反应的机理可知,X为,C正确;
D.水杨酸()中羟基和羧基都能和Na反应生成氢气,标准状况下,1ml水杨酸和金属钠完全反应能产生1mlH2,体积为22.4L,D错误;
故选C。
7. 下列各组材料组成如图装置,能形成原电池且M做正极的是
A. AB. BC. CD. D
【答案】C
【解析】
【详解】A.锌、铜和稀硫酸构成的原电池中锌是负极,银是正极,即M作负极,A不选;
B.蔗糖是非电解质,不能形成原电池,B不选;
C.银、铁和氯化铁溶液形成的原电池中铁是负极,银是正极,即M做正极,C选;
D.铝和氢氧化钠溶液反应,镁、铝和氢氧化钠溶液形成的原电池中镁是正极,铝是负极,即M做负极,D不选;
答案选C。
8. 下列实验装置能达到实验目的的是
A. B.
C. D.
【答案】C
【解析】
【详解】A.氯水中含有次氯酸,具有漂白性,因此不能用pH试纸测定氯水pH,A选项错误;
B.铝热反应为铝和氧化铁反应,采用铝粉和氧化铁的混合物,B选项错误;
C.固液分离采用过滤操作,使用仪器为烧杯、漏斗、玻璃棒,操作时注意“一贴二低三靠”,C选项正确;
D.制备氢氧化铁胶体应在沸水中滴加饱和氯化铁溶液,加热至液体变为红褐色,D选项错误;
故答案选C。
9. 下列反应的离子方程式书写正确的是
A. 用醋酸除水壶水垢():
B. “海水提镁”中用石灰乳沉镁:
C. 向溶液中滴加少量氯水,溶液颜色变成棕黄色:
D. 向中滴入溶液至恰好显中性:
【答案】C
【解析】
【详解】A.用醋酸除水壶的水垢(),醋酸为弱电解质,不能拆,故发生反应的离子方程式为:,故A项错误;
B.“海水提镁”中用石灰乳沉镁,石灰乳不能拆分为离子,所以海水提镁中用石灰乳沉镁的离子方程式为:,故B项错误;
C.向溶液中滴加少量氯水,还原性强于,先被氧化,发生的离子方程式为:,故C项正确;
D.向中滴入溶液至恰好显中性,则反应的物质的量之比为2:1,离子方程式为:,故D项错误;
故本题选C。
10. 如图所示是短周期某种非金属元素的“价-类”二维图。下列推断不正确的是
A. a与d反应产物中有离子键B. 可存在的转化
C. 常温下,d的浓溶液不能与铁发生反应D. 可用与强碱的反应来检验e中的阳离子
【答案】C
【解析】
【分析】短周期某种非金属元素的“价-类”二维图分析可知,元素最高价+5价,最低价-3价,为N元素的价类图,a为NH3,b为NO,c为NO2,d为HNO3,e为铵盐,结合物质的性质和应用分析选项。
【详解】A.由分析可知,a为NH3,d为HNO3,a与d反应产物为NH4NO3,含离子键,A正确;
B.由分析可知,a为NH3,b为NO,c为NO2,d为HNO3,可存在a→b→c→d的转化,如NH3NONO2HNO3,B正确;
C.由分析可知,d为HNO3,常温下,d的浓溶液浓硝酸能与铁发生反应,发生钝化现象,不能继续反应,C错误;
D.铵盐与强碱反应生成氨气,能使湿润的红色石蕊试纸变蓝,据此检验e中的阳离子铵根离子,D正确;
故答案为:C。
11. 根据下列实验操作和现象所得到的结论正确的是
A. AB. BC. CD. D
【答案】D
【解析】
【详解】A.酒精和水均与Na反应生成氢气,向酒精中加入少量钠块,有气泡产生,不能说明酒精中是否有水,故A错误;
B.石油裂解产物能使溴的CCl4溶液褪色,说明产物中含不饱和烃,不一定是乙烯,故B错误;
C.向蛋白质溶液中加入饱和Na2SO4溶液,产生白色沉淀,蛋白质的性质没有发生变化,为盐析过程,故C错误;
D.在淀粉溶液中加入稀硫酸,充分加热冷却后,再加入碘水,溶液变蓝,说明溶液中还存在淀粉,淀粉未完全水解,故D正确;
故选D。
12. X、Y、Z、W四种短周期元素位于三个不同的周期,且四种元素原子序数依次增大。其中,Y、Z同周期。它们能形成结构如图所示的分子,下列说法正确的是
A. 氢化物的沸点Z一定高于Y
B. Y的氧化物可以制作水晶饰品
C. X、Z、W可以形成含共价键的离子化合物
D. W元素形成的单质常温下易溶于酒精,微溶于水
【答案】C
【解析】
【分析】X、Y、Z、W四种短周期元素位于三个不同的周期,Y、Z同周期,则X位于第一周期,X形成一个共价单键,则X为H元素,Y能形成4个共价单键或2个单键和1个双键,则Y为C元素,Z形成3个共价单键,则Z为N元素,W为第三周期元素,与C能形成双键,则W为S元素。
【详解】A.Y为C元素,C元素形成的氢化物含有多种烃,碳原子数大于17时,烃的状态为固态,其沸点高于氨气,故A错误;
B.水晶饰品的成分为SiO2,Y为C元素,C元素的氧化物不能制作水晶饰品,故B错误;
C.X、Z、W形成的化合物(NH4)2S中, 和S2-之间以离子键结合,中含有共价键, (NH4)2S为含共价键的离子化合物,故C正确;
D.硫单质难溶于水,微溶于乙醇,故D错误;
故答案选C。
13. 用NA表示阿伏伽德罗常数的值,下列说法正确的是
A. 17gNH3通入水中充分反应,溶液中NH3·H2O分子数为NA
B. 现有乙烯二丙烯的混合气体共14g,其原子总数为3NA
C. 常温常压下,100g46%的乙醇溶液中,含H-O键的数目为NA
D. 足量的铜与0.5L12ml/L浓硝酸充分反应,转移的电子数目为6NA
【答案】B
【解析】
【详解】A.17gNH3物质的量为1ml,根据,溶液中NH3·H2O分子数小于NA,A错误;
B.乙烯、丙烯的最简式相同,都为CH2,则14g乙烯、丙烯的混合气体中含有原子的数目,B正确;
C.乙醇溶液中的乙醇和水均含有氢氧键,则100g46%的乙醇溶液中含有的氢氧键数目大于,C错误;
D.随着反应不断进行,浓硝酸逐渐变稀,反应停止,足量的铜与0.5L12ml/L浓硝酸充分反应,转移的电子数目小于6NA,D错误;
答案选B。
14. 同位素示踪法是研究反应机理的重要手段之一。已知1mlCH3COOH和1mlCH3CH2OD在浓硫酸作用下充分反应生成乙酸乙酯(不考虑副反应),且放出的热量为akJ。下列说法正确的是
A. 同位素(14C)示踪法常用于考古断代
B. 上述实验可用于判断该反应中乙酸和乙醇的断键位置
C. 该反应的焓变△H=-akJ/ml
D. 平衡体系中同时含有H2O、HDO和D2O
【答案】D
【解析】
【详解】A.14C常用于考古断代是因为其有固定的半衰期,而不是采用示踪法,故A错误;
B.上述乙酸和乙醇反应,无论酸脱羟基醇脱氢,还是酸脱氢醇脱羟基,最终D原子均进入水中,无法确定断键位置,故B错误;
C.该反应为可逆反应,乙醇和乙酸并没有完全反应,焓变应该小于-akJ/ml,故C错误;
D.CH3COOH和CH3CH2OD反应生成HDO,生成的乙酸乙酯与HDO发生逆反应时D原子可以进入乙酸中得到CH3COOD,H原子可以进入乙醇中得到CH3CH2OH,得到的酸与醇之间反应时会生成 H2O、HDO和D2O,故D正确;
故选:D。
15. 在体积恒定为2L的密闭容器中发生反应:X(g)4Y(s)+Z(g)。其他条件相同,在200℃和a℃时,X的浓度随时间变化的曲线如图所示。下列说法不正确的是
A. 由图可知,a小于200
B. a℃、5min时,v正>v逆
C. a℃、8min时,c(Z)可能为0.5ml/L
D. a℃时,当压强不变时,反应达到平衡状态
【答案】C
【解析】
【详解】A.根据相同时间段内温度越低反应速率越小可知,a小于200,A正确;
B.a℃、5min时,反应未到达平衡,因此v正>v逆,B正确;
C.、8 min时,X的浓度为,即X消耗了,若Z的起始浓度为0,则Z的浓度为,若Z的起始浓度不为0,则Z的浓度大于,C错误;
D.反应为气体的分子数增大的反应,在恒温恒容条件下,反应过程中压强改变,当压强不变时,反应达到平衡状态,D正确;
故答案选C。
16. 某同学用下列装置完成了浓硫酸和SO2性质实验(夹持装置已省略)。下列说法正确的是
A. 反应后,向试管Ⅰ中的白色固体中加入蒸馏水,溶液呈蓝色
B. 取下试管Ⅲ并不断振荡,试管中出现浑浊,是因为生成了BaSO4
C. 试管Ⅳ中KMnO4溶液褪色,说明SO2具有氧化性
D. 试管Ⅴ中的NaOH溶液可用NaHSO3溶液代替
【答案】B
【解析】
【分析】浓硫酸和铜在加热条件下反应生成SO2,试管Ⅱ中品红褪色,证明二氧化硫具有漂白性;SO2不与氯化钡溶液,则试管Ⅲ中无现象;酸性高锰酸钾具有强氧化性,能够氧化二氧化硫,则试管Ⅳ中高锰酸钾褪色;试管V为NaOH溶液,用于吸收二氧化硫,防止污染环境
【详解】A.试管Ⅰ中可能有浓硫酸剩余,向浓硫酸中加水会发生危险,应该将反应后溶液沿器壁慢慢注入水中,A错误;
B.SO2无法与氯化钡溶液反应生成BaSO3,但SO2溶于水后容易被空气中的氧气氧化,生成硫酸根,从而产生硫酸钡沉淀,B正确;
C.酸性高锰酸钾具有强氧化性,试管Ⅳ中KMnO4溶液褪色,说明SO2具有还原性,C错误;
D.二氧化硫和亚硫酸氢钠不反应,不能用其代替氢氧化钠溶液,D错误;
故选B。
第Ⅱ卷(共56分)
二、非选择题:本题包括4小题,共56分。
17. 丙烯酸乙酯(CH2=CHCOOCH2CH3)存在于菠萝水果中,合成路线如图所示。
回答下列问题:
(1)A的电子式为___________,丙烯酸分子结构中的含氧官能团名称为_______。
(2)反应C10H22→2C3H6+X,其中X的所有可能结构中,一氯代物共有____种。
(3)丙烯酸乙酯可能发生的反应类型有_____(填字母)。
①加成反应 ②水解反应 ③加聚反应 ④中和反应
A. ①③B. ①②③C. ①③④D. ①②③④
(4)写出聚丙烯酸的结构简式:_________,写出丙烯酸与B反应的化学方程式:___________,该反应的反应类型是__________。
(5)下列说法正确的是________(填字母)。
a.D与丙烯酸乙酯互为同系物
b.B→C的转化是氧化反应
c.可以用酸性KMnO4溶液鉴别A和丙烯酸
d.除去B中的C可加入生石灰,再蒸馏
【答案】(1) ①. ②. 羧基
(2)4 (3)B
(4) ①. ②. CH2=CH-COOH+CH3CH2OHCH2=CH-COOCH2CH3+H2O ③. 取代反应或酯化反应
(5)bd
【解析】
【分析】B与丙烯酸反应可生成丙烯酸乙酯,说明B为乙醇;A与水反应生成乙醇,说明A为乙烯;乙醇被酸性高锰酸钾氧化生成乙酸;乙酸与乙醇法生酯化反应生成D乙酸乙酯;
【小问1详解】
A为乙烯,其电子式为:;由丙烯酸结构简式可知其含有碳碳双键和羧基两种官能团,含氧官能团为羧基;
【小问2详解】
根据元素守恒可知X的分子式为C4H10,该分子为丁烷,有正丁烷和异丁烷两种结构,各存在2种氢原子,则其一氯代物共有4种;
【小问3详解】
丙烯酸乙酯中含酯基能发生水解反应,含碳碳双键能发生加成反应、加聚反应;不能发生中和反应,故选B;
【小问4详解】
聚丙烯酸的结构简式:;丙烯酸与乙醇反应的化学方程式:CH2=CH-COOH+CH3CH2OHCH2=CH-COOCH2CH3+H2O;该反应属于取代反应或酯化反应;
【小问5详解】
D为乙酸乙酯,而丙烯酸乙酯中含碳碳双键,两者官能团不同,不是同系物,故a错误;
B为乙醇,与高锰酸钾发生氧化反应生成乙酸,故b正确;
乙醇和丙烯酸均能被高锰酸钾氧化使其褪色,不能鉴别,故c错误;
除去乙醇中的水,可加生石灰,将水转化为氢氧化钙后再蒸馏得到乙醇,故d正确。
18. 某粉煤灰(主要含Al2O3、Fe2O3、CaCO3等)的铝、铁分离工艺流程如下:
(1)“酸浸”时,
①Fe2O3发生反应的离子方程式为__________。
②当硫酸质量分数大于50%时,金属氧化物浸出率明显下降。其原因是_____。
(2)有关金属离子以氢氧化物沉淀时离子浓度随pH变化如图所示。
①“还原”操作的作用是____________。
②“沉铝”过程中加入氨水调pH的范围是5≤pH









