

山西省2024九年级化学下学期期末学情评估试卷(附答案人教版)
展开一、选择题(本大题共10个小题。每小题2分,共20分。在每小题给出的4个选项中,只有1个选项符合题目要求。)
1.推进能源资源、产业结构转型升级,推动经济社会绿色发展,是我国经济发展的重要举措,下列做法符合这一理念的是( )
A.大力发展钢铁产业 B.加大原煤开采运输
C.增加开山采矿投资 D.建设风力发电设备
2.油茶是北方地区的一种小吃,其所含的各种营养素中能为人体提供能量的是( )
A.油脂 B.水
C.维生素 D.无机盐
3.我国自主制造的航母下海,为保证航母的使用寿命,下列防锈措施不可行的是( )
A.给某些部位涂油
B.刷防锈漆
C.船体经常用稀盐酸清洗
D.用抗锈蚀性能优异的合金制造航母零部件
4.我国5G技术处于世界领先地位,氮化镓(GaN)是生产5G芯片的关键材料之一。氮化镓可通过以下反应制得:2Ga+2NH3高温2GaN+3H2,该反应为( )
A.化合反应 B.分解反应
C.置换反应 D.复分解反应
5.食品添加剂是用于改善食品品质和防腐等而在食品中加入的物质,以下物质中能用于清除食品中过量酸性物质的是( )
A.NaOH B.Na2CO3 C.NaCl D.Na2SO4
6.同学们在实验室中设计了如图所示的“喷泉实验”,若要使B中尖嘴导管口产生“喷泉”,则A中加入的固体和液体可能是( )
(第6题)
A.氯化钠和水 B.硝酸铵和水
C.硫酸铜和稀盐酸 D.石灰石和稀盐酸
7.家庭小药箱是许多家庭日常必备的用品,其中盛放的各种物品有着不同的作用。以下有关说法正确的是( )
A.碘酒中的溶质是酒精
B.医用酒精用于皮肤消毒
C.葡萄糖口服液可修补机体
D.口罩阻挡病菌的原理为蒸发
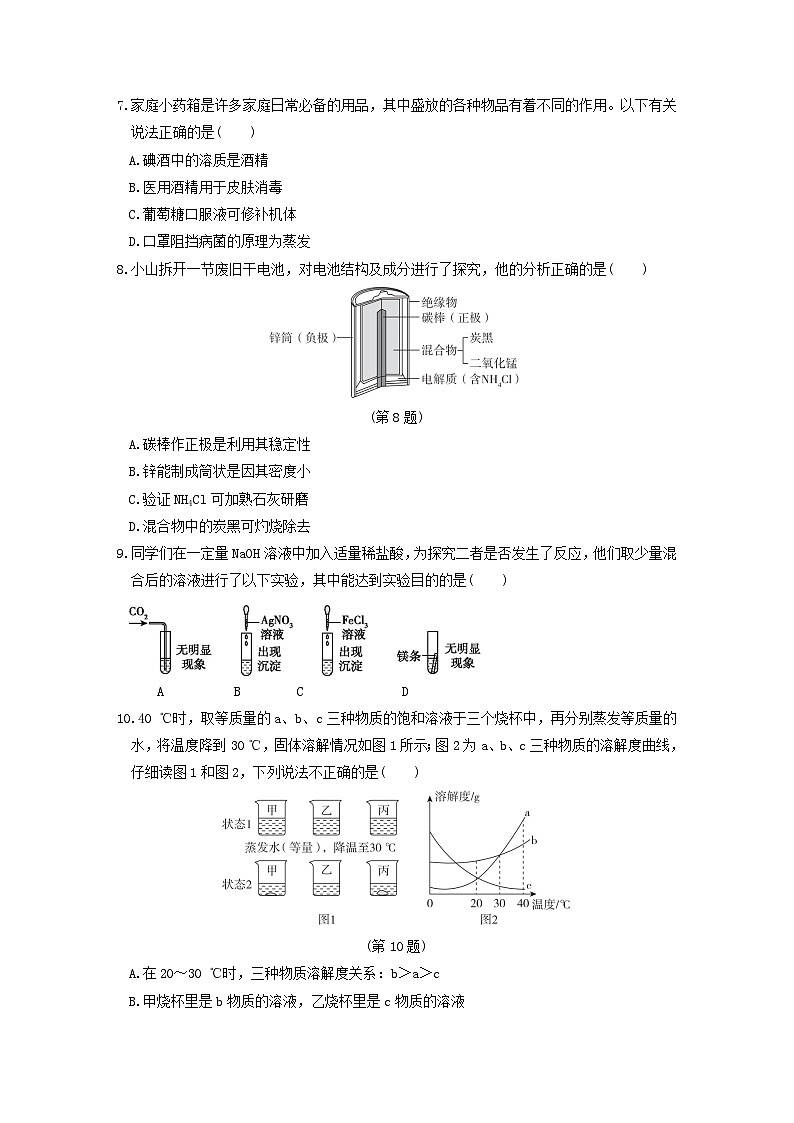
8.小山拆开一节废旧干电池,对电池结构及成分进行了探究,他的分析正确的是( )
(第8题)
A.碳棒作正极是利用其稳定性
B.锌能制成筒状是因其密度小
C.验证NH4Cl可加熟石灰研磨
D.混合物中的炭黑可灼烧除去
9.同学们在一定量NaOH溶液中加入适量稀盐酸,为探究二者是否发生了反应,他们取少量混合后的溶液进行了以下实验,其中能达到实验目的的是( )
A B C D
10.40 ℃时,取等质量的a、b、c三种物质的饱和溶液于三个烧杯中,再分别蒸发等质量的水,将温度降到30 ℃,固体溶解情况如图1所示;图2为a、b、c三种物质的溶解度曲线,仔细读图1和图2,下列说法不正确的是( )
(第10题)
A.在20~30 ℃时,三种物质溶解度关系:b>a>c
B.甲烧杯里是b物质的溶液,乙烧杯里是c物质的溶液
C.甲烧杯里是c物质的溶液,乙烧杯里是b物质的溶液
D.40 ℃时,丙烧杯溶液中水量最少
二、工程、技术应用题(本大题共5个小题。化学方程式每空2分,其余每空1分,共15分。)
【化学与工程】
我国载入史册的科技成就令人目不暇接,充分展现了新时代中国科技事业的澎湃力量。请分析图文信息,解答11~14题的相关问题。
11.首次制成栅长最小的半导体晶体管。清华大学团队利用石墨烯(单层石墨片)薄膜突破了1纳米以下半导体晶体管的研究瓶颈。从微观角度分析,石墨烯由 构成。用石墨烯作为半导体材料,利用了石墨烯的 性。
(第11题)
12.首次将二氧化碳“变成”葡萄糖。我国科研人员通过电催化结合生物合成的方式,将二氧化碳和水合成葡萄糖,并进一步合成了淀粉。自然界中合成葡萄糖的主要途径是通过植物的 ,我国科研人员这一研究的重要意义是 。
13.首次发现月球新矿物。我国科学家研究月球土壤,发现了一种新的磷酸盐矿物——“嫦娥石”,此矿物的物质类别属于 物,矿物中所含亚铁离子的符号是 ,地球岩石中至今还未发现“嫦娥石”,可能的原因是 。
(第13题)
14.中国空间站历史性完成“合体”。天和核心舱、问天实验舱与梦天实验舱形成了空间站“T”字基本构型组合体。“三舱”均由长征五号B运载火箭送入太空。用来制作火箭贮箱“防寒服”的聚氨酯泡沫塑料属于 材料。空间站运行所需的大量电能来自 能的转化。
(第14题)
【化学与技术】
15.我国有储量丰富的毒重石(主要成分为BaCO3,还有少量Fe2O3、SiO2等),工业用毒重石制备BaCl2晶体的工艺流程如下图所示。
(第15题)
(1)为使反应釜中的反应更充分,可采取的措施为 (写一种)。
(2)在反应釜中发生反应的化学方程式为 (写一个);SiO2作为反应剩余物排出,说明它所具有的性质是 。
(3)过滤池中加入的碱溶液可以是 。
(4)溶液通过蒸发池后溶质的质量分数 (填“增大”“减小”或“不变”)。
三、科普阅读题(本大题共1个小题。化学方程式每空2分,其余每空1分,共7分。)
16. “花式”土壤
土壤圈是岩石圈最外面一层疏松的部分,地球上所有的生命都依赖于它的存在,它是联系有机界和无机界的中心环节。土壤里腐殖质含量的多少和矿物质组成的差异,会让土壤呈现不同的颜色。
土壤腐殖质由动植物残体演变而成,一般黏附在土粒的表面,它的含量多少可以调节土壤颜色的深浅。黑色土一般腐殖质含量较高,而腐殖质含量较少的土则呈现灰色或灰白色。
土壤还会呈现其他美丽的颜色。紫色土中富含钙、磷、钾等,由紫色砂岩和页岩风化物发育形成。白色土的颜色常常与土壤里的氯化钠、碳酸钙、碳酸钠、硫酸钠等物质密切相关,当有高岭土、氢氧化铝等物质的粉末存在时,土壤也会显白色。氧化铁是土壤矿物质中的调色高手,当它在土壤中的含量高时,土色就会发红,甚至呈棕红色;在低洼潮湿的环境中,氧化铁与水作用转变为黄色的水合氧化铁,从而使土壤显黄色。
阅读文本,回答问题:
(1)腐殖质的含量与土壤颜色有什么关系?由此猜想腐殖质可能呈什么颜色?
。
(2)除黑色土以外,哪种颜色的土更适宜植物的生长?
。
(3)红色土在某些地区用于炼铁,请写出有关反应的化学方程式。
。
(4)山西位于黄土高原,山西土壤中一定含有哪些元素?你判断的理由是什么?
。
四、物质性质及应用题(本大题共1个小题。化学方程式每空2分,其余每空1分,共6分。)
17.学习了酸的化学性质后,某同学以稀硫酸为主题,绘制了“多彩酸世界”思维导图(如图1)。
(第17题)
(1)若得到溶液②为蓝色,可向稀硫酸中加入 (填化学式)。
(2)若看到现象⑤,此反应的化学方程式为 (写一个)。
(3)根据“多彩酸世界”思维导图,写出硫酸的一种用途: 。
(4)如图2是氢氧化钠溶液与硫酸反应时溶液pH变化的示意图。
①根据图示判断,该实验是将 (填“氢氧化钠溶液”或“硫酸”)滴加到另一种溶液中。
②滴入溶液体积为V2 mL时,溶液中的溶质为 (填化学式)。
五、定量分析题(本大题共1个小题。化学方程式1分,共7分。)
18.实验小组的同学们在做完“金属的化学性质实验”后,对含有硝酸银、硝酸铜的废液产生了兴趣,他们测定了废液中硝酸铜的质量分数,并将测定过程中的有关问题写在黑板上,与同学们分享了解决方法。
(第18题)
【观点分享】0~a段没有铜生成的原因是 。
【展示交流】结合题目要求,请写出完整的解题过程。
六、实验探究题(本大题共2个小题。化学方程式每空2分,其余每空1分,共15分。)
【实验设计】
19.在古代就有用纯碱制取烧碱的记载,为了验证这种方法制取烧碱的原理,同学们在实验室中进行了以下实验。请根据下列提示,补全实验内容。
【实验方案】
实验方法:向盛有一定量碳酸钠溶液的试管中滴加适量氢氧化钙溶液。
(1)实验原理: (用化学方程式表示)。
(2)实验现象: 。
【问题与交流】
(3)该反应能够发生的原因是 。
(4)该反应的微观实质是 。
(5)用这一反应制取烧碱时要注意 (写一条)。
【科学探究】
20.冬季下雪后,人们常使用融雪剂消除路面的积雪。化学兴趣小组的同学们对融雪剂消除积雪的原理、融雪剂的成分、使用融雪剂对环境的影响等产生了浓厚的兴趣,在老师的指导下,他们开启了项目式学习之旅。
项目一:了解融雪剂消除积雪的原理
【信息检索】
常见的融雪剂中主要含有氯化钠、氯化钙、氯化钾。融雪剂溶于水后使混合物的凝固点改变,从而融雪化冰,保障道路交通安全。
【表达交流】
(1)融雪剂中所含化合物所属物质类别是 。
(2)融雪剂溶于水后可 (填“降低”或“升高”)混合物的凝固点,以防止雪水结冰。
项目二:探究融雪剂中是否含有氯化钙
【进行实验】
【讨论交流】
③中发生反应的化学方程式是 (写一个)。
项目三:评价使用融雪剂对环境的影响
【反思评价】
长期使用融雪剂可能会腐蚀路边的钢铁制品,从环境保护的角度考虑,冬季防止路面积雪的方法还可以是 。
第二学期期末学情评估
一、1.D 2.A 3.C 4.C 5.B 6.D 7.B 8.C 9.D 10.C
二、11.碳原子;导电
12.光合作用;缓解粮食危机(合理即可)
13.混合;Fe2+;“嫦娥石”的形成环境与地球环境不同(合理即可)
14.合成;太阳
15.(1)将毒重石粉碎(合理即可)
(2)Fe2O3+6HCl2FeCl3+3H2O(合理即可);不与稀盐酸反应(合理即可)
(3)氢氧化钠溶液(合理即可)
(4)增大
三、16.(1)腐殖质越多,土壤颜色越深(合理即可);腐殖质可能呈黑色
(2)紫色土
(3)Fe2O3+3CO高温2Fe+3CO2
(4)山西土壤中一定含有H、O、Fe;氧化铁中含Fe、O,水中含H、O(合理即可)
四、17.(1)Cu(OH)2(合理即可)
(2)H2SO4+Ba(OH)2BaSO4↓+2H2O(合理即可)
(3)金属除锈(合理即可)
(4)①硫酸 ②H2SO4、Na2SO4
五、18.【观点分享】0~a段加入的铁粉与硝酸银反应生成银和硝酸亚铁
【展示交流】解:由图像可知,加入铁粉后充分反应生成的铜的质量为3.2 g,设废液中硝酸铜的质量为x。
Fe+Cu(NO3)2Cu+Fe(NO3)2
188 64
x 3.2 g
18864=x3.2g
x=9.4 g
废液中硝酸铜的质量分数为9.4g100g×100%=9.4%
答:废液中硝酸铜的质量分数为9.4%。
六、19.(1)Ca(OH)2+Na2CO3CaCO3↓+2NaOH
(2)产生白色沉淀
(3)反应物均溶于水,生成物有沉淀,符合复分解反应发生的条件
(4)钙离子与碳酸根离子结合生成碳酸钙沉淀
(5)两种反应物的用量适中(合理即可)
20.【表达交流】(1)盐 (2)降低
【进行实验】碳酸钠溶液;产生白色沉淀;硝酸银溶液;产生白色沉淀
【讨论交流】NaCl+AgNO3AgCl↓+NaNO3
[或KCl+AgNO3AgCl↓+KNO3或
CaCl2+2AgNO32AgCl↓+Ca(NO3)2]
【反思评价】使用机械除雪实验步骤
实验操作
实验现象
实验结论
①
取少量融雪剂,向其中加入一定质量的蒸馏水,搅拌、静置
得到无色
澄清溶液
融雪剂能溶于水
②
取少量上层清液于试管中,向其中滴加适量 ,振荡
该融雪剂中含有Ca2+
③
取步骤①所得上层清液于另一支试管中,滴加 ,振荡
该融雪剂中含有Cl-
陕西省2024九年级化学下学期期末学情评估试卷(附答案科粤版): 这是一份陕西省2024九年级化学下学期期末学情评估试卷(附答案科粤版),共8页。试卷主要包含了5 Fe,请结合图示分析,D 2,甲状腺疾病,2 g+0等内容,欢迎下载使用。
2024九年级化学下学期期末学情评估试卷(附答案科粤版): 这是一份2024九年级化学下学期期末学情评估试卷(附答案科粤版),共8页。试卷主要包含了5 Zn,D 2,硬度;纯铜片,2 g等内容,欢迎下载使用。
福建省2024九年级化学下学期期末学情评估试卷(附答案沪教版): 这是一份福建省2024九年级化学下学期期末学情评估试卷(附答案沪教版),共8页。试卷主要包含了碳酸钠是钠离子电池制造原料之一,9,是酸雨,懂化学会生活,下列实验方案能达到实验目的的是等内容,欢迎下载使用。












