

新教材(广西专版)高考化学一轮复习课时规范练8钠及其重要化合物含答案
展开1.下列说法正确的是( )
A.电解饱和食盐水可以得到金属钠和氯气
B.金属钠在空气中加热生成白色固体:4Na+O22Na2O
C.把水滴入盛有少量Na2O2的试管中,立即把带火星的木条放在试管口,木条复燃,反应生成了O2
D.在火焰上灼烧搅拌过某无色溶液的玻璃棒,火焰出现黄色,溶液中含Na元素
2.(2023广西河池月考)绿色化学走进课堂,某学习小组在老师的指导下,设计了“氯气与金属钠反应”的实验。实验操作:钠与氯气反应的装置可作如图改进,将一根玻璃管与氯气发生器相连,玻璃管内放一块黄豆粒大小的金属钠(已吸净煤油),玻璃管尾部塞一团浸有NaOH溶液的棉花球。先给钠预热,到钠熔化成小球时,撤火,再通入氯气,即可见钠着火燃烧,生成大量白烟。下列叙述错误的是( )
A.浸有碱液的棉花球主要用于防止空气中二氧化碳进来与钠反应
B.反应生成了大量白烟,该白烟是氯化钠晶体
C.可从实验操作“先给钠预热,到钠熔化成小球时,撤火,再通入氯气”判断钠的熔点较低
D.钠有很强的还原性,本质原因是钠原子的最外层只有1个电子,该电子很容易失去
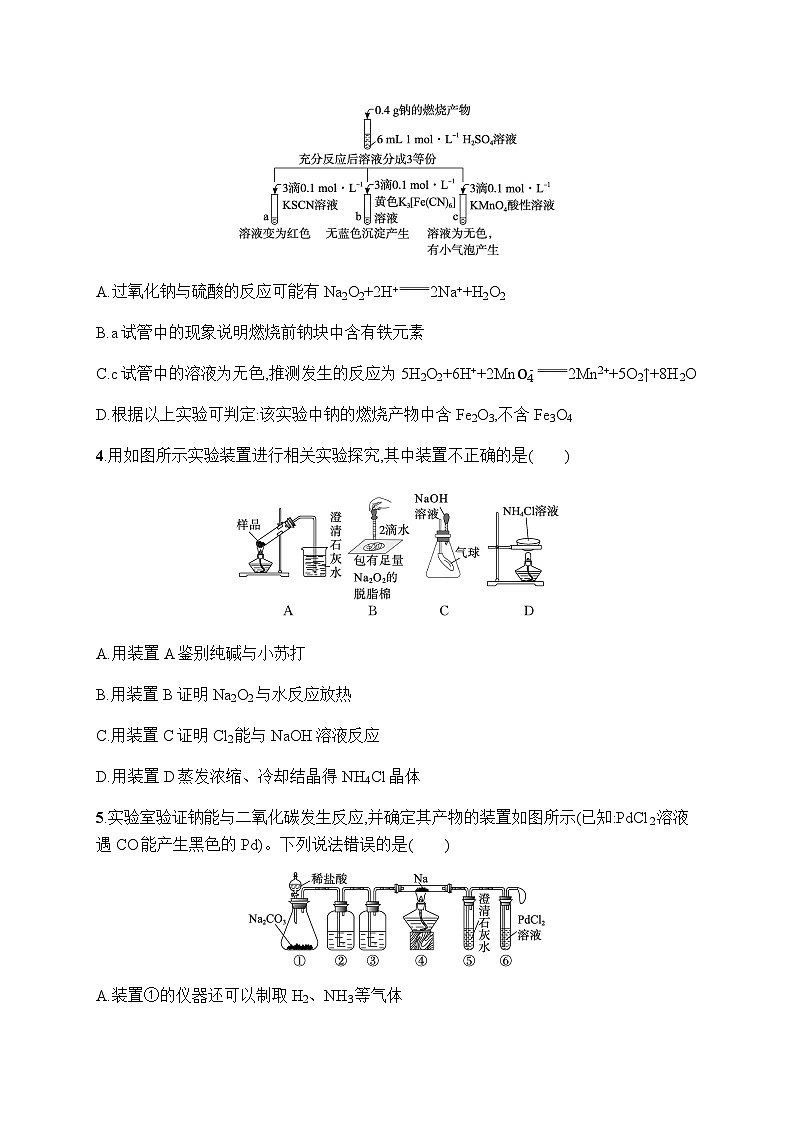
3.钠的燃烧产物中混有杂质,某研究小组进行如图所示的实验探究。下列推测错误的是( )
A.过氧化钠与硫酸的反应可能有Na2O2+2H+2Na++H2O2
B.a试管中的现象说明燃烧前钠块中含有铁元素
C.c试管中的溶液为无色,推测发生的反应为5H2O2+6H++2MnO4-2Mn2++5O2↑+8H2O
D.根据以上实验可判定:该实验中钠的燃烧产物中含Fe2O3,不含Fe3O4
4.用如图所示实验装置进行相关实验探究,其中装置不正确的是( )
A.用装置A鉴别纯碱与小苏打
B.用装置B证明Na2O2与水反应放热
C.用装置C证明Cl2能与NaOH溶液反应
D.用装置D蒸发浓缩、冷却结晶得NH4Cl晶体
5.实验室验证钠能与二氧化碳发生反应,并确定其产物的装置如图所示(已知:PdCl2溶液遇CO能产生黑色的Pd)。下列说法错误的是( )
A.装置①的仪器还可以制取H2、NH3等气体
B.装置⑤中石灰水变浑浊后,再点燃酒精灯
C.装置②③中分别盛装饱和Na2CO3溶液、浓硫酸
D.装置⑥中有黑色沉淀,发生的反应是PdCl2+CO+H2OPd↓+CO2+2HCl
6.(2023上海浦东期中)有关Na2O2性质探究实验如下:
已知:①Na2O2与水反应经历了Na2O2+2H2O2NaOH+H2O2;
②酚酞褪色原因与溶液的强碱性或强氧化性有关。
根据上述实验可以得出的结论是( )
A.双氧水能使酚酞褪色
B.浓氢氧化钠能使酚酞褪色
C.双氧水和浓氢氧化钠都能使酚酞褪色
D.可利用二氧化锰或水来完善实验方案
7.向Na2CO3、NaHCO3的混合溶液中逐滴加入稀盐酸,生成气体的量随n(HCl)的变化关系如图所示,则下列离子组在对应的溶液中一定能大量共存的是( )
A.a点对应的溶液中:Na+、OH-、SO42-、NO3-
B.b点对应的溶液中:K+、Al3+、MnO4-、SO42-
C.c点对应的溶液中:Na+、Ca2+、NO3-、Cl-
D.d点对应的溶液中:F-、NO3-、Fe2+、Ag+
8.实验室可通过沉淀法测定样品纯度,按如图装置测定纯碱(含少量NaCl)的纯度,下列说法正确的是( )
A.装置A中试剂应为浓硫酸,C中试剂应为BaCl2溶液
B.在B、C之间应增添盛有饱和NaHCO3溶液的洗气装置,以除去氯化氢气体
C.只要测定装置C在吸收CO2前后的质量差,就可以确定碳酸钠的质量分数
D.反应结束后,需经过滤、洗涤、干燥、称量等操作测定装置C中沉淀质量
9.(2023浙江温州三模)探究钠及其化合物的性质,下列方案设计、现象及结论都正确的是( )
二、非选择题:本题共2小题。
10.化工专家侯德榜发明的侯氏制碱法为我国纯碱工业和国民经济发展做出了重要贡献。某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备NaHCO3,进一步处理得到产品Na2CO3和NH4Cl,实验流程如图:
回答下列问题:
(1)从A~E中选择合适的仪器制备NaHCO3,正确的连接顺序是 (按气流方向,用小写字母表示)。为使A中分液漏斗内的稀盐酸顺利滴下,可将分液漏斗上部的玻璃塞打开或 。
(2)B中使用雾化装置的优点是 。
(3)生成NaHCO3的总反应的化学方程式为 。
(4)反应完成后,将B中U形管内的混合物处理得到固体NaHCO3和滤液。
向滤液中加入NaCl粉末,存在NaCl(s)+NH4Cl(aq)NaCl(aq)+NH4Cl(s)过程。为使NH4Cl沉淀充分析出并分离,根据NaCl和NH4Cl溶解度曲线,需采用的操作为 、 、洗涤、干燥。
(5)无水Na2CO3可作为基准物质标定盐酸浓度。称量前,若无水Na2CO3保存不当,吸收了一定量水分,用其标定盐酸浓度时,会使结果 (填字母)。
A.偏高 B.偏低 C.不变
11.某实验小组欲探究Na2CO3和NaHCO3的性质,但发现实验室里盛放两种固体的试剂瓶丢失了标签。于是他们先对固体A、B进行鉴别,再通过实验进行性质探究。
(1)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊。A受热分解的化学方程式为 。
(2)称取两种固体各2 g,分别加入两个小烧杯中,再各加10 mL蒸馏水,振荡,测量温度变化;待固体充分溶解并恢复至室温,向所得溶液中各滴入2滴酚酞溶液。
①发现Na2CO3固体完全溶解,而NaHCO3固体有剩余,由此得出结论: 。
②同学们在两烧杯中还观察到以下现象。其中盛放Na2CO3的烧杯中出现的现象是 (填字母)。
a.溶液温度下降
b.溶液温度升高
c.滴入酚酞后呈蓝色
d.滴入酚酞后呈红色
(3)如下图所示,在气密性良好的装置Ⅰ和Ⅱ中分别放入药品,将气球内的固体同时倒入试管中。
①两试管中均产生气体, (填“Ⅰ”或“Ⅱ”)的反应程度更为剧烈。
②反应结束后,气球均有膨胀,恢复至室温,下列说法正确的是 。
a.装置Ⅰ的气球体积较大
b.装置Ⅱ的气球体积较大
c.生成气体的体积根据盐酸计算
d.生成气体的体积根据固体计算
(4)同学们将两种固体分别配制成
0.5 ml·L-1的溶液,设计如下方案并对反应现象做出预测:
实施实验后,发现操作2的现象与预测有差异:产生白色沉淀和气体。则该条件下,NaHCO3溶液与CaCl2溶液反应的离子方程式为 。
参考答案
课时规范练8 钠及其重要化合物
1.C 解析 电解饱和食盐水可以得到NaOH、H2和Cl2,A项错误。金属钠在空气中加热生成淡黄色固体的化学方程式为2Na+O2Na2O2,B项错误。做焰色试验时应用铁丝或铂丝,不能用玻璃棒,D项错误。
2.A 解析 浸有碱液的棉花球主要用于吸收氯气,防止污染空气,A错误;钠与氯气反应生成氯化钠,因此生成的大量白烟是氯化钠晶体,B正确;给钠预热,钠熔化成小球,据此判断钠的熔点较低,C正确;钠原子的最外层只有1个电子,该电子很容易失去,所以钠有很强的还原性,D正确。
3.D 解析 钠燃烧的产物为过氧化钠,结合c试管中有小气泡产生且KMnO4酸性溶液褪色的现象推知过氧化钠和硫酸可能发生反应Na2O2+2H+2Na++H2O2、5H2O2+6H++2MnO4-2Mn2++5O2↑+8H2O,A、C项正确;a试管中溶液变为红色,说明溶液中含有Fe3+,则燃烧前钠块中含有铁元素,B项正确;由a、b试管中的现象可知,钠的燃烧产物溶于H2SO4溶液后含有Fe3+,不含Fe2+,因为溶液中H2O2具有氧化性,不能判断是否含有Fe3O4,D项错误。
4.A 解析 鉴别纯碱与小苏打,试管口应略向下倾斜,A错误;过氧化钠与水反应放出大量的热,能使脱脂棉燃烧,B正确;氯气与NaOH溶液反应时,锥形瓶中氯气被消耗,压强减小,气球会变大,C正确;点燃酒精灯加热,可对NH4Cl溶液进行蒸发浓缩,熄灭酒精灯,可自然冷却结晶得到NH4Cl晶体,D正确。
5.C 解析 装置①为固体和液体不加热反应制备气体,锌与稀硫酸反应制氢气,氧化钙与浓氨水反应制备氨都可以用装置①,A项正确;金属钠与空气中的氧气、水蒸气等发生反应,因此实验之前,用二氧化碳气体排出装置内的空气,当看到装置⑤中澄清石灰水变浑浊后,空气已排净,再点燃酒精灯,B项正确;反应产生的二氧化碳气体含有氯化氢和水蒸气,因此先用饱和碳酸氢钠溶液除去氯化氢(因为碳酸钠溶液与二氧化碳反应),再用浓硫酸吸收水蒸气,C项错误;根据题给信息可知,PdCl2被CO还原为黑色的Pd,发生反应PdCl2+CO+H2OPd↓+CO2+2HCl,D项正确。
6.D 解析 由实验现象和题给信息可知,实验中酚酞褪色可能是双氧水具有强氧化性将酚酞氧化而漂白褪色,也可能是氢氧化钠溶液浓度过大导致酚酞褪色,所以还必须补充除去过氧化氢或降低氢氧化钠溶液浓度的实验来验证褪色原因。
7.C 解析 图中a→b段加入稀盐酸,不产生气体,则a点溶液含有大量HCO3-,HCO3-可与OH-反应而不能大量共存,A不符合题意;b点为NaHCO3和NaCl的混合液,Al3+与HCO3-发生相互促进的水解反应生成Al(OH)3沉淀和CO2气体,不能大量共存,B不符合题意;c点为NaCl溶液,四种离子不发生反应,可以大量共存,C符合题意;d点为NaCl和HCl的混合液,NO3-、Fe2+和H+发生氧化还原反应,F-和H+结合生成HF,不能大量共存,D不符合题意。
8.D 解析 为了防止空气中的二氧化碳对实验的影响,需先通过装置A吸收空气中的二氧化碳,则装置A中的试剂为NaOH溶液,C中的试剂应能与二氧化碳反应生成沉淀,应为Ba(OH)2溶液,A错误;若B、C之间添加饱和NaHCO3溶液的洗气瓶,挥发出的HCl气体会与NaHCO3反应生成CO2气体,对测定纯碱纯度会有影响,B错误;盐酸易挥发,B中可能有HCl、H2O进入C中,不能通过测定C的质量差来确定CO2的质量,应通过测量C中产生的沉淀质量来确定碳酸钠的质量分数,C错误;沉淀表面可能附着少量水分和可溶于水的杂质,应经过滤、洗涤、干燥、称量等操作测定装置C中沉淀质量,D正确。
9.B 解析 过氧化钠可与稀盐酸中的水反应生成氧气,有气泡冒出,不能证明过氧化钠已经变质,A错误;钠与二氧化碳反应生成碳酸钠和碳,产生黑、白两种固体,该反应为置换反应,B正确;碳酸根离子结合质子能力强于碳酸氢根离子,盐酸少量,碳酸钠与盐酸反应生成碳酸氢钠,无明显现象,不会产生气泡,C错误;向NH4Cl溶液中加入一定量NaOH固体时,因为氢氧化钠固体溶于水放热,所以不能据此说明该反应是放热反应,D错误。
10.答案 (1)aefbcghd 将玻璃塞上的凹槽对准漏斗颈部的小孔
(2)使氨盐水雾化,可增大与二氧化碳的接触面积,从而提高产率(或其他合理答案)
(3)NH3+H2O+NaCl+CO2NH4Cl+NaHCO3↓
(4)冷却结晶 过滤 (5)A
解析 根据工艺流程知,浓氨水中加入氯化钠粉末形成饱和氨盐水后,再通入二氧化碳气体,发生反应:NH3+H2O+NaCl+CO2NH4Cl+NaHCO3↓,得到的碳酸氢钠晶体烘干后受热分解会生成碳酸钠、二氧化碳和水,从而制得纯碱;另一方面得到的母液的主要溶质为NH4Cl,再加入氯化钠粉末,使NH4Cl结晶析出。
(1)可先选用装置A制备二氧化碳,然后通入饱和碳酸氢钠溶液中除去二氧化碳中的HCl,再与饱和氨盐水充分接触来制备NaHCO3,其中过量的二氧化碳可用氢氧化钠溶液吸收,逸出的NH3可用饱和食盐水吸收,所以按气流方向正确的连接顺序应为aefbcghd;为使A中分液漏斗内的稀盐酸顺利滴下,可将分液漏斗上部的玻璃塞打开或将玻璃塞上的凹槽对准漏斗颈部的小孔。
(2)B中使用雾化装置使氨盐水雾化,可增大与二氧化碳的接触面积,从而提高产率。
(4)根据溶解度随温度的变化曲线可以看出,氯化铵的溶解度随着温度的升高而不断增大,而氯化钠的溶解度随着温度的升高变化并不明显,要使NH4Cl充分析出并分离,需采用冷却结晶、过滤、洗涤、干燥的操作。
(5)称量前,若无水Na2CO3保存不当,吸收了一定量水分,用其配制的标准液浓度偏小,所以用其标定盐酸浓度时,消耗的碳酸钠标准溶液的体积会增大,根据c(测)=c(标)V(标)V(测)可知,最终会使结果偏高。
11.答案 (1)2NaHCO3Na2CO3+CO2↑+H2O
(2)①相同温度下,Na2CO3比NaHCO3的溶解度大 ②bd (3)①Ⅰ ②ac
(4)Ca2++CO32-CaCO3↓ Ca2++2HCO3-CaCO3↓+CO2↑+H2O
解析 (1)NaHCO3不稳定,受热易发生分解反应生成Na2CO3、CO2和H2O。
(2)Na2CO3溶于水放出热量,温度升高;Na2CO3溶液显碱性,滴加酚酞后溶液显红色。
(3)①Na2CO3与盐酸的反应分步进行,先转化为NaHCO3,再与盐酸反应生成CO2,故NaHCO3与盐酸反应更剧烈。②由题意可知,n(HCl)=0.01 L×1 ml·L-1=0.01 ml,完全反应消耗Na2CO3和NaHCO3的质量分别为0.01 ml×12×106 g·ml-1=0.53 g、0.01 ml×84 g·ml-1=0.84 g,因此在反应中盐酸均不足,计算生成气体的体积要依据盐酸的量。
(4)操作1中的白色沉淀是碳酸钙,这说明碳酸钠能与氯化钙在溶液中反应生成碳酸钙白色沉淀,反应的离子方程式为Ca2++CO32-CaCO3↓。操作2产生白色沉淀和气体,这说明白色沉淀是CaCO3,气体是CO2,因此在该条件下,NaHCO3溶液与CaCl2溶液反应的离子方程式为Ca2++2HCO3-CaCO3↓+CO2↑+H2O。
选项
方案设计
现象
结论
A
向露置在空气中的Na2O2固体中加入稀盐酸
溶液中产生气泡
Na2O2固体已经变质
B
将一小块金属钠在燃烧匙中点燃,伸入盛有CO2的集气瓶中
产生黑、白两种固体
钠的还原性强,与二氧化碳发生了置换反应
C
向2 mL 2 ml·L-1 Na2CO3溶液中滴加2滴2 ml·L-1稀盐酸
溶液中产生气泡
该Na2CO3溶液中混有NaHCO3杂质
D
向插有温度计的10 mL
0.1 ml·L-1 NH4Cl溶液中加入一定量NaOH固体
有刺激性气味产生,温度计示数增大
反应NH4++OH-
NH3↑+H2O为放热反应
实验方案
预测现象
预测依据
操作1:向2 mL Na2CO3溶液中滴加1 mL 0.5 ml·L-1 CaCl2溶液
有白色
沉淀
Na2CO3溶液中的CO32-浓度较大,能与CaCl2发生反应: (写离子方程式)
操作2:向2 mL NaHCO3溶液中滴加1 mL 0.5 ml·L-1 CaCl2溶液
无白色
沉淀
NaHCO3溶液中的CO32-浓度很小,不能与CaCl2反应
2025届高考化学一轮复习专项练习课时规范练6钠及其重要化合物: 这是一份2025届高考化学一轮复习专项练习课时规范练6钠及其重要化合物,共8页。试卷主要包含了下列有关叙述正确的是,下列叙述正确的是,下列说法中不正确的是等内容,欢迎下载使用。
2025届高考化学一轮复习专项练习课时规范练6钠及其重要化合物: 这是一份2025届高考化学一轮复习专项练习课时规范练6钠及其重要化合物,共7页。试卷主要包含了下列有关叙述正确的是,下列叙述正确的是,下列说法中不正确的是等内容,欢迎下载使用。
适用于新高考新教材广西专版2024届高考化学一轮总复习第三章金属及其化合物课时规范练9铁及其重要化合物: 这是一份适用于新高考新教材广西专版2024届高考化学一轮总复习第三章金属及其化合物课时规范练9铁及其重要化合物,共7页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。












