
26,2024年四川省成都市石室天府中学中考三模化学试题(无答案)
展开
这是一份26,2024年四川省成都市石室天府中学中考三模化学试题(无答案),共7页。试卷主要包含了成都坚持生态优先、绿色发展,下列化学用语表达错误的是等内容,欢迎下载使用。
第Ⅰ卷 (选择题,共42分)
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 C1-35.5 Fe-56 Zn-65 Cu-64 Ag-109
一、选择题(本题包括14个小题,每小题3分,共42分。每小题只有一个选项符合题意)
1.成都有许多国家级、省市级非遗项目。下列非遗项目涉及的变化属于化学变化的是( )
A.画糖画 B.烧制陶瓷 C.编制竹工艺品 D.用针线制作蜀绣
2.成都坚持生态优先、绿色发展。下列举措有误的是( )
A.水更清——防治水体污染 B.土更净——填埋废弃电池
C.天更蓝——加强大气治理 D.景更美——提高绿化覆盖
3.下列选项中物质的俗名、化学式、类别、用途完全对应的是( )
A.纯碱Na2CO3、碱、制玻璃 B.生石灰CaO、氧化物、补钙剂
C.食盐NaCl、盐、除铁锈 D.火碱NaOH、碱、制取肥皂
4.空气中各成分应用广泛,以下用途主要由其物理性质决定的是( )
A.氧气用于气焊、气割 B.食品包装中充氮气防腐
C.稀有气体用于霓虹灯 D二氧化碳用作气体肥料
5.下列实验现象及结论叙述不正确的是( )
A.打开盛有浓盐酸的试剂瓶塞:瓶口冒出白雾
B.向氢氧化钠中滴加酚酞溶液:酚酞溶液由无色变为红色
C.铁锈和足量稀硫酸反应:红褐色固体逐渐减少,放热,溶液由无色变为浅绿色
D.氧化铜与稀盐酸反应:黑色固体逐渐减少,溶液变为蓝色
6.成都水井坊是我国最古老的酿酒遗址。其特色之一是在小麦、高粱中先后拌入糖曲和酒曲,发酵后进行“质量摘酒”——以如图所示的生铁“天锅”把酒头摘出后,边摘边尝,优中选优。下列有关说法错误的是( )
A.通过“质量摘酒”可得到不同酒精浓度的酒
B.酒(C2H5OH)中碳元素的质量分数约为52.2%
C.“天锅”材料属于合金
D.小麦、高粱中均含有淀粉(C6H10O5)n淀粉中各元素质量比为6:10:5
7.下列化学用语表达错误的是( )
A.氮元素:He B.铝表面形成的致密氧化膜:Al2O3
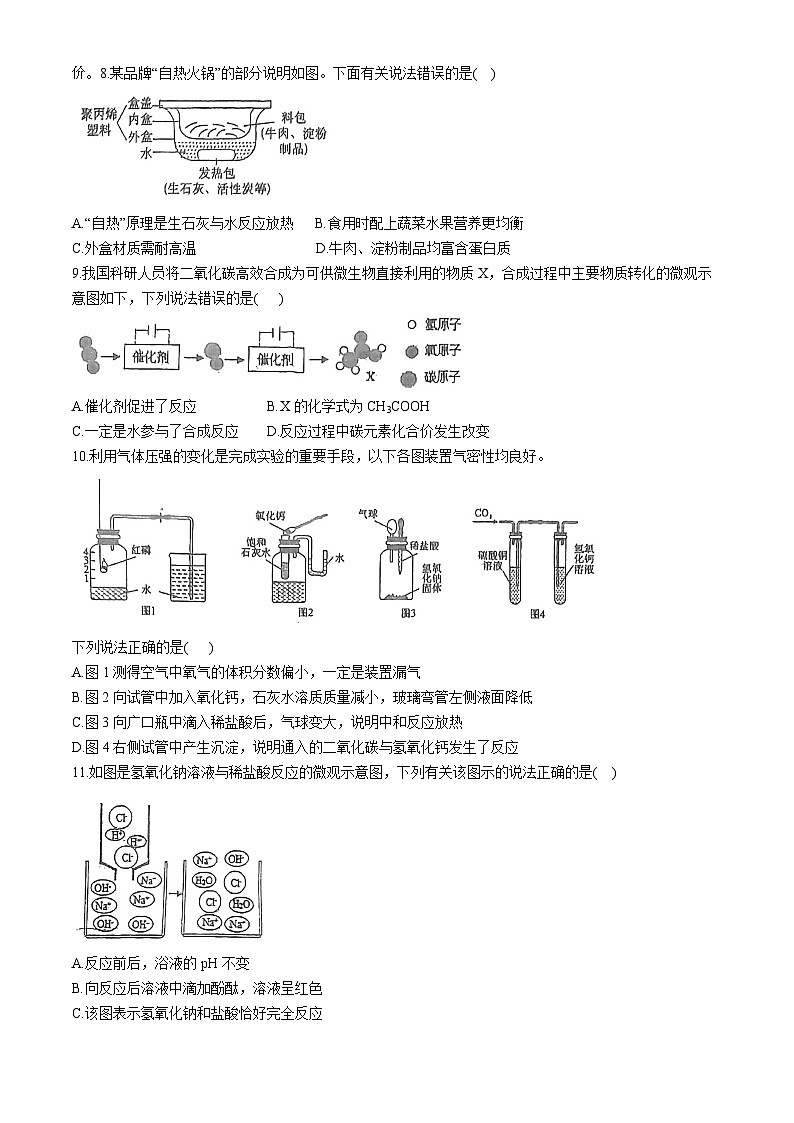
C.2个亚铁离子:2Fe2+ D.2个氮分子:2N试卷源自 试卷上新,即将恢复原价。8.某品牌“自热火锅”的部分说明如图。下面有关说法错误的是( )
A.“自热”原理是生石灰与水反应放热 B.食用时配上蔬菜水果营养更均衡
C.外盒材质需耐高温 D.牛肉、淀粉制品均富含蛋白质
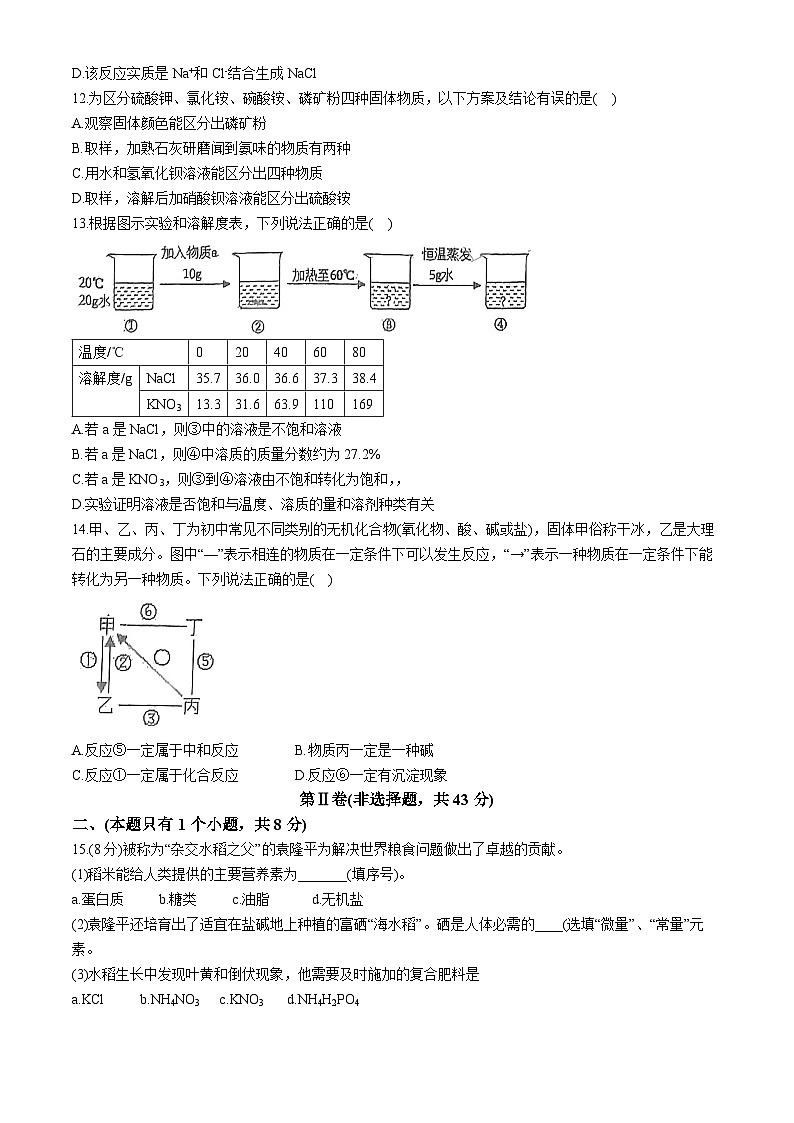
9.我国科研人员将二氧化碳高效合成为可供微生物直接利用的物质X,合成过程中主要物质转化的微观示意图如下,下列说法错误的是( )
A.催化剂促进了反应 B.X的化学式为CH3COOH
C.一定是水参与了合成反应 D.反应过程中碳元素化合价发生改变
10.利用气体压强的变化是完成实验的重要手段,以下各图装置气密性均良好。
下列说法正确的是( )
A.图1测得空气中氧气的体积分数偏小,一定是装置漏气
B.图2向试管中加入氧化钙,石灰水溶质质量减小,玻璃弯管左侧液面降低
C.图3向广口瓶中滴入稀盐酸后,气球变大,说明中和反应放热
D.图4右侧试管中产生沉淀,说明通入的二氧化碳与氢氧化钙发生了反应
11.如图是氢氧化钠溶液与稀盐酸反应的微观示意图,下列有关该图示的说法正确的是( )
A.反应前后,浴液的pH不变
B.向反应后溶液中滴加酚酞,溶液呈红色
C.该图表示氢氧化钠和盐酸恰好完全反应
D.该反应实质是Na+和Cl-结合生成NaCl
12.为区分硫酸钾、氯化铵、碗酸铵、磷矿粉四种固体物质,以下方案及结论有误的是( )
A.观察固体颜色能区分出磷矿粉
B.取样,加熟石灰研磨闻到氨味的物质有两种
C.用水和氢氧化钡溶液能区分出四种物质
D.取样,溶解后加硝酸钡溶液能区分出硫酸铵
13.根据图示实验和溶解度表,下列说法正确的是( )
A.若a是NaCl,则③中的溶液是不饱和溶液
B.若a是NaCl,则④中溶质的质量分数约为27.2%
C.若a是KNO3,则③到④溶液由不饱和转化为饱和,,
D.实验证明溶液是否饱和与温度、溶质的量和溶剂种类有关
14.甲、乙、丙、丁为初中常见不同类别的无机化合物(氧化物、酸、碱或盐),固体甲俗称干冰,乙是大理石的主要成分。图中“—”表示相连的物质在一定条件下可以发生反应,“→”表示一种物质在一定条件下能转化为另一种物质。下列说法正确的是( )
A.反应⑤一定属于中和反应 B.物质丙一定是一种碱
C.反应①一定属于化合反应 D.反应⑥一定有沉淀现象
第Ⅱ卷(非选择题,共43分)
二、(本题只有1个小题,共8分)
15.(8分)被称为“杂交水稻之父”的袁隆平为解决世界粮食问题做出了卓越的贡献。
(1)稻米能给人类提供的主要营养素为_______(填序号)。
a.蛋白质 b.糖类 c.油脂 d.无机盐
(2)袁隆平还培育出了适宜在盐碱地上种植的富硒“海水稻”。硒是人体必需的____(选填“微量”、“常量”元素。
(3)水稻生长中发现叶黄和倒伏现象,他需要及时施加的复合肥料是
a.KCl b.NH4NO3 c.KNO3 d.NH4H2PO4
(4)化肥对粮食的增产有重要作用,氮肥生产往往要先制取氨气,如图是在密闭容器中反应制氨的微观示意图,写出该反应的化学方程式____________。
(5)米饭蒸煮中能闻到浓郁的米香味,原因是________(用微粒的观点解释)。保存运输大米的真空包装袋其主要成分有聚乙烯塑料,该塑料属于_____材料,该包裝袋随意丢弃会带来的环境问题是_________(答案合理即可)。
三、(本题只有1个小题,共10分)
16.(10分)如图所示是工业上炼铁高炉:
(1)高炉中“CO2→CO”的反应主要发生在_______区域(填字母)。
(2)取小最高炉中炼出的生铁放入烧杯中,加入足量稀盐酸,发生反应的化学方程式为________,能观察到的现象是____________。
(3)炼铁厂用含氧化铁480吨的赤铁矿为原料炼铁,求得到单质铁的质量。(请写出计算过程)
四、(本题包括2个小题,共15分)
17.(8分)化学实验是科学探究的重要途径。
(1)下列说法不正确的是___________。
A.点燃可燃性气体前要检验纯度
B.稀释浓碗酸把水沿烧杯内壁慢慢注入浓硫酸中,并用玻璃棒不断搅拌
C.密封在塑料袋里的少量干冰在室温下塑料袋很快鼓起,说明温度升高分子体积变大
D.白磷通常保存在水里
(2)探究小组的同学设计如图1所示的微型实验装置来探究二氧化碳的制法和性质。
①A装置可以控制制取气体时的发生与停止,请简述反应物需要满足的条件为_________。
②打开弹簧夹,将加液器的盐酸推入制气管。当图A制气管中的盐酸消耗完,反应停止一段时间后,可观察到的现象是___________。
③用A制取的CO2含有杂质,要得到较纯净的CO2,可将制气管与B、C、D相连,仪器接口连接顺序是:从A中导出的气体→__→___→____→_____→i。请把D装置导管补画完整。
(3)向盛有一定量的硝酸银、硝酸铝和硝酸铜混合溶液的烧杯中加入足量的锌粉,所得溶液的质量与反应时间的关系如图2,请回答下列问题。
①写出a点时发生反应的化学方程式_____________。
②b点时烧杯底部的金属固体有:______________。
18.(7分)CO2的捕集与资源化利用是化学研究的热点。
(1)我国科学家李灿院士团队突破了太阳能电解水和CO2加氢制甲醇(CH3OH)的关键技术(液态太阳燃料技术),技术路线如图所示。
①氢能存储/CO2加氢(個化剂,ZnO-ZrO2、压卿50Mpa、温度,315~320℃)路成发生的反应化学方程式_______________。
②图1中可循环使用的物质有_______________。
(2)捕集燃煤电子厂烟气
【资料卡片】a.MEA水溶液低温可吸收CO2,升高温度可解吸CO2。
b.恒温流化床反应器出口温度高。
①“吸收塔”中电厂烟气从塔底通入,MEA水溶波从塔项喷淋。这样操作的优点是______________;“解吸塔”实现CO2解吸的操作是_____________。
②“设备A”可实现CH4和H2O分离,方法是_____________。
③CO2甲烷化的反应中,=___________。
五、(本题只有1个小题,共10分)
19.(10分)不少家庭养观赏鱼,有时会在鱼缸里放点“鱼浮灵”,可使水中的含氧量迅速增加。请你和小欣同学一起完成这项探究活动。
【查阅资料】过碳酸钠,白色结晶颗粒,易溶于水并迅速放出氧气。
【猜想假设】“鱼浮灵”的主要成分是过碳酸钠。
【性质探究】
【结果分析】
(3)上述实验中二氧化锰起__________作用。
(4)“鱼浮灵”主要成分是过碳酸钠,根据化学反应方程式:X+H2O=Na2CO3+H2O2,推出过碳酸钠的化学式X为_________。
【工业制备】(如图)
注:异丙醇为有机溶剂。
(5)稳定剂的作用是防止H2O2分解(或防止过碳酸钠分解),稳定剂中MgCl2和Na2SiO3发生复分解反应,生成一种难溶物将过碳酸钠粒子包裹住,该反应的化学方程式为______________。
【测定纯度】
实验资料:过碳酸钠样品中的杂质不溶于水且不与水反应。
实验原理:
2X+4HCl=4NaCl+2CO2↑+O2↑+2H2O
实验装置:
【交流与讨论】
Ⅰ.甲同学认为测定产物中O2的体积即可测定样品(含有的杂质不溶于水且不与酸反应)的纯度(样品中过碳酸钠的,质量分数)。
(6)装置②的作用是_____________。
(7)装置③的作用是_____________。
(8)Ⅱ.乙同学认为测定产物中CO2的质量(即反应前后装置②的质量差)就可测定样品的纯度。但利用上述实验装置测得CO2的质量并计算样品的纯度,结果会偏高,你认为原因可能是________(填序号)。
A.浓盐酸易挥发,产生的氯化氢气体被装置②吸收
B.二氧化碳气体逸出时带出的水蒸气在装置②中冷凝而被吸收
C.装置①、②内空气中的二氧化碳被装置②吸收
(9) Ⅲ.丙同学提出了一种新方案,得到了大家的一致认可:称取样品12.5g,滴加足量浓盐酸至样品反应完全,再将烧瓶中所有的液体蒸发、结晶、烘干,称得氯化钠固体11.7g,则该样品的纯度为__________。温度/℃
0
20
40
60
80
溶解度/g
NaCl
35.7
36.0
36.6
37.3
38.4
KNO3
13.3
31.6
63.9
110
169
实验
主要操作步骤(见上图)
主要实验现象
结论
(1)
在集气瓶中加入少量二氧化锰,在仪器a中加入新配制的“鱼浮灵”的饱和水溶液;打开仪器a的活塞,放出适量溶液后,在导管口放一根带火星的木条
__________
“鱼浮灵”溶于水生成过氧化氢
(2)
关闭仪器a,在仪器b中加入_______,打开活塞,放出适量溶液后,在导管口放一燃着的木条
生成大量无色气泡,木条熄灭
“鱼浮灵”溶于水生成碳酸钠
相关试卷
这是一份2024年四川省成都市石室天府中学中考三模化学试题,共6页。
这是一份09,2024年四川省成都市石室中学中考模拟诊断抽样化学试题(1),共6页。
这是一份26,2024年湖南省A佳新中考联考一模化学试题,共11页。试卷主要包含了选择题的作答,非选择题的作答,考试结束后,将答题卡上交等内容,欢迎下载使用。









