





初中化学鲁教版九年级下册第二节 金属的化学性质课堂教学课件ppt
展开
这是一份初中化学鲁教版九年级下册第二节 金属的化学性质课堂教学课件ppt,文件包含第九单元第二节第2课时pptx、铁跟硫酸铜溶液的反应wmv、铝与氯化铜溶液铜与硝酸银溶液的反应flv等3份课件配套教学资源,其中PPT共53页, 欢迎下载使用。
金属与盐溶液的反应金属活动性顺序及应用设计实验证明金属活动性顺序
思考:为什么不同的金属与酸反应的剧烈程度不同?
【回顾思考】铁钉与硫酸铜溶液反应的现象及反应方程式【视频播放】铁跟硫酸铜溶液的反应
金属与金属化合物溶液的反应
铁钉表面有红色物质生成,蓝色溶液变成浅绿色Fe+CuSO4 FeSO4+Cu
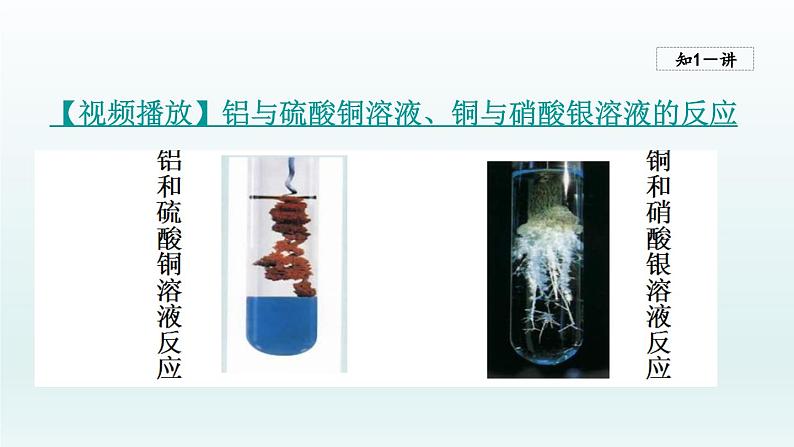
【视频播放】铝与硫酸铜溶液、铜与硝酸银溶液的反应
铝丝浸入硫酸铜溶液中现象:铝丝表面出现红色固体化学方程式:2Al+3CuSO4 Al2(SO4)3+3Cu
铜丝浸入硝酸银溶液中现象:铜丝表面出现银白色固体化学方程式:Cu+2AgNO3 Cu(NO3)2+2Ag铜丝浸入硫酸铝溶液中:无现象
金属+金属化合物 新金属+新金属化合物1. 以上反应类型都属于 反应。2. 铝、铜、银三种金属的活动性顺序是__________。
【中考•山西】在学习金属的化学性质时,老师给大家演示了如图所示的实验,下列说法正确的是( )A.铜片表面始终没有明显变化B.一段时间后溶液由无色变为浅绿色C.反应后溶液中一定有硝酸铜,可能有硝酸银D.通过实验现象推测银和硫酸铜溶液也可以反应
导引:铜片与硝酸银反应,可观察到:铜片的表面覆盖一层银白色固体,溶液逐渐变成蓝色;反应后的溶液中一定有生成的硝酸铜,还可能有过量的硝酸银;根据实验现象可知银与硫酸铜溶液不反应。
1.(1)将铁钉放入硝酸银溶液中,过一段时间后可观察到的现象有_________________________________ ,发生反应的化学方程式为 。
铁钉表面覆盖一层银白色固体,溶液变成浅绿色
Fe+2AgNO3===Fe(NO3)2+2Ag
(2)将铁丝放入ZnSO4溶液中,过一段时间后,可观察到______________。(3)上述两个反应所属的基本反应类型是___________。
2.【中考•广州】将铜丝插入下列溶液中,有明显现象的是( )A.HCl溶液 B.AgNO3溶液C.MgSO4溶液 D.FeSO4溶液
3.【中考·新疆】如图是探究铁和铜金属活动性的实验,关于此实验说法错误的是( )A.铁丝需要砂纸打磨B.溶液由蓝色变为无色C.金属活动性强弱:Fe>CuD.化学反应方程式为:Fe+CuSO4===Cu+FeSO4
对金属活动性顺序的理解(1)在金属活动性顺序里,金属的位置越靠前,它的活 动性就越强。
(2)在金属活动性顺序里,排在氢前面的金属能与盐酸、稀硫酸反应放出氢气,而排在氢后面的金属不能与盐酸、稀硫酸反应放出氢气。(3)在金属活动性顺序里,位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来。
废旧手机的某些部件含有 Mg、Al、Cu、Ag、Pb、Pt 等金属,为了回收贵重金属,把旧手机部件浸入足量稀硫酸中充分反应,过滤,所得固体中含有的金属是( ) A. Mg、Al、Pb B. Cu、Ag、PtC. Mg、Cu、Pb D. Cu、Pb、Pt
导引:金属活动性顺序中,只有氢前金属如 K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb 能与酸反应产生氢气,氢后金属与酸不反应。Mg、Al、Pb 能与稀硫酸充分反应而溶解,Cu、Ag、Pt 在金属活动性顺序中位于氢后,不能与稀硫酸反应。
4.【中考·苏州】下列金属活动性由强至弱的顺序及元素名称、符号均正确的一组是( )A.钾K>钙Ca>钠Na>镁MgB.铝Al>锌Zn>铁Fe>锡XiC.铅Pb>铜Cu>贡HgD.金Au>银Ag>铂pt
5.【中考·德州】金属锰与氯化亚铁溶液可发生如下反应:Mn+FeCl2===MnCl2+Fe,下列说法错误的是( )A.该反应属于置换反应B.锰的金属活动性比铁强C.锰能置换出盐酸中的氢D.反应前后元素化合价都不变
6.初中化学课学完以后,化学学习兴趣小组对 “金属活动性顺序”从内容、规律以及应用等方面进行了总结。请你认真填写下面的空白内容:(1)金属活动性顺序:K、Ca、Na、____、Al、Zn、 Fe、Sn、Pb、(H)、Cu、_______、Ag、Pt、Au。
(2)金属与酸反应的规律是____________________________________________________________。试举出实际应用的实例__________________________________________(可用化学方程式表示)。
在金属活动性顺序里,只有排在氢前面的金属才能置换出酸中的氢
Fe+2HCl====FeCl2+H2↑(合理即可)
(3)金属与金属化合物发生置换反应,必须符合两点:①________________________________________________________________,但K、Ca、Na三种金属非常活泼,不能把金属直接从其化合物溶液中置换出来;②__________________________。
在金属活动性顺序里,金属必须排在金属化合物中相应金属的前面
金属化合物必须是可溶性的
试举出实际应用的实例_______________________________________(可用化学方程式表示)。(4)铁与稀盐酸、稀硫酸、氯化铜溶液发生置换反应时,生成的化合物分别为________、________和________。
Fe+CuSO4====FeSO4
如何设计实验验证金属的活动性顺序?
设计实验证明金属活动性顺序
1.设计原理:根据金属与酸能否反应或反应的剧烈程度或根据金属能否把另一金属从其盐溶液里置换出来等方法,设计探究实验。
2.设计方法:(1)验证两种金属的活动性顺序时,可以将一种金属放在另一种金属的可溶性盐溶液中,观察能否将另一金属置换出来或根据与酸能否反应及反应的剧烈程度来判断。
(2)比较三种金属活动性的实验设计。①方法一:“两金夹一盐”。即选用三种金属活动性最强和最弱的两种金属的单质及活动性介于两种金属之间的金属的盐溶液作为试剂,根据两种金属单质分别与盐溶液反应的情况进行判断。
②方法二:“两盐夹一金”。即选用三种金属中活动性排在中间的金属单质及其他两种金属的盐溶液作为试剂,根据金属单质分别与两种盐溶液反应的情况判断。
[中考·自贡] 现有X、Y 两种金属,如果把X、Y 分别放入稀盐酸中,X 溶解并产生氢气,Y 不反应;如果把Y 放入硝酸铜溶液中,无明显现象,则X、Y、Cu 的金属活动性强弱顺序是( )A. Cu > X > Y B. X > Cu > YC. X > Y > Cu D. Y > X > Cu
解题秘方:根据金属与酸、金属与盐溶液反应的条件来推断金属活动性强弱。解:把X、Y 两种金属分别放入稀盐酸中,X 溶解并产生氢气,Y 不反应,说明活动性X > H > Y;把Y 放入硝酸铜溶液中,无明显现象,说明Y 的金属活动性比铜弱,即活动性铜> Y,则X、Y、Cu 的金属活动性强弱顺序是X > Cu > Y。
[中考·海南] 为验证Zn、Cu 和Ag 三种金属的活动性顺序,设计的下列实验方案能达到目的的是( )A. 将Zn、Cu 分别加入AgNO3 溶液中B. 将Zn、Cu 和Ag 分别加入稀盐酸中C. 将Zn、Ag 分别加入CuSO4 溶液中D. 将Zn 分别加入CuSO4、AgNO3 溶液中
解题秘方:解答本题可采用金属与盐溶液反应的“中间原则”。解:将Zn、Cu 分别加入AgNO3 溶液中,均能与硝酸银溶液反应,说明活动性锌>银,铜>银,但无法确定锌和铜的活动性强弱,A 错误;将Zn、Cu 和Ag 分别加入稀盐酸中,锌能与稀盐酸反应生成氢气,Cu、Ag 不能与稀盐酸反应,故无法确定银和铜的活动性强弱,B 错误;
将Zn、Ag 分别加入CuSO4 溶液中,Ag 与CuSO4 溶液不反应,说明活动性铜>银;锌与CuSO4 溶液反应置换出铜,说明活动性锌>铜,由此可得出三种金属活动性锌>铜>银,C 正确;将Zn 分别加入CuSO4、AgNO3 溶液中,均能反应,说明活动性锌>铜、锌>银,但无法确定银和铜的活动性强弱。
[中考·威海] 下列事实能用金属活动性解释的是( )①铝制品比铁制品耐腐蚀②用硫酸铜溶液和铁制取铜③用稀盐酸除铁锈④金属铜不能与稀硫酸反应A. ①② B. ①②③ C. ②④ D. ①②④
解题秘方:解答这类题目时,首先要熟记和理解金属活动性顺序及其应用,以及与之相关的知识等,理解其应用原则,学会处理实际问题。解:①铝制品比铁制品耐腐蚀,是因为铝易与氧气反应生成一层致密的氧化铝薄膜,阻止内部的铝被氧化,不能说明铁的活动性比铝强,不能用金属活动性解释;
②用硫酸铜溶液和铁制取铜,是因为铁比铜活泼,铁能将铜置换出来,能用金属活动性解释;③用稀盐酸除铁锈,是酸与金属氧化物反应,不能用金属活动性解释;④金属铜不能与稀硫酸反应,是由于在金属活动性顺序中铜位于氢的后面,能用金属活动性解释。故C 正确。
7.【中考•西宁】有甲、乙、丙、丁四种颗粒大小相同的金属,分别投入等质量、等浓度的稀硫酸中,乙、丙表面有气泡产生,且丙产生气泡较快,甲、丁无现象;再将甲投入丁的化合物溶液中,甲的表面有丁析出,则这四种金属的活动性由强到弱的顺序为( )A.甲>乙>丙>丁 B.丙>乙>甲>丁C.丙>乙>丁>甲 D.丁>甲>乙>丙
8.【中考•临沂】下列四个实验中只需要完成三个就可以证明Zn、Cu、Ag三种金属的活动性顺序,其中不必进行的实验是( )A.将锌片放入稀硫酸中B.将铜片放入稀硫酸中C.将铜片放入硝酸银溶液中D.将锌片放入硝酸银溶液中
一、金属与金属化合物溶液反应2Al+3CuSO4=3Cu+Al2(SO4)3 Cu+2AgNO3=2Ag+Cu(NO3)2Cu和Al2(SO4)3不反应结论:金属活动性Al>Cu>Ag
二、金属活动性顺序的应用1. 金属的位置越靠前,它的活动性越强。2. 位于氢前的金属能置换出盐酸和稀硫酸中的氢。3. 位于前面的金属能把位于后面的金属从它们的盐溶液中置换出来(除K、Ca、Na外)。
三、探究金属活动性常用的两种方法1. 利用金属和金属盐溶液反应探究(验证Zn、Ag、Cu三种金属活动性)。(1)“中间的金属,两端的溶液”的方法(Cu丝、ZnCl2溶液、AgNO3溶液)。
(2)“中间的溶液,两端的金属”的方法(Zn片、Ag片、CuSO4溶液)。2. 利用金属和酸反应探究(验证Mg、Zn、Cu、Ag的活动性)。
1.【中考•温州】根据金属活动性判断下列容器与所盛溶液不会发生化学反应的是( )A.用铁制容器盛盐酸B.用铜制容器盛盐酸C.用铁制容器盛硝酸银溶液D.用铜制容器盛硝酸银溶液
2.波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、生石灰加水配置而成。为什么不能用铁制容器来配置波尔多液?
若用铁制容器配制波尔多液,会发生化学反应:Fe+CuSO4====FeSO4+Cu,既损坏了容器,又降低了波尔多液的药效。
3.写出镁、铜、氧气、盐酸两两间能发生反应的化学方程式,并注明反应类型。
4.下列物质能否发生反应?写出能发生反应的化学方程式。(1 )银与稀盐酸 (2)锌与硫酸铜溶液(3 )铜与硫酸锌溶液(4)铝与硝酸银溶液
(1)不反应。(2)Zn+CuSO4 ==== ZnSO4+Cu。(3)不反应。(4)Al+3AgNO3 ==== Al(NO3)3+3Ag。
5. 填写下列表格(“混合物”栏中括号内为杂质)。
Fe+2HCl === FeCl2+H2↑
加盐酸至无气泡产生,过滤,洗涤,干燥
Fe+CuCl2 === FeCl2+Cu
加过量无锈铁钉或铁粉,充分反应后过滤
6. 现有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产生氢气, Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Y表面有银析出, 而Z没有变化。根据以上实验事实,判断X、Y和Z的金属活动性顺序。
相关课件
这是一份初中鲁教版第二节 金属的化学性质教学演示ppt课件,文件包含第二节金属的化学性质第2课时1pptx、金属与盐的反应wmv、铁跟硫酸铜溶液的反应wmv等3份课件配套教学资源,其中PPT共20页, 欢迎下载使用。
这是一份初中化学鲁教版九年级下册第二节 金属的化学性质课堂教学课件ppt,文件包含第二节金属的化学性质第1课时1pptx、金属与酸的反应mp4、铁的燃烧mp4、铜跟氧气反应mp4、镁条燃烧mp4等5份课件配套教学资源,其中PPT共23页, 欢迎下载使用。
这是一份初中化学鲁教版九年级下册第二节 金属的化学性质课前预习ppt课件,共33页。PPT课件主要包含了交流共享,慧眼识金,小试牛刀,化学反应的基本类型,你知道吗,我也会,砸蛋做题,你选择的是第二题,学完本课题你应该知道等内容,欢迎下载使用。









