

湖北省黄冈中学2024届高三下学期第二次模拟考试化学试卷(含答案)
展开
这是一份湖北省黄冈中学2024届高三下学期第二次模拟考试化学试卷(含答案),共20页。试卷主要包含了单选题,实验题,填空题等内容,欢迎下载使用。
一、单选题
1.化学与生产、生活、科技密切相关。下列说法正确的是( )
A.北斗卫星导航系统所用计算机芯片的主要材料是二氧化硅
B.乡村公路铺设的沥青属于天然无机材料
C.可用于丝织品漂白是由于其能氧化丝织品中有色成分
D.铜官窑彩瓷是以黏土为主要原料经高温烧结而成
2.下列关于准晶的说法正确的是( )
A.准晶和晶体可以通过射线衍射实验加以区别
B.准晶具有良好的导电、导热性
C.自然界中不存在天然条件下形成的准晶
D.已知的准晶中都含有共价键
3.黑火药配方“一硫二硝三木炭”的爆炸反应为:。设为阿伏加德罗常数的值,下列说法正确的是( )
A.溶液中含数目小于
B.含键数目为
C.每生成转移电子数目为
D.晶体中含离子数目为
4.科学研究发现新型含碳化合物和,它们的结构类似,均为直线形分子。下列结论中错误的是( )
A.和分子中碳原子的杂化方式均为
B.是非极性分子,和也是非极性分子
C.、分子全部由双键构成
D.、分子中所有原子最外层均满足8电子稳定结构
5.锂电池寿命结束时,其处理和回收将成为十分棘手的问题。锂电回收主要针对正极中的钴和镍。关于和,下列说法正确的是( )
A.和都是区的元素
B.和核外未成对电子数之比为
C.的空间构型是平面正方形,中键数目是
D.由熔点可知,晶体是分子晶体
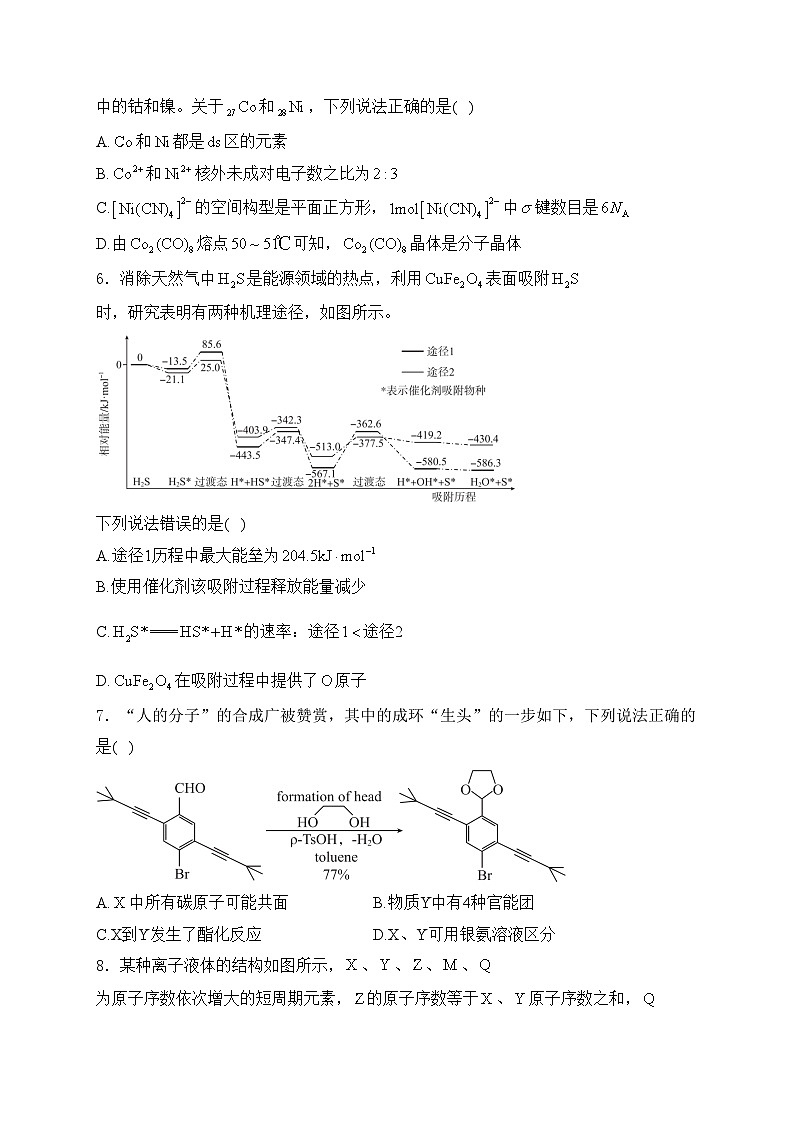
6.消除天然气中是能源领域的热点,利用表面吸附时,研究表明有两种机理途径,如图所示。
下列说法错误的是( )
A.途径1历程中最大能垒为
B.使用催化剂该吸附过程释放能量减少
C.的速率:途径途径2
D.在吸附过程中提供了原子
7.“人的分子”的合成广被赞赏,其中的成环“生头”的一步如下,下列说法正确的是( )
A.中所有碳原子可能共面B.物质Y中有4种官能团
C.X到Y发生了酯化反应D.X、Y可用银氨溶液区分
8.某种离子液体的结构如图所示,、、、、为原子序数依次增大的短周期元素,的原子序数等于、原子序数之和,为非金属性最强的元素。下列说法正确的是( )
A.分子的极性:
B.分子的VSEPR模型为三角锥形
C.在同族元素形成的单质中键能最大
D.五种元素的基态原子中,的未成对电子最多
9.下列离子方程式错误的是( )
A.去除废水中的
B.补铁剂中滴加溶液:
C.向次氯酸钙溶液通入足量二氧化碳:
D.加入热水中:
10.中科院研制出了双碳双离子电池,以石墨和中间相炭微粒球为电极,电解质溶液为含有的有机溶液,其充电示意图如下。下列说法错误的是( )
A.固态时为离子晶体
B.充电时MCMB电极为阴极,放电时为负极
C.充电时,若阳极增重,则阴极增重
D.充电时,阳极发生反应为
11.下列有关实验操作、现象(或数据)和结论均正确的是( )
A.AB.BC.CD.D
12.铝电解厂烟气净化的一种简单流程如下:
下列说法正确的是( )
A.陶瓷耐高温,可作吸收塔内衬材料
B.工业采用电解冰晶石制备金属铝
C.合成槽中产物主要有和
D.采用溶液喷淋法可提高烟气吸收效率
13.中国科学院理化所发现利用可使PLA()转化为丙酮酸()的速率显著提高,并且优异的稳定性确保了可以维持的反应性能,其反应机理如图所示,在光照条件下产生带正电空穴(用表示,可捕获电子)和电子。下列说法错误的是( )
A.可作乳酸制备丙酮酸的催化剂,降低反应活化能
B.光照为该反应提供能量,增大光的强度有利于加快反应速率
C.丙酮酸的酸性比丙酸强
D.当PLA完全转化成丙酮酸时,理论上中至少产生
14.钾、铁、硒可以形成一种超导材料,其晶胞在、和平面投影分别如图所示:
下列说法错误的是( )
A.该超导材料的最简化学式为
B.原子的配位数为3
C.该晶胞参数、,则该晶体的密度为
D.Se为第四周期第ⅥA族元素,位于周期表区
15.电位滴定法是根据滴定过程中指示电极电位的变化来确定滴定终点的一种滴定分析方法。常温下,的电离常数,利用盐酸滴定某溶液中的含量,其电位滴定曲线与曲线如图所示。下列说法正确的是( )
(注:—表示电极电位曲线;---表示曲线)
A.水的电离程度:
B.该滴定过程需要加入酸碱指示剂
C.点溶液中
D.点溶液中存在:
二、实验题
16.磺酰胺易溶于醇,溶于热水,不溶于冷水,在酸性、中性、碱性水溶液中性质稳定,主要用于制造医药、农药、染料等。制备磺酰胺的装置如下,其原理为:
。已知:磺酰氯熔点为,沸点为,遇潮湿空气会水解产生酸雾。
Ⅰ.磺酰胺的制备
(1)试剂的名称为______。
(2)装置B中盛放的试剂为______(填字母)。
a.碱石灰b.浓硫酸c.d.无水
(3)写出水解的化学方程式:______。
(4)装置C中多孔球泡的作用是______。
Ⅱ.用如下装置测定产品的含量(假设只含杂质,部分装置已省略)
(5)蒸氨:取a样品进行测定。添加药品后,加热仪器,蒸出的通入含有标准溶液的锥形瓶中。仪器的名称为______,单向阀的作用是______。
(6)滴定:将液封装置2中的水放入锥形瓶中,再将锥形瓶中的溶液倒入容量瓶中配制成的溶液,取溶液用的标准溶液滴定过量的,共消耗标准溶液,产品中的含量是______(列出计算式)。
三、填空题
17.钛白粉是一种重要的工业原料,可作白色颜料和增白剂。一种以钛铁矿(主要成分是,含有少量的等杂质)为原料生产制备的工艺流程如下:
回答下列问题:
(1)基态的核外价层电子排布式为___________。
(2)“酸浸”是用硫酸在加热下“溶煮”钛铁矿,“滤液1”中的存在形式为,则“酸浸”中发生反应的离子方程式为__________。由图可知,当浸出率为70%时,所采用的实验条件为__________。
(3)绿矾是,则“还原”加入过量铁粉的目的是__________。
(4)“水解”过程中适当稀释并加热的目的是__________。
(5)钛是一种性能非常优越的金属.工业上可利用与反应制备金属钛。下列金属冶炼方法与冶炼的方法相似的是__________。(填标号)
A.高炉炼铁
B.电解熔融制钠
C.铝热反应制锰
D.分解制银
(6)转化为有以下两种方法.在时反应的热化学方程式如下:
①
②
请分析方法②加入的目的可能是______________________。
18.为生产医药布洛芬的原料之一,其合成路线如下:
回答下列问题:
(1)中官能团名称:______。
(2)的反应类型为:______。
(3)的手性碳原子有______个。
(4)B的同分异构中满足下列条件的有______种。
a.含有两个b.可发生银镜反应c.苯环上有三个取代基
其中核磁共振氢谱有五组峰,峰面积之比为的结构简式为______。
(5)设计由制备的合成路线(依据题中流程分析)。______。
19.苯乙烯作为一种重要的基础有机化工原料,广泛用于合成塑料和橡胶。工业常采用乙苯脱氢的方法制备苯乙烯,其原理如下:
反应Ⅰ:
(1)近期有科技工作者结合是实验与计算机模拟结果,研究了乙苯在催化剂表面脱氢制苯乙烯的反应,其历程如下图所示(吸附在催化剂表面的物种用标注):
①______(计算结果保留整数)。
②依据上述反应历程,推测乙苯脱氢反应产生的副产物可能是______(填结构简式)
(2)在下,乙苯直接脱氢反应的和随温度的变化如图所示。
①直接脱氢反应在常温下______(选填“能”或“不能”)自发。
②随温度的变化曲线为______(选填“a”或“b”)。
(3)在某温度、下,向反应器中充入气态乙苯和发生反应Ⅰ,其平衡转化率为,则乙苯脱氢反应的压强平衡常数______(计算时忽略副反应)。
(4)工业上还可以利用氧化乙苯制乙烯,其原理为:
反应Ⅱ:
①在相同反应条件下,工业上可采用替代水蒸气进行乙苯脱氢反应,已知;则代替水蒸气参与反应的优点有______。
A.降低反应的能耗B.乙苯转化率更高
C.提高了反应速率D.提高了产物选择性
(5)苯乙烯被酸性高锰酸钾溶液充分氧化后的产物是______和______(填名称)。
参考答案
1.答案:D
解析:A.计算机芯片的主要成分为Si,光导纤维的主要成分是,成分不相同,故A错误;
B.沥青是由不同分子量的碳氢化合物及其非金属衍生物组成的黑褐色复杂混合物,属于有机材料故B错误;
C.可用于丝织品漂白是由于其能和丝织品中的有色成分结合成无色物质,故C错误;
D.陶瓷是以黏土为主要原料,经高温烧结而成故D正确。
2.答案:A
解析:A.晶体具有自范性,而准晶不具有自范性,可以通过X射线行射实验加以区别,A项正确;
B.准晶具有各向异性,不具有良好的导电、导热性,B项错误;
C.自然界中存在天然条件下形成的准晶,如,C项错误;
D.已知的准晶中不一定含有共价键,如中没有共价键,D项错误。
故选A。
3.答案:A
解析:A.因为水解使溶液中的数目小于,A项正确;
B.分子含有2个键,题中没有说是标况条件下,气体摩尔体积未知,无法计算键个数,B项错误;
C.的物质的量,生成转移的电子数为,则转移的电子数为,C项错误;
D.晶体含有离子为,不存在,D项错误。
4.答案:B
解析:
A.结构式为,结构式为,价层电子对数为2且无孤电子对,杂化方式均为杂化,故A正确;
B.正负电荷中心重合,为非极性分子,COS结构式为,结构不对称,正负电荷中心不重合,为极性分子,结构式为,正负电荷中心重合,为非极性分子,故B错误;
C.结构式为,结构式为,两种分子全部由双键构成,故C正确:
D.结构式为,结构式为,碳原子和氧原子最外层都满足8电子稳定结构,故D正确。
5.答案:D
解析:A. 和Ni均为第VIII族元素,都是d区的元素,故A错误;
B.的价电子排布式为的价电子排布式为,故和核外未成对电子数之比为3:2,故B错误;
C.中与4个形成4根配位键,中含有1个键,故中键数目是,故C错误;
D. 熔点为,熔点较低,则可知晶体是分子晶体,故D正确。
6.答案:B
解析:
A.由图示可知,途径1历程中最大能垒为故A正确;
B.催化剂只能改变化学反应速率,不能影响吸附过程中释放的能量,故B错误;
C.活化能越大、反应速率越小,则的速率:途径1
相关试卷
这是一份2024届湖北省黄冈中学高三下学期5月第二次模拟考试化学试卷及答案,共1页。
这是一份2024届湖北省黄冈中学高三下学期5月第二次模拟考试化学试卷及答案 (1),共10页。
这是一份湖北省黄冈中学2023届高三下学期5月第二次模拟考试化学试卷(含答案),共22页。试卷主要包含了单选题,实验题,填空题,推断题等内容,欢迎下载使用。









