






初中化学科粤版九年级上册3.2 制取氧气说课ppt课件
展开上节课我们学习了加热高锰酸钾制取氧气,实验室还常用分解过氧化氢的方法制取氧气。
【实验3-5】用浓度为10%的过氧化氢溶液和二氧化锰完成下列实验。
(2)取少量二氧化锰装入另一试管中,将带火星的木条伸进试管内,结果怎样?
(1)用量筒量取4mL过氧化氢溶液加入试管中,将带火星的木条伸进试管内,结果怎样?
(3)再取少量二氧化锰于第三支试管中,再量取4mL过氧化氢溶液加入,将带火星的木条伸进试管内,有什么现象发生?
(4)待实验(3)的试管内的液体不再放出气泡时,重新加入4mL过氧化氢溶液,再将带火星的木条伸进试管内,又有什么现象发生?
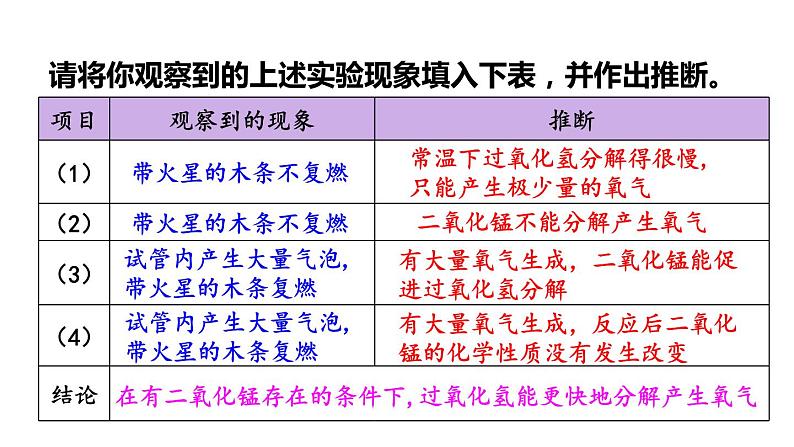
请将你观察到的上述实验现象填入下表,并作出推断。
常温下过氧化氢分解得很慢,只能产生极少量的氧气
试管内产生大量气泡,带火星的木条复燃
二氧化锰不能分解产生氧气
有大量氧气生成,二氧化锰能促进过氧化氢分解
有大量氧气生成,反应后二氧化锰的化学性质没有发生改变
在有二氧化锰存在的条件下,过氧化氢能更快地分解产生氧气
讨论与交流>>>1.比较上述几个实验,过氧化氢在什么条件下更容易分解放出氧气?
过氧化氢在有二氧化锰存在的条件下更容易分解放出氧气。
讨论与交流>>>2.上述【实验3-5】(4)可以重复多次,而且若在实验前准确称出二氧化锰的质量,实验后将二氧化锰回收、干燥、再称量,会发现它的质量没有改变。根据这个事实,你对二氧化锰所起的作用有什么看法?
二氧化锰能促进过氧化氢分解,它的质量和化学性质在反应前后都不变。
思路与方法导引>>>对比实验 对比实验是指设置两个或两个以上的实验组,通过对结果的比较分析,来探究各种因素与实验对象的关系。每次只能改变一个因素,除了改变的那个因素外,其他因素应该保持一样。如[实验3-5](1)和(3)中产生氧气的速率不同,在这一组实验中,除了有无二氧化锰外,过氧化氢溶液的浓度和体积均相同。通过对实验结果的比较分析,可以知道二氧化锰能加速过氧化氢溶液的分解,这样的实验方法称为对比实验。
此外,实验室还用在二氧化锰催化作用下加热氯酸钾的方法制取氧气。 文字表达式是:
现在你已经学习了三种实验室制取氧气的方法,请完善下表。回顾用高锰酸钾制取氧气的实验装置,设计一套用氯酸钾制取氧气的装置。
讨论与交流>>>1.请比较:实验室制取氧气的三种反应中,除了生成物都有氧气之外,还有什么其他共同之处?
反应物都是一种,生成物都是两种或两种以上。
讨论与交流>>>2.与上节所学的化合反应对比,本节所学的三种制取氧气的化学反应有什么不同特点?
化合反应的反应物是两种或两种以上,生成物只有一种;本节所学的三种制氧气的化学反应的反应物只有一种,生成物是两种或两种以上。
分解反应:由一种物质生成两种或两种以上其他物质的反应。
分解反应与化合反应的比较
实验室制取氧气的方法不适合工业生产的要求。工业上制备大量氧气时,需要考虑成本是否便宜,原料是否容易获得,生产对环境有无负面影响等。从这些角度考虑,利用空气中丰富的氧气资源是很划算的,如果能把氧气与氮气分开,不仅能得到较纯净的氧气,还能得到较纯净的氮气。 怎样才能将空气中的氧气和氮气分离开呢?
液化空气制氧气是工业上常用的方法。已知液氮的沸点是-196℃,液氧的沸点是-183℃,所以当空气液化后,适当升温到-196℃至-183℃之间,液氮即汽化为氮气,而剩下的主要就是液氧了。为了常温贮存、运输和使用,工厂将液态氧汽化成为氧气,用150倍大气压强的气压加以压缩后,贮存于钢瓶里。你如果在医院或气焊的工厂里,看到外壳漆蓝色的钢瓶,那就是氧气瓶。
利用膜分离技术富集空气中的氧气,是近年来出现的新方法。在一定压力下,让空气通过具有氧气富集功能的薄膜,反复进行多级分离,便可得到含氧气90%以上的富氧空气,它在医疗、化工、炼钢、发酵等方面都有广泛的应用。
1.过氧化氢溶液俗称双氧水。向一定浓度的过氧化氢溶液中加一些二氧化锰,立即产生氧气,下列说法正确的是( )A.过氧化氢中含有水和氧气B.过氧化氢使二氧化锰分解产生氧气C.反应物有过氧化氢和二氧化锰,不属于分解反应D.二氧化锰促进过氧化氢分解出氧气和水
2.《抱朴子·金丹篇》记载:“丹砂(HgS)烧之成水银(Hg) ,积变又还成丹砂。”下列说法错误的是( )A.“水银”是指金属汞B.“烧之”说明该反应需要加热C.“丹砂烧之成水银”是分解反应D.“积变又还成丹砂”是物理变化
4.从微观角度可以认识化学变化的实质,下图所示为_______(填“化合”“分解”或“氧化”)反应。
科粤版九年级上册3.2 制取氧气备课ppt课件: 这是一份科粤版九年级上册<a href="/hx/tb_c91785_t3/?tag_id=26" target="_blank">3.2 制取氧气备课ppt课件</a>,文件包含第1课时高锰酸钾制氧气pptx、高猛酸钾制氧气mp4等2份课件配套教学资源,其中PPT共29页, 欢迎下载使用。
初中化学科粤版九年级上册第三章 维持生命之气——氧气3.2 制取氧气课文内容ppt课件: 这是一份初中化学科粤版九年级上册第三章 维持生命之气——氧气3.2 制取氧气课文内容ppt课件,文件包含32制取氧气pptx、32制取氧气docx、32制取氧气课时1docx、32制取氧气课时2docx、补充习题32制取氧气docx等5份课件配套教学资源,其中PPT共48页, 欢迎下载使用。
2021学年3.2 制取氧气教案配套课件ppt: 这是一份2021学年3.2 制取氧气教案配套课件ppt,共24页。PPT课件主要包含了氧气的实验室制法,仪器的连接,分解反应,多变一化合反应,课堂小结,课堂测评等内容,欢迎下载使用。













