

内蒙古自治区赤峰市2024届高三下学期三模理科综合高中化学试卷(含答案)
展开
这是一份内蒙古自治区赤峰市2024届高三下学期三模理科综合高中化学试卷(含答案),共16页。试卷主要包含了单选题,填空题,实验题等内容,欢迎下载使用。
一、单选题
1.化学与人体健康和生产生活关系密切。下列说法正确的是( )
A.由于有毒,故不能用作食品添加剂
B.我国自主研发的“龙芯”芯片的主要材料是
C.汽油燃烧产物会引起“光化学烟雾”、“酸雨”等环境问题
D.“玉龙之乡”赤峰因红山而得名,红山的岩石因含而呈红色
2.阿司匹林是一种应用较广泛的消炎、解热、镇痛药物,可由柳树皮中的水杨酸与乙酸酐通过下列反应制得,下列说法错误的是( )
A.乙酰水杨酸的分子式为
B.乙酰水杨酸分子中含有三种官能团
C.水杨酸能发生氧化、加成、酯化反应
D.以上四种物质均能与NaOH发生反应
3.下列生产生活中涉及的反应方程式正确的是( )
A.用制备
B.用食醋和淀粉-KI溶液检验加碘盐中的
C.工业制硫酸时黄铁矿在足量氧气中煅烧:
D.通入石灰乳中制漂白粉:
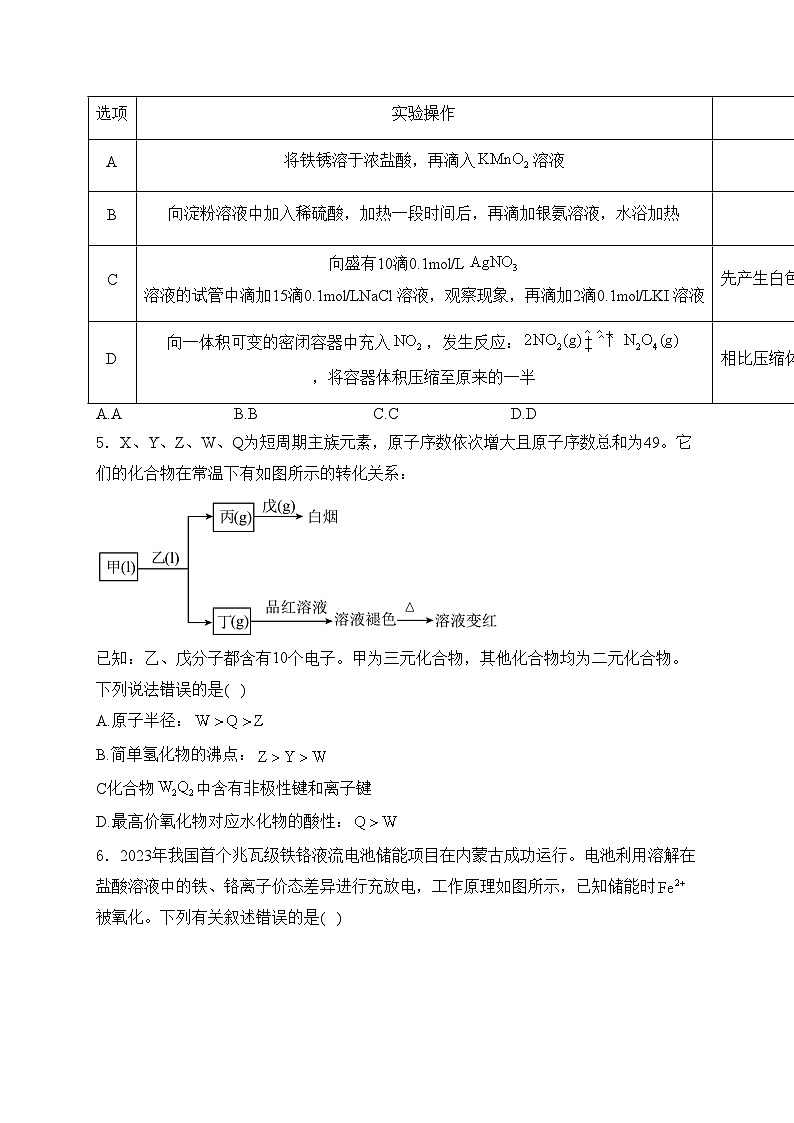
4.下列实验操作、现象及结论都正确的是( )
A.AB.BC.CD.D
5.X、Y、Z、W、Q为短周期主族元素,原子序数依次增大且原子序数总和为49。它们的化合物在常温下有如图所示的转化关系:
已知:乙、戊分子都含有10个电子。甲为三元化合物,其他化合物均为二元化合物。下列说法错误的是( )
A.原子半径:
B.简单氢化物的沸点:
C化合物中含有非极性键和离子键
D.最高价氧化物对应水化物的酸性:
6.2023年我国首个兆瓦级铁铬液流电池储能项目在内蒙古成功运行。电池利用溶解在盐酸溶液中的铁、铬离子价态差异进行充放电,工作原理如图所示,已知储能时被氧化。下列有关叙述错误的是( )
A.接风力发电时,铁铬液流电池在储备能量
B.接输电网时该电池总反应为
C.若用该电池电解水,生成标况下22.4L时,有2ml被氧化
D.放电时,移向b极,每1ml通过交换膜,减少1ml
7.常温下,向20mL0.1ml/L溶液中缓慢加入少量易溶于水的粉末(已知难溶,忽略溶液体积变化),溶液中与变化关系如图所示。已知:。下列说法错误的是( )
A.a点溶液的pH约为5
B.从a点到c点,逐渐减小
C.b点溶液中,
D.c点溶液中,=0.1ml/L
二、填空题
8.近年来,废旧锂离子电池的回收成为目前新能源产业重要的发展方向。某锂离子二次电池的正极材料主要为,还含有少量Al、Fe、Mn、Ni的化合物。通过如图所示的流程利用废旧锂离子电池制备草酸钴晶体,回答下列问题:
已知该工艺条件下,有关金属离子沉淀完全的pH如表:
(1)中C的化合价为___________,“酸浸还原”中转化为,氧化产物是,该反应中氧化剂与还原剂的物质的量之比为___________。
(2)“水解净化”的滤渣主要成分为___________(填化学式)。
(3)“氧化沉铁锰”的操作为控制体系的pH在4~5,加入NaClO溶液。其中转化为的离子方程式为___________;实际生产中,随着反应时间的延长,锰和铁的沉淀率逐渐增大,但钴的损失量也随之增大,可能的原因是___________。
(4)利用“P507萃取剂”从“滤液”中分离萃取时,C、Ni的萃取率和C/Ni分离因素与水相pH的关系如图所示。
C/Ni分离因素越大,表明萃取剂对C/Ni分离效果越好。由图可知,萃取时的最佳水相pH为___________(填字母)。
A.2.5B.3.0C.3.5D.4.0
(5)“沉钴”时反应的化学方程式为___________。
9.氢能新质生产力正加速发展。工业上利用天然气制备氢气,还能得到乙烯、乙炔等化工产品,有关反应原理如下:
反应①;
反应②:;
回答下列问题:
(1)反应③:___________kJ/ml,=___________(用含、的代数式表示)。
(2)若用、、和表示和固体催化剂,如图在催化剂表面进行反应①,从吸附到解吸的过程中,能量状态最高的是___________(填字母)。
(3)反应②的速率方程为(为正、逆反应速率常数)。其他条件相同,℃达到平衡时,℃达到平衡时。由此推知,__________(填“>”“Cl>O,A正确;
B.由于水中分子间氢键数目大于氨气中分子间氢键数目,硫化氢中无氢键,所以简单氢化物的沸点:,B正确;
C.化合物中不含离子键,C错误;
D.非金属性Cl>S,所以最高价氧化物对应水化物的酸性,D正确;
故选C。
6.答案:B
解析:A.接风力发电时,该装置是电解池,铁铬液流电池在储备能量,A正确;
B.接输电网时该装置是原电池,该电池总反应为,B错误;
C.若用该电池电解水,生成标况下22.4L时,氢气的物质的量为1ml,转移电子2ml,该装置为原电池,负极电极反应式为:,所以有2ml被氧化,C正确;
D.放电时,该装置是原电池,Cl⁻是阴离子,移向负极,b极是负极,每1ml通过交换膜,转移1ml电子,减少1ml,D正确;
故选B。
7.答案:D
解析:D.由物料守恒可知,c点除了溶液中含硫元素外,沉淀MS中也含硫元素,C>H(或O、N、C、H);大于
(4)c;
解析:(1)铜元素位于元素周期表ds区;Fe元素是第26号元素,失去2个电子后形成,基态的价层电子排布图;
(2)气态三氧化硫以单分子形式存在,结合价层电子对互斥模型分析可知S有三对价层电子,推测其分子的立体构型为为平面三角形;固体三氧化硫中存在如图b所示的三聚分子,可知S成四根键为四面体空间构型,该分子中S原子的杂化轨道类型为。
(3)①所含非金属元素为O、N、C、H,电负性由大到小的顺序为O>N>C>H;②由图可知,配离子中水分子中的氧原子与铜离子形成配位键,氧原子的孤对电子对数由2变为1,孤对电子对数越多,对成键电子对的斥力越大,键角越小,则配离子中H—O—H的键角大于水分子,
(4)①所在晶胞的位置为在c位,由均摊法计算可得该结构中的数目为2,的数目为4,根据电荷守恒可得的数目为1,所以应该在c位;
②二价铁位于体心和棱心,则一共有1+12×=4个;三价铁位于顶点和面心,一共有=4个,晶胞中有4个钾离子,根据电荷守恒可知,有4+4×2+4×3=24,其化学式为:。
11.答案:(1)羟基、羧基;取代反应(或酯化反应)
(2)
(3)使在指定的羟基上发生取代(或保护特定位置的羟基)
(4)
(5)3
(6)8;
解析:(1)根据A的结构简式,A中含氧官能团为羟基和羧基;A与乙醇发生酯化反应生成B,故反应类型为取代反应或酯化反应;
(2)根据分析,化合物B的结构简式为;
(3)设计该反应的目的是使在指定的羟基上发生取代(或保护特定位置的羟基);
(4)根据分析,反应③的化学方程式为:;
(5)有机物E中的手性碳为,共3个。
12.答案:(1)三颈烧瓶(或三口烧瓶);除去中混有的HCl(或除去HCl);(作安全瓶)防倒吸
(2)排出装置内的空气,防止干扰实验
(3)温度过高,硫脲会部分发生异构化反应;温度过低,反应速率缓慢;将装置内残留的全部排入到E中被吸收,防止污染空气
(4)(或等可溶性铁盐)
(5)
(6)(或)
解析:(1)仪器a的名称是三颈烧瓶;装置B中饱和NaHS溶液的作用是除去中混有的HCl;装置C的作用为安全瓶,防止倒吸;
(2)由于易被氧化,通入一段时间,目的是排出装置内的空气,防止空气干扰实验;
(3)根据已知信息,温度过高,硫脲会部分发生异构化反应;温度过低,反应速率缓慢;因会污染空气,则待D中反应结束后,关闭,打开,通入一段时间,目的是将装置内残留的全部排入到E中被吸收,防止污染空气;
(4)证明反应过程中硫脲发生异构化生成了,即检验是否有离子即可,所以可以用或等可溶性铁盐检验,然后观察溶液是否变为红色;
(5)由分析可知,装置E用溶液吸收多余的,防止污染空气,即与反应生成CuS沉淀和,其反应的离子方程式为:;
(6)用标准溶液滴定,滴定至终点时消耗标准溶液,消耗的物质的量为,根据反应:可知,mg产品中的物质的量为=,则样品中硫脲的质量分数为=。
选项
实验操作
现象
结论
A
将铁锈溶于浓盐酸,再滴入溶液
紫色褪去
铁锈中含有二价铁
B
向淀粉溶液中加入稀硫酸,加热一段时间后,再滴加银氨溶液,水浴加热
未产生银镜
淀粉未发生水解
C
向盛有10滴0.1ml/L溶液的试管中滴加15滴0.1ml/LNaCl溶液,观察现象,再滴加2滴0.1ml/LKI溶液
先产生白色沉淀,后产生黄色沉淀
D
向一体积可变的密闭容器中充入,发生反应:,将容器体积压缩至原来的一半
相比压缩体积之前,气体颜色变浅
增大压强,平衡向气体分子数减小的方向移动
离子
pH
9.3
3.2
9.0
4.7
10.1
8.9
相关试卷
这是一份2024山西省太原市高三下学期三模考试理科综合试卷-高中化学(原卷版+解析版),文件包含2024山西省太原市高三下学期三模考试理科综合试卷-高中化学原卷版docx、2024山西省太原市高三下学期三模考试理科综合试卷-高中化学解析版docx等2份试卷配套教学资源,其中试卷共27页, 欢迎下载使用。
这是一份2024届内蒙古自治区包头市高三下学期三模理科综合试题-高中化学(原卷版+解析版),文件包含2024届内蒙古自治区包头市高三下学期三模理科综合试题-高中化学原卷版docx、2024届内蒙古自治区包头市高三下学期三模理科综合试题-高中化学解析版docx等2份试卷配套教学资源,其中试卷共31页, 欢迎下载使用。
这是一份2024届内蒙古自治区赤峰市高三下学期三模理科综合试题-高中化学(原卷版+解析版),文件包含2024届内蒙古自治区赤峰市高三下学期三模理科综合试题-高中化学原卷版docx、2024届内蒙古自治区赤峰市高三下学期三模理科综合试题-高中化学解析版docx等2份试卷配套教学资源,其中试卷共24页, 欢迎下载使用。








