




初中化学人教版(2024)九年级上册课题2 原子结构课文ppt课件
展开
这是一份初中化学人教版(2024)九年级上册课题2 原子结构课文ppt课件,共57页。PPT课件主要包含了48cm,原子的构成,不带电,第一层,第二层,第三层,原子结构示意图,资料卡片,核外电子排布规律,最外层等内容,欢迎下载使用。
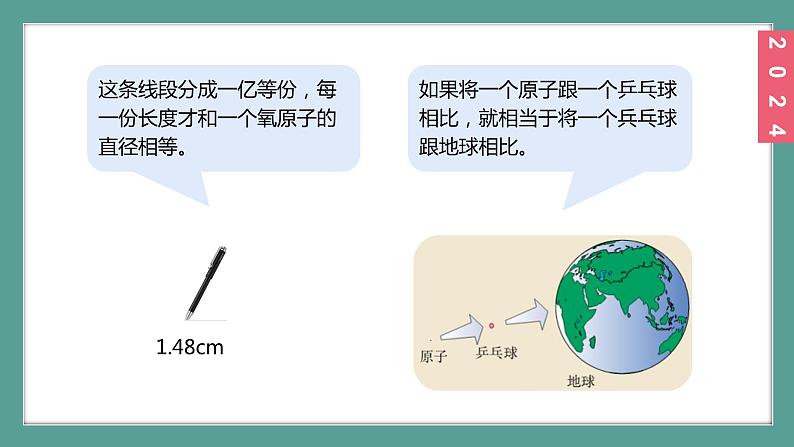
原子的体积很小。如果将一个原子与一个乒乓球相比,就相当于将一个乒乓球与地球相比。原子能够结合成分子的奥秘,正是人们在研究这小小的原子的结构时被逐步揭示出来的。
这条线段分成一亿等份,每一份长度才和一个氧原子的直径相等。
如果将一个原子跟一个乒乓球相比,就相当于将一个兵乓球跟地球相比。
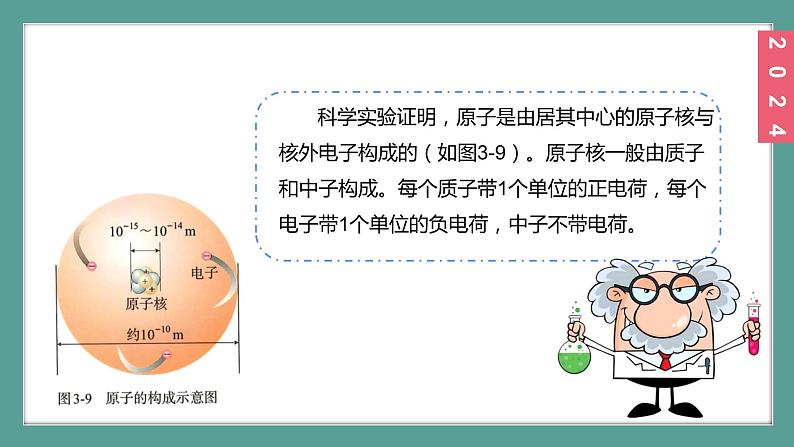
科学实验证明,原子是由居其中心的原子核与核外电子构成的(如图3-9)。原子核一般由质子和中子构成。每个质子带1个单位的正电荷,每个电子带1个单位的负电荷,中子不带电荷。
(每个电子带1个单位的负电荷)
(每个质子带1个单位的正电荷)
由于原子核内质子所带正电荷与核外电子所带负电荷数量相等、电性相反,所以原子不显电性。可见,原子核所带的正电荷数(核电荷数)就等于核内质子数,也等于核外电子数。
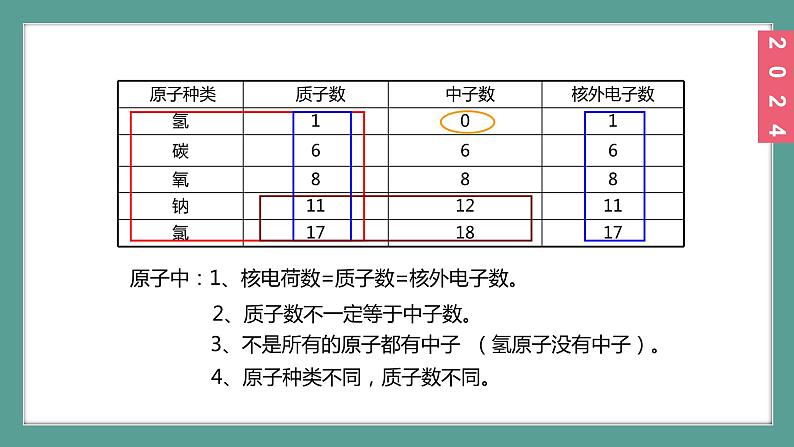
原子中:1、核电荷数=质子数=核外电子数。 2、质子数不一定等于中子数。
3、不是所有的原子都有中子 (氢原子没有中子)。
4、原子种类不同,质子数不同。
钠原子(11个电子)
(1)第一层最多排 个, 第二层最多排 个, 最外层电子数不超过 个, (第一层为最外层时,不超过 个)。(2)核外电子总是先排在离核较近的电子层,排满第一层,再依次排第二层,第三层。
最外层具有8个电子(只有一个电子层的具有2个电子)的结构,属于相对稳定结构。
稀有气体原子的原子结构示意图
金属原子的原子结构示意图
金属原子最外层电子一般少于4个,在化学反应中易失去电子,形成相对稳定结构。
非金属原子的原子结构示意图
非金属原子最外层电子一般不少于4个,在化学反应中易得到电子,形成相对稳定结构。
原子的化学性质与最外层电子数关系密切
以钠与氯气的反应为例。钠原子的最外层有1个电子,氯原子的最外层有7个电子。当钠与氯气反应时,钠原子最外层的1个电子转移到氯原子的最外层,使两者都形成相对稳定的结构(如图3-12)。
氯化钠(NaCl)的形成过程
离子:带电的原子(或原子团)。 阳离子:带正电的原子(或原子团) 阴离子:带负电的原子(或原子团)
离子也是构成物质的一种粒子。
在元素符号的右上角标出离子所带的电荷数,数值在前,正、负号在后。当离子带1个单位的正电荷或1个单位的负电荷时,“1” 可以省略不写。 如:Na+ Mg2+ Cl- O2-
练习 说出下符号的意义:
表示一个镁离子带2个单位的正电荷
原子中: 核电荷数 质子数 核外电子数阳离子: 核电荷数 质子数 核外电子数阴离子: 核电荷数 质子数 核外电子数
练习:判断下列哪些是原子、哪些是离子?
原子的质量很小。例如,1个氢原子的质量约为1.67×10-27kg,1个氧原子的质量约为2.66×10-26kg。由于原子质量的数值太小,书写和使用都不方便,
一个氢原子的质量是:一个氧原子的质量是: 一个铁原子的质量是:
0.00000000000000000000000000167千克
0.00000000000000000000000002657千克
0.00000000000000000000000009288千克
即1.67×10-27千克
即2.657×10-26千克
即9.288×10-26千克
原子的质量很小,记忆、计算都很不方便,怎么办?
国际上一致同意采用相对质量(如图3-13)。以一种碳原子①质量的为标准,其他原子的质量与它相比,得到相对原子质量(符号为A,)。根据这个标准,氢的相对原子质量约为1,氧的相对原子质量约为16。
以一种碳原子质量的1/12(1.66×10-27kg)为标准,其他原子的质量跟它相比较所得到的比,作为这种原子的相对原子质量(符号为Ar )。
一个碳12原子的实际质量
找规律:阅读上表,你能得到什么信息?
在原子中,核电荷数=核内质子数=核外电子数
跟质子、中子相比,电子质量很小,约为质子质量的1/1836,通常忽略不计,原子的质量主要集中在原子核上。质子和中子的质量跟相对原子质量标准相比较,均约等于1。
相对原子质量≈质子数+中子数
如表3-2所示,构成原子的质子、中子的相对质量都约等于1;与质子、中子相比,电子的质量很小,整个原子的质量主要集中在原子核上。在一般的化学计算中,多采用相对原子质量的近似值(如表3-3)。相对原子质量可从书后附录Ⅱ中查到。
张青莲与相对原子质量的测定 中国科学院院士张青莲教授(如图3-14)为相对原子质量的测定作出了卓越贡献。他于1983年当选为国际纯粹与应用化学联合会原子量与同位素丰度委员会委员。他主持测定的钢、依、锑、铕、铈、铒、锗、镝、锌的相对原子质量数据被确认为国际标准。
模型:氢分子、氧原子等的模型可以将微观粒子直观、生动地呈现在我们面前。构建和利用模型认识物质及其变化规律是一种常用的科学方法。 模型是对原型的模拟,构建模型应以客观事实为依据,符合科学原理,通过类比、简化和抽象等方法突出原型的主要特征。化学中常用的模型主要有实物模型、理论模型和符号模型等。利用这些模型能帮助我们描述、解释和预测物质及其变化。随着人们对原型认识的不断深入,模型也会发生改变。
科学史话 原子模型的演变
(2)汤姆孙原子模型19世纪末,英国物理学家汤姆孙(J. J. Thmsn,1856—1940)通过一系列实验发现了电子。在此基础上,他提出了一种原子模型,认为正电荷均匀分布在整个原子内,带负电荷的电子镶嵌其中。
方法点拨:核电荷数=质子数=核外电子数。
A.原子由核外电子和原子核构成 B.原子由原子核和中子构成C.原子由质子和电子构成 D.原子由质子和中子构成
下列关于原子的叙述正确的是( )
方法点拨:原子是由原子核和核外电子构成的。
方法点拨:在原子中,核内质子数等于各电子层上的电子数之和,可以据此判断原子结构示意图。
请画出氯原子,镁原子,氧原子的原子结构示意图。
1.如果该图表示的是原子,x 值为_____,2.该原子的电子层数有______层。
根据原子结构示意图回答下列问题。
是某原子的结构示意图,下列关于该原子的描述正确的是
A.容易得到电子B.属于非金属原子C.核电荷数为11D最外层电子数为11
如图为某原子结构模型的示意图,其中a、b、c是构成该原子的三种不同粒子,下列说法正确的是
A.决定该原子种类的粒子是bB.原子中b与c的数目一定相同C.原子中a与c的数目一定相同D.原子的质量集中在a和c上
(1)具有相对稳定结构的是 (填序号,下同);(2)属于金属原子的是 ;(3)属于稀有气体原子的是 。
根据下列原子的结构示意图,回答下列问题:
图中A、B、C、D是四种粒子的结构示意图,请回答下列问题。
(1)A中x=______;A粒子属于______。(填“原子”或“离子”)(2)由B粒子的结构示意图可知,B粒子的名称是________。(3)以上四种结构示意图所表示的粒子中,表示离子的是________(填字母)。
分析钠原子、钠离子的结构示意图得到的以下说法中,错误的是( )
A.钠原子有3个电子层,钠离子有2个电子层B.钠原子、钠离子的质子数都为11C.1个钠原子在化学反应中可失去1个电子 D.钠原子和钠离子的中子数不同
最近,俄罗斯科学家宣布他们通过核反应合成了核电荷数为114、相对原子质量为289的超重元素原子,该原子内质子数为 ,中子数为 ,核外电子数为 。
将答案填写在题中划线处:
铁的相对原子质量为56,它表示( )
A.铁的质量为56gB.1个铁原子的质量为56gC.铁的原子核内有56个质子D.1个铁原子的质量是1个碳12原子质量1/12的56倍
铀235(其原子核内有92个质子,相对原子质量为235)是核电站的主要燃料。下列有关说法正确的是( )
A.该原子的相对原子质量等于质子数和中子数之和B.该原子的核电荷数为92C.该原子核内有51个中子D.该原子核外有143个电子
解析:铀的相对原子质量约等于质子数与中子数之和;铀235原子核内有92个质子,在原子中,核电荷数=核内质子数=核外电子数,则该原子的核电荷数为92,该原子核外有92个电子;铀235原子核内有92个质子,相对原子质量为235,该原子核内有235-92=143个中子。
根据氯离子的结构示意图(如图所示),判断以下说法错误的是( )
A.氯离子核内有17个质子B.氯离子核外有3个电子层C.氯离子在化学反应中易得到电子 D.氯离子的符号为Cl-
解析:氯原子得到1个电子形成具有相对稳定结构的氯离子,在化学反应中不再易得到电子。
2.原子中的核外电子是分层排布的,可以用原子结构示意图表示。3.构成物质的微观粒子除了原子、分子,还有离子。带电荷的原子叫作离子。4.以一种碳原子质量的为标准,其他原子的质量与它相比,得到相对原子质量。
相关课件
这是一份人教版(2024)九年级上册课题2 水的组成教案配套ppt课件,共30页。PPT课件主要包含了水的组成,课题2,情景素材1,情景素材2,情景素材3,氢气的性质,向下排空气,排水法,化学性质,可燃性等内容,欢迎下载使用。
这是一份人教版(2024)九年级上册课题2 原子结构示范课ppt课件,共18页。PPT课件主要包含了核外电子分层排布,合作探究,离子的形成,带电的原子或原子团,电荷数,省略不写,正负号,⑵数字的意义,一个氧离子,一个铝离子等内容,欢迎下载使用。
这是一份初中化学人教版(2024)九年级上册课题2 原子结构课前预习ppt课件,共20页。PPT课件主要包含了原子的构成,原子很小,合作探究,原子结构的发现,原子的结构,粒子带电情况分析,不带电,电荷守恒的原因,质子数,电子数等内容,欢迎下载使用。










