




浙江省七彩阳光新高考研究联盟2023-2024学年高二下学期4月期中联考化学试题(Word版附解析)
展开
这是一份浙江省七彩阳光新高考研究联盟2023-2024学年高二下学期4月期中联考化学试题(Word版附解析),文件包含浙江省七彩阳光新高考研究联盟联考2023-2024学年高二下学期4月期中考试化学试题Word版含解析docx、浙江省七彩阳光新高考研究联盟联考2023-2024学年高二下学期4月期中考试化学试题Word版无答案docx等2份试卷配套教学资源,其中试卷共32页, 欢迎下载使用。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Cr-52 A1-27 Cu-64 Cl-35.5 Ag-108
选择题部分
一、选择题(本大题共16小题,每小题3分,共48分。每小题列出的四个备选项中只有一个是符合题目要求的,不选、多选、错选均不得分)
1. 下列物质属于电解质的是
A. CuB. 盐酸C. D.
2. 碳酸氢钠常用作食用碱或工业用碱,下列说法不正确的是
A. 向碳酸氢钠固体中加入少量水后,会出现放热现象
B. Na元素位于周期表s区
C. 中C原子的杂化类型为sp杂化
D. 碳酸氢钠溶液呈碱性是因为碳酸氢根离子的电离程度小于水解程度
3. 下列表示不正确的是
A. HCl的形成过程:
B. 的VSEPR模型:
C. 的空间结构: (平面三角形)
D. 硅的基态原子轨道表示式:
4. 关于反应,下列说法正确的是
A. 生成,转移电子B. 发生氧化反应
C. 还原产物与氧化产物的物质的量之比为1:4D. 若设计成原电池,为负极产物
5. 在溶液中能大量共存的离子组是
A. B.
C. D.
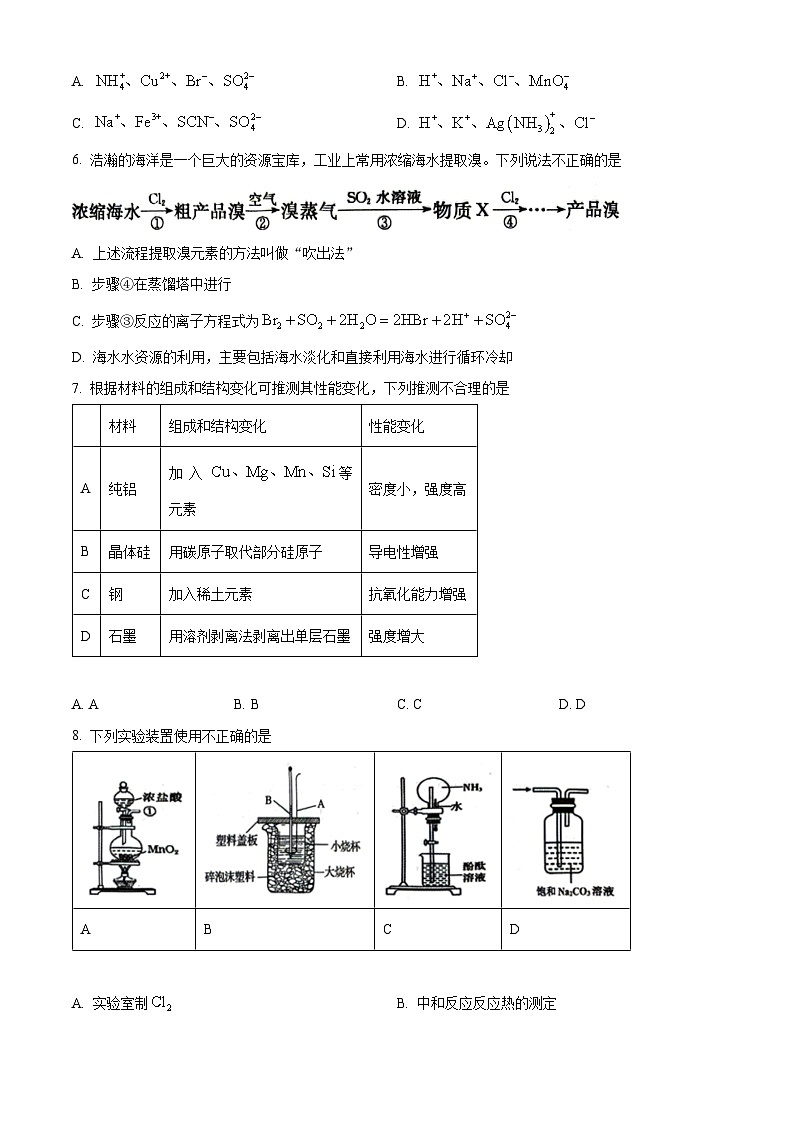
6. 浩瀚的海洋是一个巨大的资源宝库,工业上常用浓缩海水提取溴。下列说法不正确的是
A. 上述流程提取溴元素的方法叫做“吹出法”
B. 步骤④在蒸馏塔中进行
C. 步骤③反应的离子方程式为
D. 海水水资源的利用,主要包括海水淡化和直接利用海水进行循环冷却
7. 根据材料的组成和结构变化可推测其性能变化,下列推测不合理的是
A. AB. BC. CD. D
8. 下列实验装置使用不正确的是
A. 实验室制B. 中和反应反应热的测定
C. 验证易溶于水且水溶液呈碱性D. 除去中混有的少量HCl
9. 关于物质的检验,下列说法正确的是
A. 将海带灰浸出液过滤,在滤液中加入氯水,再滴几滴淀粉溶液,溶液呈蓝色,说明海带中含有碘单质
B. 向某溶液中滴加浓盐酸,将产生的气体通入石蕊溶液,溶液先变红后褪色,说明溶液中含有或者
C. 向某溶液中滴加溶液,加热产生能使湿润蓝色石蕊试纸变红的气体,说明溶液中含有
D. 向某无色溶液中加稀盐酸酸化,无明显现象,再加入氯化钡溶液,若有白色沉淀生成,说明溶液中含有
10. 下列化学反应与方程式不相符的是
A. 溶液中滴加少量的溶液:
B. 食醋去除水垢中的
C. 利用覆铜板制作印刷电路板:
D. 乙醇在有催化剂的条件下被氧气氧化:
11. 金属硫化物催化反应,既可以除去天然气中的,又可以获得。下列说法正确的是
A. 该反应的
B. 该反应的平衡常数
C. 题图所示的反应机理中,步骤Ⅰ可理解为中的与催化剂中的之间发生作用
D. 加入催化剂,可提高的去除速率和转化率
12. 前四周期元素W、X、Y、Z的原子序数依次增大,且都不在同一周期。X的价电子排布式为nsxnpx+1,Y的最高能级的单电子数是W的3倍,Z与W中的单电子数和最外层电子数均相同,但两者族序数不同。下列说法不正确的是
A. Y原子核外电子有9种空间运动状态
B. X元素的第一电离能高于其相邻元素
C. X的简单氢化物比Y的简单氢化物键角大
D. Z元素在周期表中的位置可能为第四周期第VIB族
13. 高氯酸在化工生产中有广泛应用,工业上以为原料制备高氯酸的原理如图所示。
下列说法正确的是
A. 上述装置中,e极为光伏电池的负极B. a、b处均通入溶液
C. d处得到较浓的溶液,c处得到溶液D. 若转移电子,理论上生成
14. 二氧化碳加氢制甲烷过程中的主要反应为
在密闭容器中,、时,平衡转化率、在催化剂作用下反应,相同时间所测得的实际转化率随温度的变化如题图所示,的选择性可表示为:。
下列说法不正确的是
A. 反应的焓变
B. 的平衡转化率随着温度的升高而增加
C. 用该催化剂催化二氧化碳反应的最佳温度范围约为350~400℃
D. 450℃时,提高的值或增大压强,均能使平衡转化率达到X点的值
15. 25℃时,和在水中达沉淀溶解平衡时关系图,(可认为M离子沉淀完全)。
下列叙述正确的是
A. 由a点可求得
B. 时的溶解度为
C. 浓度均为的和可通过分步沉淀进行分离
D. 混合溶液中时二者不会同时沉淀
16. 根据实验目的设计方案并进行实验,观察到相关现象,其中方案设计和结论都正确的是
A. AB. BC. CD. D
非选择题部分
二、非选择题部分(共5题,共52分)
17. 锌在工业中有重要作用,也是人体必需的微量元素。请回答:
(1)基态的价层电子排布式_______,中阴离子空间结构为_______。
(2)下列说法正确的是_______。
A. 电负性:B. 离子半径:
C. Fe位于元素周期表的第四周期第Ⅷ族D. Cr在元素周期表中处于d区
(3)已知:和的熔点数据如下表:
熔点明显高于,原因是_______。
(4)的晶胞形状为长方体,边长分别为anm、bnm、cnm,结构如图所示。
晶胞中的个数为_______。已知的摩尔质量是,阿伏加德罗常数为,该晶体的密度为_______。()
18. 砷的化合物可用于半导体领域,如我国“天宫”空间站的核心舱“天和号”就是采用砷化镓薄膜电池来供电。一种从酸性高浓度含砷废水[砷主要以亚砷酸()形式存在]中回收砷的工艺流程如下:
已知:Ⅰ.
Ⅱ.
Ⅲ.砷酸()在酸性条件下有强氧化性
Ⅳ.,
请回答:
(1)从含砷废水到滤液Ⅰ,浓度明显减小的阳离子为__________(用离子符号表示)。
(2)下列说法正确的是__________。
A. 沉砷时产生的废气可用溶液吸收处理
B. 酸化的目的是增加价砷的氧化性
C. 浸取后所得滤渣的主要成分是,不含
D. 酸性:
(3)“沉砷”过程中是否可用过量的替换__________(填“是”或“否”);请从平衡移动的角度解释原因__________。
(4)砷酸“还原”过程中发生的化学方程式为__________。还原后溶液需检验是否仍剩余砷酸,设计检验实验方案__________。
19. 固体化合物X由3种元素组成,某学习小组开展如下探究实验。
已知:白色沉淀B能溶于溶液。请回答:
(1)白色固体C的化学式是_______,化合物X的化学式是_______。
(2)写出A转化为B的离子方程式_______。
(3)下列说法正确的是_______。
A. 白色溶液E可溶于氨水
B. 加入足量氨水后形成的深蓝色溶液是因为有配合物生成,其中氨气中氮原子提供空轨道
C. 蓝色溶液D的溶质有3种
D. 白色沉淀B具有两性
(4)蓝色溶液A与作用,溶液蓝色褪去,同时生成易溶于硝酸的白色沉淀F。设计实验检验白色沉淀F中的组成元素_______。
20. 利用电化学方法可以将CO2有效地转化为HCOO-(其中C元素化合价为+2价),装置如图所示。
(1)在该装置中,右侧Pb电极反应为_______。
(2)一定条件下,水气变换反应CO+H2OCO2+H2的中间产物是HCOOH。为探究该反应过程,研究HCOOH水溶液在密封石英管中的分解反应:
Ⅰ:HCOOHCO+H2O (快)
Ⅱ:HCOOHCO2+H2 (慢)
研究发现,在反应Ⅰ、Ⅱ中,H+仅对反应Ⅰ有催化加速作用;反应Ⅰ速率远大于反应Ⅱ,近似认为反应Ⅰ建立平衡后始终处于平衡状态。忽略水的电离,其浓度视为常数。回答下列问题:
①一定条件下水气变换反应焓变_______(用含、的代数式表示)。
②反应I正反应速率方程为:,k为反应速率常数。T1温度下,HCOOH电离平衡常数为Ka,当HCOOH平衡浓度为时,此时反应Ⅰ速率_______ (用含Ka、x和k的代数式表示)。
(3)反应Ⅲ:CO+H2OHCOOH且在恒温、恒容的密闭容器中进行,采用充分搅拌催化剂M的DMSO(有机溶剂)溶液,使CO2和H2在该溶液中反应制备HCOOH,反应过程中保持CO2和H2压强不变,反应速率为,反应机理如下列三个基元反应,各反应的活化能。
Ⅳ:
V:
Ⅵ:
①催化剂M足量的条件下,下列说法正确的是_______。
A.反应Ⅳ是总反应的决速反应 B.与溶液中溶解的CO2浓度有关
C.温度升高,反应速率一定增大 D.催化剂可以降低反应的活化能,加快反应速率
②该总反应随催化剂浓度的增加,反应速率先增大后保持不变,请解释原因_______。
21. 将和空气(不参与反应)按体积比1:3混合通入含水8%的中制备,并用水吸收 (不含)制备HClO溶液。实验装置如图。
已知:常温常压下、一氧化二氯()为棕黄色气体,沸点为3.8℃、42℃以上会分解生成和,易溶于水、并与水反应生成HClO。
(1)装置A中盛装浓盐酸的仪器名称是_______。
(2)各装置连接顺序为_______。
(3)下列说法正确的是_______。
A. 装置C的作用是吸收中的
B. 反应过程中装置B需放在冷水中
C. 相对用直接溶于水制备,此法的优点是制备的纯度高、浓度大
D. 工业上用装置A制,制得的中会混有HCl
(4)装置B中多孔球泡的作用是_______。
(5)写出B装置中制备的化学方程式_______。
(6)已知可被还原,用下列实验方案测定装置E所得溶液中的物质的量浓度:量取上述溶液,并稀释至,再从其中取出于锥形瓶中,用邻二氮菲作指示剂,并加入的标准溶液滴定至终点,消耗标准溶液,则原HClO溶液的浓度为_______。材料
组成和结构变化
性能变化
A
纯铝
加入等元素
密度小,强度高
B
晶体硅
用碳原子取代部分硅原子
导电性增强
C
钢
加入稀土元素
抗氧化能力增强
D
石墨
用溶剂剥离法剥离出单层石墨
强度增大
A
B
C
D
目的
方案设计
现象
结论
A
探究碘在不同溶剂中的溶解性
在装有碘的CCl4溶液的试管中加入等体积浓KI溶液,振荡
分层,下层由紫红色变浅,上层呈棕黄色
碘在浓KI溶液中的溶解能力小于在CCl4中的溶解能力
B
比较F﹣与SCN﹣结合Fe3+的能力
等物质的量浓度的KF和KSCN混合溶液中加入过量FeCl3溶液,振荡
溶液变红
结合Fe3+的能力:F﹣<SCN﹣
C
探究Cu(OH)2和Mg(OH)2Ksp大小
向NaOH溶液中加入一定量的MgCl2溶液,充分反应后再加少量的CuCl2溶液
先生成白色沉淀,后产生蓝色沉淀
Ksp大小:Cu(OH)2<Mg(OH)2
D
探究温度对反应速率的影响
等体积、等物质的量浓度的Na2S2O3与H2SO4溶液在不同的温度下反应
温度高的溶液中先出现浑浊
温度升高反应速率加快
物质
熔点/℃
800.7
相关试卷
这是一份浙江省七彩阳光新高考研究联盟2023-2024学年高三下学期返校考化学试题,文件包含浙江省七彩阳光新高考研究联盟2023-2024学年高三下学期返校考化学试题pdf、高三化学-参考答案评分细则pdf等2份试卷配套教学资源,其中试卷共11页, 欢迎下载使用。
这是一份浙江省“七彩阳光”新高考研究联盟2023-2024学年高一上学期期中化学试卷(Word版附解析),文件包含浙江省“七彩阳光”新高考研究联盟2023-2024学年高一上学期期中检测化学试卷原卷版docx、浙江省“七彩阳光”新高考研究联盟2023-2024学年高一上学期期中检测化学试卷Word版含解析docx等2份试卷配套教学资源,其中试卷共26页, 欢迎下载使用。
这是一份浙江省七彩阳光新高考研究联盟2023-2024学年高三化学上学期开学联考试题(Word版附解析),共23页。试卷主要包含了考试结束后,只需上交答题卷, 关于反应,下列说法正确的是, 下列反应的离子方程式正确的是, 下列说法不正确的是等内容,欢迎下载使用。









